
科目: 来源: 题型:
【题目】实验室可用环己醇(沸点:160.84℃,微溶于水)制备环己酮(沸点:155.6℃,微溶于水),使用的氧化剂可以是次氯酸钠、重铬酸钾等。

下列装置分别是产品的合成装置和精制装置示意图:

合成实验过程如下:
向装有搅拌器、滴液漏斗和温度计的三颈烧瓶中依次加入5.2 mL环己醇和25 mL冰醋酸。开动搅拌器,将40 mL次氯酸钠溶液逐渐加入到反应瓶中,并使瓶内温度维持在30~35℃,用磁性搅拌器搅拌5 min。然后,在室温下继续搅拌30 min后,在合成装置中再加入30 mL水、3g氯化铝和几粒沸石,加热蒸馏至馏出液无油珠滴出为止。回答下列问题:
(1)在合成装置中,甲装置的名称是__________________。
(2)三颈烧瓶的容量为____________(填“50 mL"、“100 mL”或“250 mL")。
(3)滴液漏斗具有特殊的结构,主要目的是__________。
(4)蒸馏完成后,向馏出液中分批加入无水碳酸钠至反应液呈中性为止,其目的是_________。然后加入精制食盐使之变成饱和溶液,其目的是________。再将混合液倒入分液漏斗中,分离得到有机层。
(5)有机层先加无水MgSO4,用如上右图对粗产品进行精制,加入无水MgSO4的作用是_____。检验精制后的坏己酮是否纯净,可使用的试剂为________________。
A.重铬酸钾溶液B.金属钠C.酚酞溶液 D.新制的氢氧化铜悬浊液
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子,在强碱性溶液中可以大量共存的是
A. K+ 、Fe3+、NO3- 、Cl- B. Ba2+ 、Na+ 、Cl- 、NO3-
C. NH4+、K+、NO3-、Cl- D. Na+ 、Al3+ 、Cl- 、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A.1mol水的质量为18g/mol
B.标准状况下,3.01×1023个CO2分子的质量为22g
C.标准状况下,1mol任何物质体积约为22.4 L
D.二氧化硫的摩尔质量是64 g
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的数值,则下列说法中正确的是( )
A.44gCO2所含质子数为44NA个
B.常温常压,11.2L氧气含原子数为NA个
C.2.3g钠变为离子失电子数0.1NA
D.常温常压下,NA个氢原子的质量为2g
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是工业上以有机物A、E为基本原料制备有机物M的一种合成路线.A能与Na2CO3溶液及溴水反应,且1molA最多可与2molBr2反应;B的苯环上有四种不同化学环境的氢原子;E、F均是芳香烃;M是一种具有特殊香气的物质。

已知: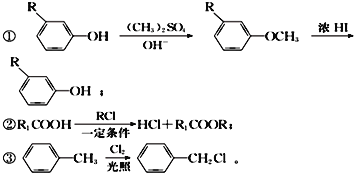
④酚羟基易被高锰酸钾酸性溶液、浓硝酸等氧化
回答下列问题:
(1)在F的同系物中,相对分子质量最小的物质是______(填名称);C中含氧官能团的名称为____________;
(2)A的结构简式为___________;E→F的反应类型为________;
(3)D+G→M的化学方程式为_____________________________;
(4)C的同分异构体中能同时满足下列条件的共有______种(不含立体异构);
①遇FeCl3溶液发生显色反应 ②能发生水解反应
其中核磁共振氢谱显示为5组峰,且峰面积比为2:2:2:1:1的是_____(写结构简式)。
(5)参照有机物M的上述合成路线,设计一条由![]() 和(CH3)3CCl为起始原料制备
和(CH3)3CCl为起始原料制备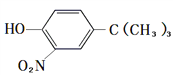 的合成路线:___________________________。
的合成路线:___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质必须隔绝空气保存的是
①Na ②Na2O ③Na2O2 ④NaOH ⑤Na2CO3 ⑥NaCl
A. ①② B. ②③④⑤ C. ①②③④ D. ①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容性方面有很好的应用前景。PPG的一种合成路线如下:

已知:①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢;
②化合物B为单氯代烃,化合物C的分子式为C5H8;
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
④![]()
回答下列问题:
(1)A的结构简式为________________。
(2)由B生成C的化学方程式为_________________________________。
(3)由E和F生成G的反应类型为___________,G的化学名称为_______________。
(4)①由D和H生成PPG的化学方程式为________________________。
②若PPG平均相对分子质量为10000,则其平均聚合度约为__________(填标号)。
a.48 b.58 c.76 d.122
(5)D的同分异构体中能同时满足下列条件的共有________种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体
②既能发生银镜反应,又能发生皂化反应
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是_________(写结构简式);D的所有同分异构体在下列—种表征仪器中显示的信号(或数据)完全相同,该仪器是____(填标号)。
a.质谱仪b.红外光谱仪 c.元素分析仪 d.核磁共振仪
查看答案和解析>>
科目: 来源: 题型:
【题目】二氯亚砜(SOCl2)是一种无色易挥发液体,遇水剧烈水解生成两种气体,常用作脱水剂,其熔点-105℃,沸点79℃,140℃以上时易分解。
(1)用硫黄(用S表示)、液氯和三氧化硫为原料在一定条件合成二氯亚砜,原子利用率达100%,则三者的物质的量比为________。写出SOCl2吸收水蒸气的化学方程式:____________。
(2)甲同学设计下图装置用ZnCl2·xH2O晶体制取无水ZnCl2,回收剩余的SOCl2并验证生成物中含有SO2(夹持及加热装置略):

①装置的连接顺序为A→B→______→______→______→______。
②搅拌的作用是______,冷凝管的作用是______。
③实验结束后,为检测ZnCl2·xH2O晶体是否完全脱水,称取蒸干后的固体ag溶于水,加入足量稀硝酸和硝酸银溶液,过滤,洗涤,干燥,称得固体为bg。若![]() _____(保留一位小数),即可证明ZnCl2·xH2O晶体已完全脱水。
_____(保留一位小数),即可证明ZnCl2·xH2O晶体已完全脱水。
④乙同学认为直接将ZnCl2·xH2O晶体置于坩埚中加热即可得到无水ZnCl2,但老师说此方法不可。请用化学方程式解释原因:____________。
(3)丙同学认为SOCl2还可用作由FeCl3·6H2O制取无水FeCl3的脱水剂,但丁同学认为该实验会发生氧化还原反应。请你设计并简述实验方案判断丁同学的观点:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com