
科目: 来源: 题型:
【题目】下列各物质中,互为同位素的是 , 互为同素异形体的是 , 互为同系物的是 , 互为同分异构体的是 .
①金刚石与石墨
②12C与14C
③ ![]() 与
与 ![]()
④ 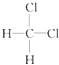 与
与 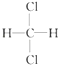
⑤ 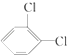 与
与 ![]()
⑥ 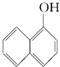 与
与 ![]()
⑦CH4与C(CH3)4 .
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,有pH=12的NaOH溶液100 mL,要使它的pH降为11。(假设溶液混合体积等于稀释前两液体体积之和)
(1)若加入蒸馏水,应加_______________mL。
(2)若加入pH为10的NaOH溶液,应加____________mL。
(3)若加入0.01 mol/L的盐酸,应加_______________mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各有机物的系统命名正确的是
A、CH2=CH-CH=CH2 1,3-二丁烯 B、CH3CH2OOCCOOCH2CH3 乙二酸二乙酯
C、CH3CH2CH(OH)CH3 3-丁醇 D、CH3CH(CH2CH3)CH3 2-乙基丙烷
查看答案和解析>>
科目: 来源: 题型:
【题目】氨是最重要的氮肥,是产量最大的化工产品之一。德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol,他因此获得了1918年诺贝尔化学奖。密闭容器中,使2 mol N2和6 mol H2混合发生反应:N2(g)+3H2(g)
2NH3(g) ΔH=-92.4 kJ/mol,他因此获得了1918年诺贝尔化学奖。密闭容器中,使2 mol N2和6 mol H2混合发生反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应)。
2NH3(g)(正反应为放热反应)。
(1)当反应达到平衡时,N2和H2的浓度比是___________;N2和H2的转化率比是_____________。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量____________,密度_____________。(填“变大”、“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将_____________(填“正向”、“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将________(填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________(填“大于”、“小于”或“等于”)原来的2倍。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述错误的是( )
A.生命在于运动
B.没有水就没有生命
C.双氧水、医用酒精等外用药可用于皮肤消毒
D.蛋白质遇到( NH4)2SO4、CuSO4等硫酸盐均可发生盐析
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W四种短周期元素,有关数据如下表,下列叙述正确的是( )
元素代号 | X | Y | Z | W |
原子半径/pm | 66 | 70 | 143 | 160 |
主要化合价 | -2 | +5、+3、-3 | +3 | +2 |
A. W和Y形成的化合物为共价化合物
B. Y的最高价氧化物对应的水化物为强酸
C. Y的简单气态氢化物的沸点高于X的简单气态氢化物
D. 工业上经常采用电解Z的氯化物溶液制备Z单质
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出). 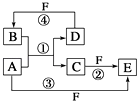
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,反应①的化学方程式Na2CO3:0.1mol;NaHCO3:0.05mol.
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,且光照条件下D与F也可以反应,则反应②的离子方程式是Na2CO3:0.1mol;NaHCO3:0.05mol.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为Na2CO3:0.1mol;NaHCO3:0.05mol.将标准状况下3.36L 物质E 与含10.0g 氢氧化钠溶质的溶液充分反应,所得溶液溶质成分为Na2CO3:0.1mol;NaHCO3:0.05mol(写出化学式和对应的物质的量).
查看答案和解析>>
科目: 来源: 题型:
【题目】美国通用原子能公司(GA)提出的碘硫热化学循环是由反应Ⅰ、Ⅱ、Ⅲ三步反应组成的(如下图所示),下列有关说法正确的是( )

A. 设计该循环是为了制取能源气体O2
B. 整个循环过程中产生1 mol O2的同时产生44.8 L H2
C. 若反应Ⅰ、Ⅱ、Ⅲ的反应热分别为△H1、△H2、△H3,则△H1+△H2+△H3>0
D. 图中反应Ⅰ、Ⅱ、Ⅲ均可在常温常压下进行
查看答案和解析>>
科目: 来源: 题型:
【题目】疏松的糕点、饼干、面包等在制作过程中都使用了疏松剂。疏松剂受热分解,产生的气体使食品酥脆、松软。下列物质可作为食品制作过程中使用的疏松剂的是
A. NaCl B. Na2CO3 C. NaHCO3 D. NaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图所示. 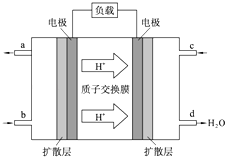
(1)该电池工作时,b口通入的物质为 , c口通入的物质为 .
(2)该电池负极的电极反应式为 .
(3)工作一段时间后,当6.4g甲醇完全反应生成CO2时,有NA个电子转移.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com