
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”–ΜζΈοM «“Μ÷÷≥Θ”ΟœψΝœ2ΒΡ÷ς“Σ≥…Ζ÷÷°“ΜΘ§”…ΧΰAΚœ≥…Τδ¬ΖœΏ»γœ¬ΓΘ
ΦΚ÷ΣΘΚΔΌBΒΡΫαΙΙΦρ ΫΈΣΘΚ![]()
ΔΎRCΓ‘CHΘΪHCHO![]() RCΓ‘CCH2OHΘΜ
RCΓ‘CCH2OHΘΜ
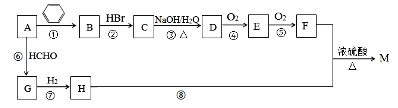
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©AΒΡœΒΆ≥ΟϋΟϊΈΣ_________ΓΘ
Θ®2Θ©Ζ¥”ΠΔόΖ¥”Πάύ–Ά «____________ΘΜF÷–ΙΌΡήΆ≈ΒΡΟϊ≥Τ_______________ΓΘ
Θ®3Θ©Έο÷ MΒΡΫαΙΙΦρ ΫΈΣ_____________________ΓΘ
Θ®4Θ©Ζ¥”ΠΔέΒΡΜ·―ßΖ¥”ΠΖΫ≥Χ ΫΈΣ_______________________ΓΘ
Θ®5Θ©ΖϊΚœœ¬Ν–ΧθΦΰΒΡFΒΡΆ§Ζ÷“λΙΙΧεΙ≤”–____÷÷ΓΘ
ΔΌΡήΖΔ…ζ“χΨΒΖ¥”ΠΘΜΔΎΡήΖΔ…ζΥ°ΫβΖ¥”ΠΘΜΔέ τ”ΎΖΦœψΉεΜ·ΚœΈοΘΜΔή±ΫΜΖ…œ”–ΝΫΗω«β‘≠Ή”±Μ»Γ¥ζΓΘ(6)“―÷ΣΘΚΔΌΒ±±ΫΜΖ…œ“―”–ΓΣΗωΓΑ“Μ CH3Γ± ±Θ§–¬“ΐ»κΒΡ»Γ¥ζΜυ“ΜΑψ‘Ύ‘≠”–»Γ¥ζΜυΒΡΝΎΈΜΜρΕ‘ΈΜ…œΓΘΔΎΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΩ…“‘Α―±ΫΜΖ…œΒΡΓΑ“ΜCH3Γ±―θΜ·≥…ΓΑΓΣCOOHΓ±ΓΘ«κ”ΟΚœ≥…Ζ¥”ΠΝς≥ΧΆΦ±μ Ψ≥ω”…ΦΉ±ΫΚΆΤδΥϊΈο÷ Κœ≥…![]() ΒΡΉνΦ―ΖΫΑΗΘ§Κœ≥…Ζ¥”ΠΝς≥Χ±μ ΨΖΫΖ® Ψάΐ»γœ¬ΘΚ
ΒΡΉνΦ―ΖΫΑΗΘ§Κœ≥…Ζ¥”ΠΝς≥Χ±μ ΨΖΫΖ® Ψάΐ»γœ¬ΘΚ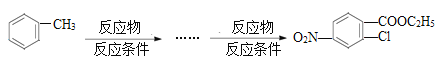 ________________ΓΘ
________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“ΜΕ®ΧθΦΰœ¬Θ§œ¬Ν–Ζ¥”Π÷–Υ°’τΤχΚ§ΝΩΥφΖ¥”Π ±ΦδΒΡ±δΜ·«ς ΤΖϊΚœ»γΆΦΒΡ «Θ® Θ©
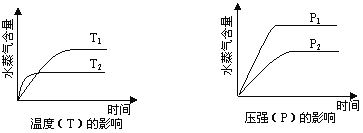
A. CO2(g)ΘΪ2NH3(g)![]() CO(NH2)2(s)ΘΪH2O(g)ΠΛHΘΦ0
CO(NH2)2(s)ΘΪH2O(g)ΠΛHΘΦ0
B. CO2(g)ΘΪH2(g)![]() CO(g)ΘΪH2O(g) ΠΛHΘΨ0
CO(g)ΘΪH2O(g) ΠΛHΘΨ0
C. CH3CH2OH(g)![]() CH2=CH2(g)ΘΪH2O(g) ΠΛHΘΨ0
CH2=CH2(g)ΘΪH2O(g) ΠΛHΘΨ0
D. 2C6H5CH2CH3(g)ΘΪO2(g)![]() 2C6H5CH=CH2(g)ΘΪ2H2O(g) ΠΛHΘΦ0
2C6H5CH=CH2(g)ΘΪ2H2O(g) ΠΛHΘΦ0
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ(ΝρΜ·ΦνΖ® «ΙΛ“Β…œ÷Τ±ΗNa2S2O3ΒΡΖΫΖ®÷°“ΜΘ§Ζ¥”Π‘≠άμΈΣΘΚ2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2Θ®ΗΟΖ¥”ΠΓςHΘΨ0Θ©ΓΘΡ≥―–ΨΩ–ΓΉι‘Ύ Β―ι “”ΟΝρΜ·ΦνΖ®÷Τ±ΗNa2S2O3ΓΛ5H2OΝς≥Χ»γœ¬ΓΘ
![]()
Θ®1Θ©ΈϋΝρΉΑ÷Ο»γΆΦΥυ Ψ
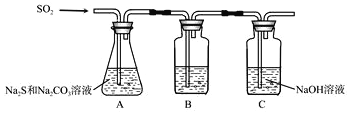
ΔΌΉΑ÷ΟBΒΡΉς”Ο «Φλ―ιΉΑ÷ΟA÷–SO2ΒΡΈϋ ’–߬ Θ§B÷– ‘ΦΝ «______Θ§±μΟςSO2Έϋ ’–߬ ΒΆΒΡ Β―ιœ÷œσ «B÷–»ή“Κ_________ΓΘ
ΔΎΈΣΝΥ ΙSO2ΨΓΩ…ΡήΈϋ ’Άξ»ΪΘ§‘Ύ≤ΜΗΡ±δA÷–»ή“Κ≈®Ε»ΓΔΧεΜΐΒΡΧθΦΰœ¬Θ§≥ΐΝΥΦΑ ±ΫΝΑηΖ¥”ΠΈοΆβΘ§ΜΙΩ…≤…»ΓΒΡΚœάμ¥κ © «___________________ΓΘΘ®¥π“ΜΧθΘ©
Θ®2Θ©ΦΌ…η±Ψ Β―ιΥυ”ΟΒΡNa2CO3Κ§…ΌΝΩNaClΓΔNaOHΘ§…ηΦΤ Β―ιΖΫΑΗΫχ––Φλ―ιΓΘ«κΆξ≥…ΗΟ Β―ιΖΫΑΗΓΘΘ®“―÷ΣΘΚ “Έ¬ ±CaCO3±ΞΚΆ»ή“ΚΒΡpHΘΫ10.2Θ©
–ρΚ≈ | Β―ι≤ΌΉς | ‘ΛΤΎœ÷œσ | Ϋα¬έ |
ΔΌ | »Γ…ΌΝΩ―υΤΖ”Ύ ‘Ιή÷–Θ§Φ”»κ ΝΩ’τΝσΥ°Θ§≥δΖ÷’ώΒ¥»ήΫβΘ§ ______ΓΘ | ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥… | ―υΤΖΚ§NaCl |
ΔΎ | Νμ»Γ…ΌΝΩ―υΤΖ”Ύ…’±≠÷–Θ§Φ”»κ ΝΩ’τΝσΥ°Θ§≥δΖ÷ΫΝΑη»ήΫβΘ§_____ΓΘ | ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…Θ§…œ≤ψ«ε“ΚpH>10.2 | ―υΤΖΚ§NaOH |
Θ®3Θ©Na2S2O3»ή“Κ «Ε®ΝΩ Β―ι÷–ΒΡ≥Θ”Ο ‘ΦΝΘ§≤βΕ®Τδ≈®Ε»ΒΡΙΐ≥Χ»γœ¬ΘΚ
ΒΎ“Μ≤ΫΘΚΉΦ»Ζ≥Τ»Γa g KIO3Θ®Μ·―ß ΫΝΩΘΚ214Θ©ΙΧΧε≈δ≥…»ή“ΚΘΜ
ΒΎΕΰ≤ΫΘΚΦ”»κΙΐΝΩKIΙΧΧεΚΆH2SO4»ή“ΚΘ§ΒΈΦ”÷Η ΨΦΝΘΜ
ΒΎ»ΐ≤ΫΘΚ”ΟNa2S2O3»ή“ΚΒΈΕ®÷Ν÷’ΒψΘ§œϊΚΡNa2S2O3»ή“ΚΒΡΧεΜΐΈΣV mLΓΘ‘ρc(Na2S2O3)ΘΫ___molΓΛL-1ΓΘ
Θ®4Θ©‘Ύ(3)ΒΡ Β―ι÷–Θ§Ρ≥Ά§―ßΒΎ“Μ≤ΫΚΆΒΎΕΰ≤ΫΒΡ≤ΌΉςΕΦΚήΙφΖΕΘ§ΒΎ»ΐ≤ΫΒΈΥΌΧΪ¬ΐΘ§’β―υ≤βΒΟΒΡNa2S2O3≈®Ε»Ω…Ρή___________Θ®ΧνΓΑ≤Μ ή”ΑœλΓ±ΓΔΓΑΤΪΒΆΓ±ΜρΓΑΤΪΗΏΓ±Θ©Θ§‘≠“ρ «_____________ΓΘ(”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ)ΓΘ(“―÷ΣΘΚIO3-ΘΪ5I-+6H+= 3I2ΘΪ3H2OΘ§4I-ΘΪO2+4H+=I2ΘΪ2H2OΘ§2S2O32-ΘΪI2=S4O62-ΘΪ2I-)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕ‘”ΎΖ¥”ΠΘΚ4CO(g)+2NO2(g)=4CO2(g)+N2(gΘ©ΓςH=-1200KJ/molΘ§Έ¬Ε»≤ΜΆ§(T2>T1Θ©ΤδΥϊΧθΦΰœύΆ§ ±Θ§œ¬Ν–ΆΦœώ’ΐ»ΖΒΡ «

A. A B. B C. C D. D
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΙΛ“Β…œ”Ο¬ΝΆΝΩσ(÷ς“Σ≥…Ζ÷ΈΣAl2O3Θ§ΜΙΚ§”–…ΌΝΩFe2O3ΓΔSiO2Β»‘”÷ )Χα»Γ―θΜ·¬Ν

≤ΌΉςΙΐ≥Χ»γœ¬ΘΚ
(1)≥ΝΒμA÷–÷ς“ΣΚ§”– (ΧνΜ·―ß Ϋ)Θ§≥ΝΒμB÷–Κ§”– (ΧνΜ·―ß Ϋ)ΘΜ
(2)(Δώ)(Δρ)≤Ϋ÷η÷–Ζ÷άκ»ή“ΚΚΆ≥ΝΒμΒΡ≤ΌΉςΟϊ≥Τ « ΘΜ
(3)¬Υ“ΚX÷–Θ§≥ΐΝΥH+ΓΔFe3+ΆβΘ§ΜΙΚ§”–¥σΝΩΒΡ―τάκΉ” « ΘΜ
(4)–¥≥ω(Δτ)≤Ϋ÷η÷–«β―θΜ·¬ΝΦ”»»Ζ÷ΫβΒΡΜ·―ßΖΫ≥Χ ΫΘΚ ΘΜ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“ΜΖί»ή“Κ÷–Ω…Ρή¥σΝΩΚ§”–K+ΓΔA13+ΓΔH+ΓΔNH4+ΓΔCl-ΓΔBr-ΓΔI-ΓΔClO-ΓΔA1O2-Β»άκΉ”÷–ΒΡ»τΗ…÷÷ΓΘΈΣΝΥ»ΖΕ®»ή“ΚΒΡΉι≥…Θ§Ϋχ––ΝΥ»γœ¬≤ΌΉςΘΚ
Θ®1Θ©ΆυΗΟ»ή“Κ÷–÷πΒΈΦ”»κNaOH»ή“Κ≤Δ Β±Φ”»»Θ§≤ζ…ζ≥ΝΒμΚΆΤχΧεΒΡΈο÷ ΒΡΝΩ(n)”κΦ”»κNaOH»ή“ΚΒΡΧεΜΐΙΊœΒ»γΆΦΥυ ΨΘΚ
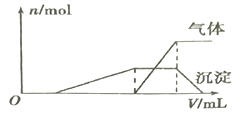
‘ρΗΟ»ή“Κ÷–“ΜΕ®¥φ‘ΎΒΡάκΉ” «________Θ§“ΜΕ®≤Μ¥σΝΩ¥φ‘ΎΒΡάκΉ” «__________ΓΘ
Θ®2Θ©Ψ≠Φλ≤βΚσΘ§ΗΟ»ή“Κ÷–Κ§”–¥σΝΩΒΡCl-ΓΔBr-ΓΔI-Θ§»τœρ1LΗΟΜλΚœ»ή“Κ÷–Ά®»κ“ΜΕ®ΝΩΒΡ¬»ΤχΘ§‘ρ»ή“Κ÷–Cl-ΓΔBr-ΓΔI-ΓΔ”κΆ®»κ¬»ΤχΒΡΧεΜΐ(±ξΉΦΉ¥Ωωœ¬)ΙΊœΒ»γœ¬±μΥυ ΨΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Cl2ΒΡΧεΜΐ(±ξΉΦΉ¥Ωωœ¬) | 2.8 L | 5.6 L | 11.2 L |
n(Cl-) | 1.25 mol | 1.5 mol | 2 mol |
n(Br-) | 1.5 mol | 1.4 mol | 0.9 mol |
n(I-) | a mol | 0 | 0 |
Β±Ά®»κΒΡ¬»ΤχΈΣ2.8L(±ξΉΦΉ¥Ωωœ¬) ±Θ§»ή“Κ÷–ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ___________Θ§‘≠»ή“Κ÷–n(Cl-)ΈΣ____molΘΜΆ®»κ¬»ΤχΒΡΧεΜΐ‘Ύ2.8LΓΪ5.6L(±ξΉΦΉ¥Ωωœ¬)÷°Φδ ±ΒΡ”–ΙΊάκΉ”ΖΫ≥Χ ΫΈΣ(»γ”–ΕύΗωΖ¥”ΠΘ§«κΖ÷ΩΣ ι–¥)_________________Θ§‘≠»ή“Κ÷–Cl-ΓΔBr-ΓΔI-ΒΡΈο÷ ΒΡΝΩ≈®Ε»÷°±»ΈΣ_______________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Έο÷ τ”Ύ¥ΩΨΜΈοΒΡ «(ΓΓΓΓ)
A. Τ·ΑΉΖέ B. “Κ¬» C. Υ°≤ΘΝß D. ―ΈΥα
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»γœ¬ΆΦΥυ ΨΘ§CΓΔDΓΔEΓΔFΓΔXΓΔYΕΦ «Εη–‘ΒγΦΪΓΘΫΪΒγ‘¥Ϋ”Ά®ΚσΘ§œρ““÷–ΒΈ»κΖ”ΧΣ ‘“ΚΘ§‘ΎFΦΪΗΫΫϋœ‘Κλ…ΪΓΘ ‘Άξ≥…“‘œ¬Έ ΧβΘΚ

Θ®1Θ©Βγ‘¥BΦΪΒΡΟϊ≥Τ «________ΓΘ
Θ®2Θ©““ΉΑ÷Ο÷–ΒγΫβΖ¥”ΠΒΡΉήΜ·―ßΖΫ≥Χ Ϋ «________________________ΓΘ
Θ®3Θ©»γΙϊ ’Φ·ΦΉΉΑ÷Ο÷–ΝΫΦΪ…œΈω≥ωΒΡΈο÷ Θ§ΝΫ÷÷Έο÷ ΒΡΈο÷ ΒΡΝΩ±» «Θ®―τΦΪ±»“θΦΪΘ©________ΓΘ
Θ®4Θ©”ϊ”Ο±ϊΉΑ÷ΟΗχΆ≠ΕΤ“χΘ§G”ΠΗΟ «____Θ®ΧνΓΑΆ≠Γ±ΜρΓΑ“χΓ±Θ©Θ§ΒγΕΤ“ΚΒΡ÷ς“Σ≥…Ζ÷ «______Θ®ΧνΜ·―ß ΫΘ©ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚ ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©Ρ≥Έ¬Ε» ±Θ§‘Ύ3LΟή±’»ίΤς÷–Ϋχ––ΒΡΡ≥“ΜΩ…ΡφΖ¥”ΠΘ§ΗΟΖ¥”Π÷–ΒΡXΓΔYΓΔZ»ΐ÷÷Έο÷ ΒΡΈο÷ ΒΡΝΩΥφ ±Φδ±δΜ·ΒΡ«ζœΏ»γœ¬ΆΦΥυ ΨΓΘ”…ΆΦ÷– ΐΨίΖ÷ΈωΘΚ

ΔΌΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ______________________ΓΘ
ΔΎΖ¥”ΠΩΣ Φ÷Ν3minΡ©Θ§ZΒΡΖ¥”ΠΥΌ¬ ΈΣ_____________________ΓΘ
ΔέΗΟΖ¥”Π «”…_____________ΩΣ ΦΖ¥”ΠΒΡΓΘΘ®ΧνΓΑ’ΐΖ¥”ΠΓ±ΓΔΓΑΡφΖ¥”ΠΓ±ΜρΓΑ’ΐΓΔΡφΖ¥”ΠΆ§ ±Γ±Θ©
Θ®2Θ©ΫΪSO2ΓΔO2‘ΎΡ≥Οή±’»ίΤς÷–ΜλΚœΘ§‘Ύ450 ΓφΖΔ…ζΖ¥”ΠΘΚ2SO2Θ®gΘ©ΘΪO2Θ®gΘ© ![]() SO3Θ®gΘ©ΓΘ
SO3Θ®gΘ©ΓΘ
ΔΌ‘ω¥σ―Ι«ΩΘ§‘ρ’ΐΖ¥”ΠΥΌ¬ ________Θ®Χν:‘ω¥σΓΔΦθ–ΓΜρ≤Μ±δ,œ¬Ά§Θ©Θ§ΡφΖ¥”ΠΥΌ¬ ________ΓΘ
ΔΎΈ§≥÷»ίΤς»ίΜΐ≤Μ±δΘ§Φ”»κ0.1 mol SO2ΒΡ“ΜΥ≤ΦδΘ§’ΐΖ¥”ΠΥΌ¬ ________Θ§ΡφΖ¥”ΠΥΌ¬ ________ΘΜ»τΦ”»κΒΡ «0.1 mol HeΘ§‘ρ’ΐΓΔΡφΖ¥”ΠΥΌ¬ ________ΓΘ
Δέ»τΈ§≥÷»ίΤς―Ι«Ω≤Μ±δΘ§Φ”»κ0.1 mol HeΚσΘ§»ίΤςΒΡ»ίΜΐ________Θ§Έο÷ ΒΡ≈®Ε»________Θ§Ζ¥”ΠΥΌ¬ ________ΓΘ
Θ®3Θ©‘Ύ100Γφ ±Θ§ΫΪ0.100mol N2O4ΤχΧε≥δ»κ1LΚψ»ί≥ιΩ’ΒΡΟή±’»ίΤς÷–Θ§Ητ“ΜΕ® ±ΦδΕ‘ΗΟ»ίΤςΡΎΈο÷ ΒΡ≈®Ε»Ϋχ––Ζ÷ΈωΒΟΒΫ»γ±μ ΐΨίΘΚ
±ΦδΘ®sΘ© | 0 | 20 | 40 | 60 | 80 |
cΘ®N2O4Θ©/molΓΛLΘ≠1 | 0.100 | c1 | 0.050 | c3 | c4 |
cΘ®NO2Θ©/molΓΛLΘ≠1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
ΔΌΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐ±μ¥ο ΫΈΣ___________ΘΜ¥”±μ÷–Ζ÷ΈωΘΚc1___________c2Θ§ c3___________c4Θ®ΧνΓΑ>Γ±ΓΔΓΑ<Γ±ΜρΓΑΘΫΓ±Θ©ΓΘ
ΔΎ‘Ύ…œ ωΧθΦΰœ¬Θ§¥”Ζ¥”ΠΩΣ Φ÷±÷Ν¥οΒΫΜ·―ßΤΫΚβ ±Θ§N2O4ΒΡΤΫΨυΖ¥”ΠΥΌ¬ ΈΣ________molΓΛLΘ≠1ΓΛsΘ≠1
Δέ»τ‘ΎœύΆ§ΧθΦΰœ¬Θ§Τπ Φ ±÷Μ≥δ»κ0.080 mol NO2ΤχΧεΘ§‘ρ¥οΒΫΤΫΚβ ±NO2ΤχΧεΒΡΉΣΜ·¬ ΈΣ_________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com