
科目: 来源: 题型:
【题目】我国科学家前不久成功合成3nm长的管状碳纳米管,长度居世界之首。这种碳纤维具有强度高、刚度(抵抗变形的能力)高、密度小(只有钢的1/4)、熔点高,化学稳定性好的特点,因此被称为“超级纤维”。下列对碳纤维的说法中不正确的是( )
A.它是制造飞机的理想材料
B.它的主要组成元素是碳元素
C.它的结构与石墨相似
D.碳纤维复合材料不易导电
查看答案和解析>>
科目: 来源: 题型:
【题目】t℃时,将2mol SO2和1mol O2通入体积为2L的恒温恒容密闭容器中,发生如下反应:2SO2(g)+O2(g)2SO3(g),2min时反应达到化学平衡,此时测得反应物O2还剩余0.2mol,请填写下列空白:
(1)从反应开始到化学平衡,生成SO3的平均反应速率为;平衡时SO2转化率为 .
(2)下列叙述能证明该反应已达到化学平衡状态的是 .
A.容器内压强不再发生变化
B.SO2的体积分数不再发生变化
C.容器内气体原子总数不再发生变化
D.相同时间内消耗2n mol SO2的同时消耗n mol O2
E.相同时间内消耗2n mol SO2的同时生成n mol O2
(3)t℃时,该反应的平衡常数为
(4)t1℃时,若将物质的量之比n(SO2):n(O2)=1:1的混合气体通入一个恒温恒压的密闭容器中,反应达到平衡时,混合气体体积减少了10%.SO2的转化率为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法正确的是
A.25℃ 101kPa时,CH4(g)+2O2(g)=CO2(g) +2H2O(g) △H=-Q kJ/mol,则甲烷的燃烧热为Q kJ/mol
B.CaCO3(s)=CaO(s)+CO2(g) 室温下不能自发进行,说明该反应的 ΔH<0
C.反应N2(g)+3H2(g)![]() 2NH3(g)ΔH<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大
2NH3(g)ΔH<0达到平衡后,升高温度,反应速率v(H2)和H2的平衡转化率均增大
D.已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q1、Q2的值均大于零):H2(g) +Cl2(g)=2HCl(g),△H1=—Q1 kJ/mol,H2(g) +Br2(g)=2HBr(g),△H2=—Q2 kJ/mol,则△H1<△H2
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上通常用下列方法治理含氮化合物的污染.
(1)用稀土等催化剂能将汽车尾气中的CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染.写出NOx与CO催化转化成N2和CO2的化学方程式______.
(2)用NH3还原NOx生成N2和H2O.现有NO、NO2的混合气3L,可用同温同压下3.5L的NH3恰好使其完全转化为N2,则原混合气体中NO和NO2的物质的量之比为______.
(3)电化学降解治理水中硝酸盐污染.在酸性条件下,电化学降解NO的原理如图1,阴极反应式为______.

(4)科研小组研究铁屑对地下水脱氮的反应原理.
①pH=2.5时,用铁粉还原KNO3溶液,相关离子浓度、pH随时间的变化关系如图2(部分副反应产物曲线略去).请根据图中信息写出t1时刻前发生反应的离子方程式______,t1时刻后,反应仍在进行,溶液中NH4+的浓度在增大,Fe2+的浓度却没有增大,可能的原因是______.
②pH=2.5时,将铁屑和活性炭同时加入硝酸钾溶液中,可以加快脱氮速率,其原因是______.通常地下水中含有CO32﹣,会降低脱氮效果,其原因为____________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸合铁酸钾晶体Kx[Fe(C2O4)y]3H2O是一种光敏材料,下面是一种制备草酸合铁酸钾晶体的实验流程.
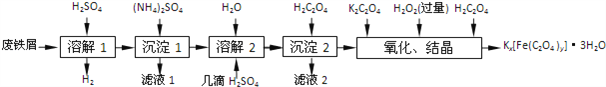
已知:(NH4)2SO4、FeSO47H2O、莫尔盐[(NH4)2SO4FeSO46H2O]的溶解度如下表:
温度/℃ | 10 | 20 | 30 | 40 | 50 |
(NH4)2SO4/g | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 |
FeSO47H2O/g | 40.0 | 48.0 | 60.0 | 73.3 | ﹣ |
(NH4)2SO4FeSO46H2O/g | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 |
(1)“溶解1”应保证铁屑稍过量,其目的是______.“溶解2”加“几滴H2SO4”的作用是______.
(2)“复分解”制备莫尔盐晶体的基本实验步骤是:蒸发浓缩、______、过滤、用乙醇洗涤、干燥.用乙醇洗涤的目的是______.
(3)“沉淀”时得到的FeC2O42H2O沉淀需用水洗涤干净.检验沉淀是否洗涤干净的方法是______.
(4)“结晶”时应将溶液放在黑暗处等待晶体的析出,这样操作的原因是______.
(5)请补全测定草酸合铁酸钾产品中Fe3+含量的实验步骤【备选试剂:KMnO4溶液、锌粉、铁粉、NaOH溶液】:
步骤1:准确称取所制备的草酸合铁酸钾晶体a g,配成250mL待测液.
步骤2:用移液管移取25.00mL待测液于锥形瓶中,加入稀H2SO4
步骤3:向步骤2所得溶液中______加热至充分反应(溶液黄色刚好消失),过滤、洗涤、将过滤及洗涤所得溶液收集到锥形瓶中.
步骤4:用c molL﹣1 KMnO4标准溶液滴定步骤3所得溶液至终点,消耗V mL KMnO4标准溶液.
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中充入CO2、CO、CH4的混合气体共m g,若加入足量Na2O2,充分振荡并不断用电火花引燃至反应完全,测得固体质量增加m g,则CO2与CH4的体积比为( )
A.3∶1B.2∶1C.1∶1D.任意比
查看答案和解析>>
科目: 来源: 题型:
【题目】下列一步转化中,一定要加入氧化剂才能实现的是( )
A. SiO2―→Na2SiO3 B. Na2O2―→NaOH
C. N2―→NH3 D. NH3―→NO
查看答案和解析>>
科目: 来源: 题型:
【题目】有以下四种物质(标准状况下):①11.2L二氧化碳,②19.2g甲烷,③9.03×1023个氮气分子,④1mol的H2S气体.标准状况下体积最小的是(填序号,下同),它们所含分子数最多的是 , 所含原子数最多的是 , 质量最小的是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】A,B,C,D都是短周期元素,原子半径D>C>A>B,其中A、B处在同一周期,A、C处在同一主族.C原子核内质子数等于A,B原子核内质子数之和,C原子最外层上的电子数是D原子最外层电子数的4倍.试回答:
(1)这四种元素分别是:A , B , C , D . (填元素符号)
(2)A,B,C元素各自形成的氢化物的稳定性由强到弱的顺序是 (填化学式,下同)
(3)A与B形成的三原子分子的电子式是 , B与D形成的原子个数比为1:1的化合物的电子式是 .
(4)A元素某氧化物与D元素某氧化物反应生成单质的化学方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com