
科目: 来源: 题型:
【题目】将4molSO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2+O22SO3 测得平衡时SO3的浓度为0.5mol/L,求:
(1)平衡时各物质的浓度;
(2)平衡时SO2的转化率;
(3)该条件下的平衡常数K.
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物J具有抗缺血性脑损伤的作用,合成J的一种路线如图: 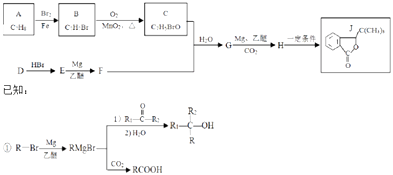
②E的核磁共振氢谱只有一组峰
③C能发生银镜反应
回答下列问题:
(1)D所含有官能团的名称 .
(2)由D生成E的化学方程式为 , 其反应类型为 .
(3)G的结构简式为 .
(4)C的某同系物X,相对分子质量比C大14,X的结构有种,其中核磁共振氢谱为4组峰,且锋面积比为1:2:2:2的是(写结构简式).
(5)由甲醛和化合物A经下列步骤可得到2﹣苯基乙醇. ![]()
反应条件1为;反应条件2所选择的试剂为;L的结构简式为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】浓度为2.00mol/L的盐酸溶液1L,欲使其浓度变为4.00mol/L,下列方法可行的是( )
A.蒸发掉0.5L水
B.标况下通入44.8L HCl气体
C.将溶液加热蒸发浓缩至0.5L
D.加入10mol/L盐酸0.6L,再将溶液稀释至2L
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种新型燃料,甲醇燃料电池即将从实验室走向工业化生产。工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
CO(g)+ 2H2(g)![]() CH3OH(g) △H1=-116 kJ·mol-1
CH3OH(g) △H1=-116 kJ·mol-1
(1)已知: ![]() △H2=-283 kJ·mol-1
△H2=-283 kJ·mol-1
![]() △H3=-242 kJ·mol-1
△H3=-242 kJ·mol-1
则表示1mol气态甲醇完全燃烧生成CO 2和水蒸气时的热化学方程式:________________
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃、270℃三种温度下合成甲醇的规律。右图是上述三种温度下不同的H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。请回答:

①在上述三种温度中,曲线Z对应的温度是________________
②利用图中a点对应的数据,计算出曲线Z在对应温度下CO(g)+2H2(g)![]() CH3OH(g)的平衡常数 K=_________。
CH3OH(g)的平衡常数 K=_________。
(3)在某温度下,将一定量的CO和H2投入10L的密闭容器中,5min时达到平衡,各物质的物质的浓度 (molL-1)变化如下表所示:
0min | 5min | 10min | |
CO | 0.1 | 0.05 | |
H2 | 0.2 | 0.2 | |
CH3OH | 0 | 0.04 | 0.05 |
若5min~10min只改变了某一条件,所改变的条件是_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中发生如下反应:A(s)+2B(g)![]() 2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是
2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是

A. 反应开始2 min内,v(B)=0.1 mol/(L·min)
B. t1时改变的条件可能是升高温度
C. t3时改变的条件可能是加压,此时c(B)不变
D. t4时可能是使用了催化剂,此时c(B)不变
查看答案和解析>>
科目: 来源: 题型:
【题目】在周期表中1~36号之间的W、X、Y、Z、Q六种元素,它们的原子序数依次增大,已知W与其余五种元素既不同周期也不同主族,X原子的L层p轨道中有2个电子,Y元素原子的最外层有3个自旋方向相同的未成对电子,Z元素原子基态时,核外电子排布在3个能级上,且有2个未成对电子.Q元素在第四周期,原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.
(1)按电子排布,Q元素在周期表中属区.
(2)第一电离能YZ,电负性YZ(填“>”,“=”或“<”).
(3)W与Z形成的常见化合物有W2Z、W2Z2 , W与Y能形成多种二元化合物,如YW3、Y2W4、Y3W5、Y4W6…,W2Z分子中Z原子的杂化类型为 , YW3分子的立体构型为 , YW3极易溶于W2Z的主要原因有 .
(4)若向含有Q2+的硫酸盐溶液中滴加过量氨水,得到深蓝色溶液后再加乙醇,有深蓝色晶体析出,该晶体阳离子中含有的化学键有 .
(5)Q+与Y3﹣形成的晶胞结构如图所示,阴、阳离子间的核间距为 a pm,阿伏伽德罗常数用NA 表示,则晶体的密度为gcm﹣3 . 
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B.在常温常压下,1 mol 氦气含有的原子数为NA
C.常温常压下,22.4L氯气与足量金属钠充分反应,转移的电子数为2NA
D.常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液,一定呈中性的是
A. 由等体积、等物质的量浓度的硫酸跟NaOH溶液混合后所形成的溶液
B. c(H+)=1.0×10-7mol·L-1的溶液
C. pH=7的溶液
D. c(H+)=![]() 的溶液(Kw为该温度下水的离子积常数)
的溶液(Kw为该温度下水的离子积常数)
查看答案和解析>>
科目: 来源: 题型:
【题目】环己酮是重要化工原料,是制造尼龙、己内酰胺和己二酸的主要中间体.实验室常用铬酸氧化环己醇制备,但铬酸较贵且污染环境.某化学兴趣兴趣小组尝试用中学化学更常见的次氯酸钠代替铬酸制备环己酮.有关物质信息、实验流程如图1及实验装置如图2如下:环己酮:无色或浅黄色透明液体,有强烈的刺激性臭味,相对水的密度:0.95,熔点:﹣45℃,沸点:155℃,溶解度(100mL H2O):2.4g (31℃ ). 回答下列问题:
回答下列问题:
(1)仪器A的名称是 .
(2)在反应开始的5min,为了将体系温度维持在30~35℃,除了用冰水浴冷却外,采取的措施还有、 .
(3)加入饱和NaHSO3溶液时发生的主要反应是(用离子方程式表示),确保加入的饱和NaHSO3溶液已经足量的实验操作是 .
(4)为将馏出液的pH调至中性,可以加入的试剂是 .
A.稀盐酸
B.无水碳酸钠
C.浓硫酸
D.氢氧化钠固体
(5)调节pH后还需加入精制食盐,其目的是 , “取有机层”时使用的主要仪器是 . (填图3对应的字母).
(6)实验条件的优化对实验成败至关重要,小组成员觉得有必要对NaClO溶液的最佳浓度进行探究.他们配制了一系列不同浓度的NaClO溶液,并用滴定法标定.具体方法是:用移液管取10.00mL NaClO溶液于500mL容量瓶中定容,取25.00mL于锥形瓶中,加入适量稀盐酸和KI固体(足量),用0.1000mol/L Na2S2O3标准溶液滴定至终点(用淀粉溶液作指示剂),三次平行实验平均消耗Na2S2O3标准溶液18.00mL,已知I2+2Na2S2O3═2NaI+Na2S4O6 . 则该NaClO溶液的浓度是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com