
【题目】下列溶液,一定呈中性的是
A. 由等体积、等物质的量浓度的硫酸跟NaOH溶液混合后所形成的溶液
B. c(H+)=1.0×10-7mol·L-1的溶液
C. pH=7的溶液
D. c(H+)=![]() 的溶液(Kw为该温度下水的离子积常数)
的溶液(Kw为该温度下水的离子积常数)
科目:高中化学 来源: 题型:
【题目】据报道科研人员应用计算机模拟出结构类似C60的物质N60 。已知:①. N60分子中每个氮原子均以N—N键结合三个N原子而形成8电子稳定结构;②.N—N键的键能为167 kJ/mol,N≡N键的键能为942kJ/mol。试回答下列问题:
(1)N60组成的晶体为_______ 晶体,其熔、沸点比N2的 _______(高或低),其原因是__________ 。
(2)1mol N60 分解成N2时吸收或释放的热量为________________kJ。
(3)常温常压下,向50 mL 0.4mol/L的NaOH溶液中加入过量的稀H2SO4,测得放热 a kJ.写出上述反应的热化学方程式:____________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧气可发生如下反应:P4+5O2===P4O10。已知断裂下列化学键需要吸收的能量分别为P-P:a kJ·mol-1、P—O:b kJ·mol-1、P===O:c kJ·mol-1、O===O:d kJ·mol-1。根据下图所示的分子结构和有关数据估算该反应的ΔH,其中正确的是( )

A. (6a+5d-4c-12b) kJ·mol-1
B. (4c+12b-6a-5d) kJ·mol-1
C. (4c+12b-4a-5d) kJ·mol-1
D. (4a+5d-4c-12b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A~K分别代表一种物质.已知A易溶于水,分解得到B、C、D的物质的量比为1:1:2,B气体能使品红溶液褪色,C为常见的液体,D气体能使湿润的紫色石蕊试纸变蓝,F为淡黄色固体单质,K为常见的二元强酸,图中有部分生成物未标出.
(1)A的化学式为 .
(2)写出反应①的离子方程式: .
(3)写出反应②、④、⑤的化学方程式:②;
④;
⑤ .
(4)在反应③中,每生成标准状况下2.24L G时,转移电子的物质的量为mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式表达正确的是(![]() 的绝对值均正确)
的绝对值均正确)
A. C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g) △H=–1367.0 kJ/mol(燃烧热)
B. NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1) △H= +57.3kJ/mol(中和热)
C. S(s)+O2(g)=SO2(g) △H=–269.8kJ/mol (反应热)
D. 2NO2=O2+2NO △H= +116.2kJ/mol (反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓度为2.00mol/L的盐酸溶液1L,欲使其浓度变为4.00mol/L,下列方法可行的是( )
A.蒸发掉0.5L水
B.标况下通入44.8L HCl气体
C.将溶液加热蒸发浓缩至0.5L
D.加入10mol/L盐酸0.6L,再将溶液稀释至2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2)是一种白色、无毒、难溶于水的固体,在350℃时会迅速分解生成CaO和O2 , 杀菌消毒,广泛用于果蔬保鲜、空气净化、污水处理等方面,其工业生产流程如下:
(1)步骤②制取CaO28H2O的反应(填“属于”或“不属于”)氧化还原反应.
(2)该流程中可循环使用的物质是 .
(3)检验CaO28H2O是否洗净的方法是 .
(4)在CaO28H2O加热脱水的过程中,需不断通入不含二氧化碳的氧气,目的是抑制CaO2分解和 .
(5)实验室用如图所示装置测定产品中CaO2的含量(加热、夹持、连接管等仪器省略).
①装置连接的顺序为(填字母);A中药品为 .
②写出实验开始前检验装置的气密性的方法: .
③若所取产品的质量是m g,测得气体体积为V mL(已换算成标准状况),则产品中CaO2的质量分数为(用含m、V的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右下图中P是可自由平行滑动的活塞。在相同温度时,向A容器中充入2 mol SO3(g),关闭K,向B容器中充入1 mol SO3(g),两容器分别发生反应:2SO3(g) ![]() 2SO2(g)+O2(g)。已知起始时容器A和B的体积均为a L。试回答:
2SO2(g)+O2(g)。已知起始时容器A和B的体积均为a L。试回答:
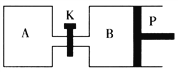
(1)反应达到平衡时容器B的体积变为1.2aL,容器B中SO3转化率为___________。
(2)若打开K,一段时间后重新达到平衡,容器B的体积为___________L(连通管中气体体积忽略不计)。
(3)将不同物质的量的H2O(g)和 CO分别通入体积为2L的恒容密闭容器中,发生反应:H2O(g)+CO(g)![]() CO2(g)+H2(g) △H,得到如下数据:
CO2(g)+H2(g) △H,得到如下数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | CO | H2 | |||
Ⅰ | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
Ⅱ | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
Ⅲ | 900 | 2 | 1 | a | b | t |
①由表中数据可知该反应的△H_______ 0(填“>”或“<”)。
②实验Ⅲ中a=______,达平衡时实验Ⅱ和实验Ⅲ中H2O(g)的转化率的大小关系为:α2(H2O)____α3(H2O)(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com