
科目: 来源: 题型:
【题目】用18mol/L 浓硫酸配制100ml 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积,②量取一定体积的浓硫酸,③溶解,④检漏、转移、洗涤,⑤定容、摇匀.回答下列问题:
(1)所需浓硫酸的体积是(保留到小数点后一位),量取浓硫酸所用的量筒的规格是(从下列中选用:A.10ml B.25ml C.50ml D.100ml)
(2)在上述实验步骤中,需要用到玻璃棒的有(填序号).
(3)第⑤步实验的操作是:继续向容量瓶注入蒸馏水至离刻度线1﹣2cm处,改用胶头滴管向容量瓶滴加至为止.塞紧瓶塞,倒转摇匀.
(4)下列情况对所配制的稀硫酸浓度有何影响?(填“偏大”、“偏小”或“无影响”) A.所用的浓硫酸长时间放置在密封不好的容器中
B.容量瓶用蒸馏水洗涤后残留有少量的水
C.所用过的烧杯、玻璃棒未洗涤
D.定容时俯视溶液的凹液面 .
查看答案和解析>>
科目: 来源: 题型:
【题目】金属铬和氢气在工业上都有重要的用途.已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4).铜铬构成原电池如图所示,盐桥中装的是饱和KCl琼脂溶液,下列关于此电池的说法正确的是( ) 
A.盐桥的作用是使整个装置构成通路、保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以用饱和KCl琼脂溶液
B.理论上1molCr溶解,盐桥中将有2molCl﹣进入左池,2molK+进入右池
C.此过程中H+得电子,发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥到转移到左烧杯中
查看答案和解析>>
科目: 来源: 题型:
【题目】现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图. 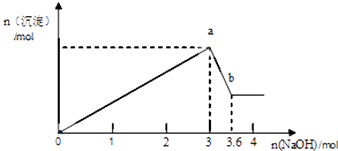
(1)a点对应的沉淀为(填化学式).
(2)计算原混合液中FeCl3的物质的量浓度为多少?
查看答案和解析>>
科目: 来源: 题型:
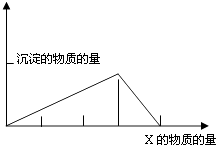
【题目】将物质X逐渐加入(或滴入)Y溶液中,其生成沉淀的量与加入X的物质的量关系如下图所示,符合图示情况的是( )
A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质结构的说法中正确的是(设NA为阿伏加德罗常数的值)( )
A. 构成单质分子的微粒一定含有共价键
B. 1.8 g NH4+中含有的电子数为NA
C. 离子化合物中一定不含有共价键
D. 离子化合物中只存在阴、阳离子之间的吸引作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com