
科目: 来源: 题型:
【题目】室温下向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中 ![]() 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mLpH=11的NaOH溶液,混合液的pH=7
查看答案和解析>>
科目: 来源: 题型:
【题目】据美国《科学》杂志报道:在40GPa高压下,用激光器加热到1800K,制得具有高熔点、高硬度的二氧化碳晶体.下列关于该晶体的说法正确的是( )
A.该晶体属于分子晶体
B.该晶体易汽化,可用作制冷材料
C.一定条件下,该晶体可跟氢氧化钠反应
D.每摩尔该晶体中含5 mol C﹣O键
查看答案和解析>>
科目: 来源: 题型:
【题目】在元素周期表中横行的编排依据是( )
A. 按元素的相对原子质量递增顺序从左到右排列
B. 按元素的原子核外电子层数依次递增顺序从左到右排列
C. 电子层相同的元素,按原子序数依次递增顺序从左到右排列
D. 按元素的原子最外层电子数依次递增顺序从左到右排列
查看答案和解析>>
科目: 来源: 题型:
【题目】镁及其化合物用途非常广泛,目前世界上60%的镁是从海水中提取.从海水中先将海水淡化获得淡水和浓海水,浓海水的主要成分如下:
离子 | Na+ | Mg2+ | Cl﹣ | SO42﹣ |
浓度/(gL﹣1) | 63.7 | 28.8 | 144.6 | 46.4 |
再利用浓海水提镁的一段工艺流程如下图:
请回答下列问题
(1)浓海水主要含有的四种离子中物质的量浓度最小的是 . 在上述流程中,可以循环使用的物质是 .
(2)在该工艺过程中,X试剂的化学式为 .
(3)“一段脱水”目的是制备MgCl22H2O;“二段脱水”的目的是制备电解原料.若将MgCl26H2O直接加热脱水,则会生成Mg(OH)Cl.若电解原料中含有Mg(OH)Cl,电解时Mg(OH)Cl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率.生成MgO的化学方程式为 .
(4)若制得Mg(OH)2的过程中浓海水的利用率为80%,由Mg(OH)2至“二段脱水”制得电解原料的过程中镁元素的利用率为90%,则1m3浓海水可得“二段脱水”后的电解原料质量为g.
(5)以LiCl﹣KCl共熔盐为电解质的Mg﹣V2O5电池是战术导弹的常用电源,该电池的总反应为:Mg+V2O5+2LiCl MgCl2+V2O4Li2O 该电池的正极反应式为 .
(6)Mg合金是重要的储氢材料.2LiBH4/MgH2体系放氢焓变示意图如下,则: Mg(s)+2B(s) MgB2(s)△H= . 
查看答案和解析>>
科目: 来源: 题型:
【题目】呋喃酚是生产农药克百威的主要中间体.其合成路线如下: 
(1)A物质核磁共振氢谱中各组吸收峰的峰面积之比为 , B→C的反应类型是 , E中含氧官能团的名称是 , 1molD最多可以消耗molNaOH.
(2)已知X的分子式为C4H7Cl,写出A→B的化学方程式: .
(3)Y是X的同分异构体,分子中无支链且不含甲基,则Y发生消去反应所得产物的名称(系统命名)是 .
(4)下列有关化合物C、D的说法正确的是 . ①可用氯化铁溶液鉴别C和D
②C和D含有的官能团完全相同
③C和D互为同分异构体
④C和D均能使溴水褪色
(5)E有多种同分异构体,写出符合下列条件的所有同分异构体的结构简式 . ①属于芳香族化合物
②苯环上的一氯代物只有一种
③含有酯基
④能发生银镜反应.
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室可用NaClO3制取ClO2气体,再由ClO2制得NaClO2 , 实验装置如图所示:回答下列问题: 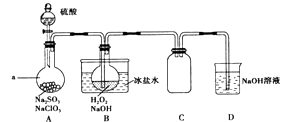
(1)仪器a的名称为;装置C的作用是 .
(2)该实验必须使NaClO3稍微过量,目的是 .
(3)为使ClO2气体能被均匀、充分吸收,操作时应注意 .
(4)NaOH吸收ClO2尾气,生成物质的量之比为1:1的两种阴离子,一种为ClO2﹣ , 则另一种为 .
(5)B中反应的离子方程式为 .
(6)证明NaClO2具有氧化性的方法是:将B中溶液加热除去H2O2 , 加入(填序号,下同)酸化,再加入检验. ①稀HNO3②稀H2SO4③K2SO3溶液 ④BaCl2溶液 ⑤FeCl2溶液 ⑥KSCN溶液
(7)预计NaClO3转化为NaClO2的转化率为80%,若要制得28.9g NaClO23H2O(相对质量:144.5),至少需g NaClO3(相对质量:106.5).
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、C原子都有两个未成对的单电子,D的二价阳离子与C的阴离子具有相同的电子层结构. B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 .
(2)B的氢化物的分子空间构型是 , 其中心原子的杂化方式是 .
(3)AC2的电子式 , 是分子(填“极性”或“非极性”),一种由B、C组成的化合物与AC2互为等电子体,其化学式为
(4)E的核外电子排布式是 , ECl3与B、C的氢化物形成的配合物的化学式为 .
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com