
科目: 来源: 题型:
【题目】某小组同学利用如图所示装置探究二氧化硫气体的性质. 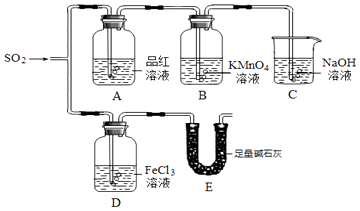
请回答:
(1)仪器E的名称是 . 若没有装置C,将气体直接排放到空气中,会带来的主要环境问题是 .
(2)观察到B中溶液颜色变浅,说明了SO2具有的性质是;
(3)写出仪器D中的实验现象 , 发生氧化还原反应的离子方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是 ( )
A.1 mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质体积均为22.4L
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,将20.0 g质量分数为14.0%的KNO3溶液与30.0 g质量分数为24.0%的KNO3溶液混合,得到的密度为1.15 g/cm3的混合溶液。计算(写出计算步骤):
(1)混合后溶液的质量分数。
(2)混合后溶液的物质的量浓度(计算结果保留两位小数,下同)。
(3)在1 000 g水中需溶解多少摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物的分子式为C10H14O2Cl2,分子结构中不含有环和碳碳三键,只含有一个碳氧双键,则该分子中含有碳碳双键的数目为( )
A.1个B.2个C.3个D.4个
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某强氧化剂[RO(OH)2]2+离子2.4×10-3mol被亚硫酸钠还原到较低价态,需12mL0.2mol/L的亚硫酸钠溶液,则反应后R的化合价为( )
A.0B.+2C.+3D.+4
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平.C在一定条件下也会生成D,D能使石蕊溶液变红;E是具有果香味的有机物,F是一种高分子化合物,可制成多种包装材料. 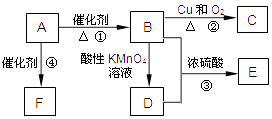
(1)A物质的结构简式为 .
(2)B→C的反应类型:;
(3)反应③的化学方程式为 .
(4)请设计一个简单的实验,以验证C物质存在该官能团的方法 .
查看答案和解析>>
科目: 来源: 题型:
【题目】某溶液可能含有Cl﹣、SO42﹣、CO32﹣、NH4+、Fe3+、Fe2+和Na+ . 某同学为了确认其成分,取部分溶液,设计并完成了如图实验:下列说法正确的是( ) 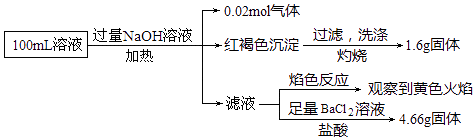
A.原溶液中c(Fe3+)=0.2molL﹣1
B.SO42﹣、NH4+、Na+一定存在,CO32﹣一定不存在
C.要确定原溶液中是否含有Fe2+ , 其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量氯水,溶液呈血红色,则含有Fe2+
D.溶液中至少有4种离子存在,其中Cl﹣一定存在,且c(Cl﹣)≥0.2molL﹣1
查看答案和解析>>
科目: 来源: 题型:
【题目】
(1)氢化钠(NaH)为白色晶体,其中H-有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价,写出其化学反应方程式,并用单线桥标出电子转移的方向与数目;NaH能与水剧烈反应NaH +H2O=NaOH+H2↑,NaH与液氨也有类似反应,写出反应的化学方程式。
(2)配平反应方程式:。![]() Al+
Al+ ![]() NaNO3+
NaNO3+ ![]() H2O=
H2O= ![]() Al(OH)3+
Al(OH)3+ ![]() N2↑+
N2↑+ ![]() NaAlO2
NaAlO2
(3)实验室用MnO2和浓盐酸制氯气的反应为MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑。反应中,如果有17.4 g纯MnO2被还原,那么:
MnCl2+2H2O+Cl2↑。反应中,如果有17.4 g纯MnO2被还原,那么:
①被氧化的氯化氢的质量为。
②转移电子的数目为。
③纺织工业中常用氯气作漂白剂,漂白布匹后,过量的氯需要除去,通常可用Na2SO3作“脱氯剂”,脱氯后的产物为Na2SO4 , 氯变为-1价。若把本题中产生的Cl2完全转化,需要Na2SO3的质量为。
查看答案和解析>>
科目: 来源: 题型:
【题目】粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如图: 
(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有:Pb﹣2e﹣+SO42﹣=PbSO4和 .
(2)碱浸渣的主要成分是、 . (写化学式)
(3)操作I的主要步骤为 .
(4)写出用SO2还原AuCl4﹣的离子方程式 .
(5)为了减少废液排放、充分利用有用资源,工业上将滤液2并入硝酸进行循环操作,请指出流程图中另一处类似的做法 .
(6)已知298K时,Ksp(PbCO3)=1.5×10﹣13 , Ksp(PbSO4)=1.8×10﹣8 , 将1mol PbSO4固体放入1L Na2CO3溶液中,充分反应后达到平衡,溶液中c(CO32﹣)为5mol/L,溶液体积在反应前后保持不变,则平衡后c(SO42﹣)= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com