
科目: 来源: 题型:
【题目】氨是重要的氮肥,合成原理为:N2(g)+3H2(g) ![]() 2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
(1)写出平衡常数K的表达式 , 如果降低温度,该反应K值E,化学反应速率 , N2的转化率(填“增大”、“减小”或“不变”).
(2)在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题: 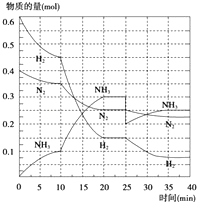
①10min内以NH3表示的平均反应速率: .
②在10~20min内:NH3浓度变化的原因可能是
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加NH3物质的量
③第1次平衡的时间为: , 第2次平衡的时间为: , 第1次平衡:平衡常数K1=(带数据的表达式),第2次平衡时NH3的体积分数;
④在反应进行至25min时,曲线发生变化的原因: ,
达第二次平衡时,新平衡的平衡常数K2K1 , (填“大于”、“小于”或“等于”).
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是( )
A.各能级的原子轨道数按s、p、d、f的顺序分别为1、3、5、7
B.N原子的轨道表示式: ![]() 违反了泡利不相容原理
违反了泡利不相容原理
C.电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理
D.电子排布式(23V)1s22s22p63s23p63d34s2违反了洪特规则
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的晶体直接由原子构成的一组是( )
①CO2 ②SiO2 ③晶体Si ④白磷 ⑤氨基乙酸 ⑥固态He
A.①②③④⑤⑥
B.②③④⑥
C.②③⑥
D.①②⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】1 L水中溶有Mg(HCO3)2和CaCl2的浓度分别是bmol/L和2bmol/L,现用一种试剂(适量)把Ca2+、Mg2+除去,这种试剂最好选用( )
A.Ca(OH)2B.NaOH
C.NaHCO3D.Na2CO3]
查看答案和解析>>
科目: 来源: 题型:
【题目】A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O2 ![]() 2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。
2CH3COOH。现以A为主要原料合成乙酸乙酯,其合成路线如图所示。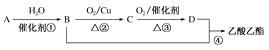
回答下列问题:
(1)写出A的电子式 , A的结构简式。
(2)B、D分子内含有的官能团分别是、(填名称)。
(3)写出下列反应的反应类型:① , ② , ④。
(4)写出下列反应的化学方程式:
①;
②;
④。
查看答案和解析>>
科目: 来源: 题型:
【题目】合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
(1)【实验方案一】将铝镁合金与足量NaOH溶液反应,测定剩余固体质量.实验中发生反应的化学方程式是 【实验步骤】
称取5.4g铝镁合金粉末样品,溶于VmL 2.0mol/LNaOH溶液中,充分反应.则NaOH溶液的体积V≥ .
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将(填“偏高”、“偏低”或“无影响”).
(3)【实验方案二】 将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01105Pa)的体积.
【问题讨论】
同学们拟选用图1实验装置完成实验:
①你认为最简易的装置其连接顺序是:A接接接(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因. .
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 .
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平,读取量筒中水的体积
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了图2所示的实验装置. ①装置中导管a的作用是 .
②实验前后碱式滴定管中液面读数分别为V1mL、V2mL.则产生氢气的体积为mL.
查看答案和解析>>
科目: 来源: 题型:
【题目】FeSO47H2O广泛用于医药和工业领域.以下是FeSO47H2O的实验室制备流程图. 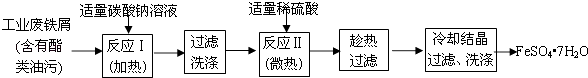
根据题意完成下列填空:
(1)碳酸钠溶液能除去酯类油污,是因为(用离子方程式表示),
(2)废铁屑中含氧化铁,无需在制备前除去,理由是(用离子方程式回答) , . 以下是测定某补血剂(FeSO47H2O)中铁元素含量的流程图.根据题意完成下列填空: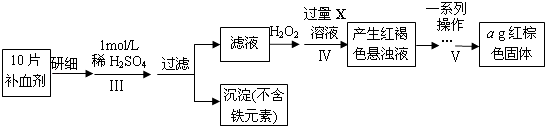
(3)步骤Ⅲ需要100mL1mol/L的稀硫酸,用98.3%,ρ=1.84g/cm3的浓硫酸配制,所用的仪器有量筒、烧杯、玻璃棒、胶头滴管及 .
(4)步骤Ⅴ一系列操作依次是:①过滤②洗涤③④冷却⑤称量⑥恒重操作.操作⑥的目的是 .
(5)假设实验无损耗,则每片补血剂含铁元素的质量g(用含a的代数式表示).
查看答案和解析>>
科目: 来源: 题型:
【题目】将1 mol乙醇(其中的氧用18O标记)在浓硫酸存在时与足量乙酸充分反应。下列叙述错误的是( )
A.生成的乙酸乙酯中含有18O
B.生成的水分子中含有18O
C.可能生成88 g乙酸乙酯
D.不可能生成90 g乙酸乙酯
查看答案和解析>>
科目: 来源: 题型:
【题目】把 ![]() 通入氨水中发生如下反应:
通入氨水中发生如下反应: ![]() ,当逸出的气体中含有0.28g
,当逸出的气体中含有0.28g ![]() 时,计算:
时,计算:
(1)参加反应的氨气的物质的量是多少?
(2)反应中被氧化的氨气的质量是多少克?
查看答案和解析>>
科目: 来源: 题型:
【题目】反应3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,试回答:
(1)增加Fe的量,其反应速率(填“增大”、“不变”或“减小”,下同).
(2)将容器的体积缩小一半,其反应速率 .
(3)保持体积不变,充入N2使体系压强增大,其反应速率 .
(4)保持压强不变,充入N2使容器的体积增大,其反应速率 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com