
【题目】合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
(1)【实验方案一】将铝镁合金与足量NaOH溶液反应,测定剩余固体质量.实验中发生反应的化学方程式是 【实验步骤】
称取5.4g铝镁合金粉末样品,溶于VmL 2.0mol/LNaOH溶液中,充分反应.则NaOH溶液的体积V≥ .
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将(填“偏高”、“偏低”或“无影响”).
(3)【实验方案二】 将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01105Pa)的体积.
【问题讨论】
同学们拟选用图1实验装置完成实验:
①你认为最简易的装置其连接顺序是:A接接接(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因. .
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 .
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平,读取量筒中水的体积
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了图2所示的实验装置. ①装置中导管a的作用是 .
②实验前后碱式滴定管中液面读数分别为V1mL、V2mL.则产生氢气的体积为mL.
【答案】
(1)2Al+2NaOH+2H2O=2NaAlO2+3H2↑;97mL
(2)偏高
(3)E;D;G;镁、铝与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大;ACD
(4)保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差;V1﹣V2
【解析】解:方案一:铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑; 所以答案是:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;(1)含镁为3%时,金属铝的含量最高,5.4g合金中铝的质量为,5.4g×(1﹣3%)=5.4×97%g,则:
2Al + | 2NaOH+2H2O=2NaAlO2+3H2↑ |
54g | 2mol |
5.4g×97%g | V×10﹣3L×2.0mol/L |
所以54g:(5.4g×97%g)=2mol:(V×10﹣3L×2.0mol/L),解得:V=97,故V(NaOH溶液)≥97mL;
所以答案是:97mL;(2)镁上会附着偏铝酸钠等物质,未洗涤导致测定的镁的质量偏大,镁的质量分数偏高,所以答案是:偏高;
方案二:(1)①装置的组装顺序:合金与水反应,用排水量气法测定氢气的体积,其中盛水的试剂瓶导管一定要短进长出,利用增大压强原理将水排出,量筒中水的体积就是生成氢气的体积,量筒内导管应伸入量筒底部,故连接顺序为:(A)接(E)(D)接(G);
所以答案是:E;D;G;
②镁、铝与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大,导致硫酸不能顺利滴入锥形瓶;
所以答案是:镁、铝与稀硫酸反应放热且生成气体,使锥形瓶中气体压强变大;
③反应放热导致氢气的温度偏高,故应冷却后再进行读取氢气的体积,读取实验中生成氢气的体积时上下移动量筒,使其中液面与广口瓶中液面相平,视线与凹液面的最低点水平读取氢气的体积;
故选ACD;(2)①装置中导管a的作用是:保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差;
所以答案是:保持分液漏斗内气体压强与锥形瓶内气体压强相等,打开分液漏斗活塞时稀硫酸能顺利滴下,滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差;
②滴定管的数值零刻度在上方,两次的体积之差为测定的氢气的体积,收集氢气后滴定管内液面读数减小,故测定氢气的体积为V1﹣V2;
所以答案是:V1﹣V2 .


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
【题目】金属晶体堆积密度大,原子配位数高,能充分利用空间的原因是( )
A.金属原子的价电子数较少
B.金属晶体中存在自由移动的电子
C.金属晶体的原子半径较大
D.金属键不具有方向性和饱和性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( ) 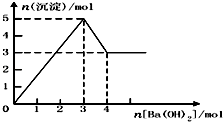
A.NH4Al(SO4)2
B.KAl(SO4)2
C.Al2(SO4)3
D.NaAlO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里要配制400mL0.2mol/L的硫酸钠溶液。
(1)实验步骤如下:A.在天平上称出g硫酸钠固体,把它放在烧杯里,用适量的蒸馏水溶解。
B.把得到的溶液冷却后小心地沿着注入 中。
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液也小心转入容量瓶中。
D.继续向容量瓶中加蒸馏水至液面距刻度l~2cm处,改用小心滴加蒸馏水至溶液凹液面底部与刻度线水平相切。
E.将瓶塞塞紧,充分摇匀。
F.将配好的溶液倒入试剂瓶中,贴上标签,并洗涤容量瓶。
请填写上述空白处。
(2)下列情况会使所配溶液浓度偏低的是(填序号)。
a.某同学定容时观察液面的情况如图所示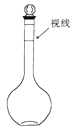
b.没有进行上述的操作步骤C
c.摇匀后发现液面低于刻度线
d.B操作时将少量液体洒到外面
e.容量瓶用前内壁沾有水珠
(3)如果实验室用18mol/L的浓硫酸配制3. 6mol·L-1的稀硫酸250mL。计算所需浓硫酸的体积为mL,在实验时应用量取浓硫酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
(1)【实验方案一】将铝镁合金与足量NaOH溶液反应,测定剩余固体质量.实验中发生反应的化学方程式是 【实验步骤】
称取5.4g铝镁合金粉末样品,溶于VmL 2.0mol/LNaOH溶液中,充分反应.则NaOH溶液的体积V≥ .
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将(填“偏高”、“偏低”或“无影响”).
(3)【实验方案二】 将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01105Pa)的体积.
【问题讨论】
同学们拟选用图1实验装置完成实验:
①你认为最简易的装置其连接顺序是:A接接接(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶.请你帮助分析原因. .
③实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 .
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平,读取量筒中水的体积
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小.于是他们设计了图2所示的实验装置. ①装置中导管a的作用是 .
②实验前后碱式滴定管中液面读数分别为V1mL、V2mL.则产生氢气的体积为mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是重要的氮肥,合成原理为:N2(g)+3H2(g) ![]() 2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
2NH3(g)△H=﹣92.4kJ/mol.回答下列问题:
(1)写出平衡常数K的表达式 , 如果降低温度,该反应K值E,化学反应速率 , N2的转化率(填“增大”、“减小”或“不变”).
(2)在500℃、20MPa时,将N2、H2置于一个容积为2L的密闭容器中发生反应,反应过程中各种物质的量变化如图所示,回答下列问题: 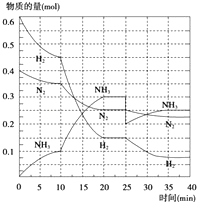
①10min内以NH3表示的平均反应速率: .
②在10~20min内:NH3浓度变化的原因可能是
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加NH3物质的量
③第1次平衡的时间为: , 第2次平衡的时间为: , 第1次平衡:平衡常数K1=(带数据的表达式),第2次平衡时NH3的体积分数;
④在反应进行至25min时,曲线发生变化的原因: ,
达第二次平衡时,新平衡的平衡常数K2K1 , (填“大于”、“小于”或“等于”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表所列各组物质中,物质之间通过一步反应能实现如图所示转化的是( )
X | Y | Z | |
① | Cu | CuO | Cu(OH)2 |
② | CH3CH2OH | CH3CHO | CH2=CH2 |
③ | S | SO3 | H2SO4 |
④ | NO | NO2 | HNO3 |
⑤ | FeCl2 | Fe | FeCl3 |

A.④⑤
B.③④
C.②⑤
D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g)在一可变容积的密闭容器中进行,试回答:
(1)增加Fe的量,其反应速率(填“增大”、“不变”或“减小”,下同).
(2)将容器的体积缩小一半,其反应速率 .
(3)保持体积不变,充入N2使体系压强增大,其反应速率 .
(4)保持压强不变,充入N2使容器的体积增大,其反应速率 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学式为C3H6O2的有机物的PMR谱有三个信号蜂,其强度比为3∶2∶1,则该有机物的结构简式不可能是
A. CH3CH2COOH B. CH3COOCH3
C. HCOOCH2CH3 D. CH3COCH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com