
科目: 来源: 题型:
【题目】PbI2是生产新型敏化太阳能电池的敏化剂﹣﹣甲胺铅碘的原料.合成PbI2的实验流程如图1: 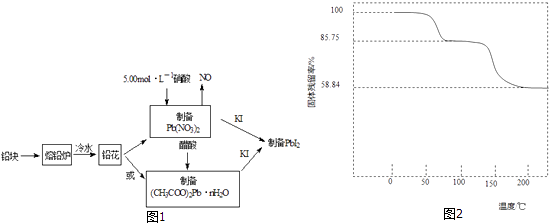
(1)将铅块制成铅花的目的是 .
(2)31.05g铅花用5.00molL﹣1的硝酸溶解,至少需消耗5.00molL﹣1硝酸mL,同时产生L(标准状况下)NO.
(3)取一定质量(CH3COO)2PbnH2O样品在N2气氛中加热,测得样品固体残留率( ![]() ×100%)随温度的变化如图2所示(已知:样品在75℃时已完全失去结晶水).
×100%)随温度的变化如图2所示(已知:样品在75℃时已完全失去结晶水).
①(CH3COO)2PbnH2O中结晶水数目n=(填数字).
②100~200℃间分解产物为铅的氧化物和一种有机物,则该有机物为(写结构简式).
(4)称取一定质量的PbI2固体,用蒸馏水配制成室温时的饱和溶液,准确移取25.00mLPbI2饱和溶液分次加入阳离子交换树脂RH中,发生:2RH(s)+Pb2+(aq)=R2Pb(s)+2H+(aq),用锥形瓶接收流出液,最后用蒸馏水淋洗树脂至流出液呈中性,将洗涤液合并到锥形瓶中.加入2~3滴酚酞溶液,用0.002500molL﹣1NaOH溶液滴定,到滴定终点时用去氢氧化钠标准溶液20.00mL.计算室温时PbI2 的Ksp (请给出计算过程).
查看答案和解析>>
科目: 来源: 题型:
【题目】三乙酸甘油酯是一种优良的溶剂、定香剂和增塑剂.实验室制备三乙酸甘油酯的反应原理、实验装置及相关数据如下:3CH3COOH+ ![]()
![]()
![]() +3H2O
+3H2O
物质 | 相对 | 密度/gcm﹣3 | 沸点/℃ | 水中 |
甘油 | 92 | 1.2636 | 290 | 溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
三乙酸甘油酯 | 218 | 1.1596 | 258 | 不溶 |

实验步骤:
步骤1.在500mL反应器中加入200g冰醋酸,92g甘油和100mL苯,开动搅拌器,慢慢从插温度计口加入3mL浓硫酸后,缓缓加热并回流1h,停止加热.
步骤2.用5%碳酸钠溶液洗涤,再用水洗涤,最后加入无水氯化钙.
步骤3.先进行常压蒸馏收集75~85℃馏分.
步骤4.将常压馏分再进行减压蒸馏,收集128~131℃/933Pa馏分,最终得产品176g.
(1)步骤1先开搅拌器后加浓硫酸的目的是;冰醋酸过量的目的是
(2)用5%碳酸钠溶液洗涤的主要目的是;加无水氯化钙的目的是
(3)最后用减压蒸馏而不用常压蒸馏其原因是
(4)本次实验产率为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应3Cl2+6NaOH==5NaCl+NaClO3+3H2O,以下叙述正确的是( )
A. Cl2是氧化剂,NaOH是还原剂
B. 被氧化的Cl原子和被还原的Cl原子的物质的量之比为5∶1
C. Cl2既做氧化剂又做还原剂
D. 氧化剂得电子数与还原剂失电子数之比为5∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】K4[Fe(CN)6]强热可发生反应:3K4[Fe(CN)6] ![]() 2 (CN)2↑+12KCN+N2↑+Fe3C+C
2 (CN)2↑+12KCN+N2↑+Fe3C+C
(1)K4[Fe(CN)6]中Fe2+的配位数为(填数字);Fe2+基态核外电子排布式为 .
(2)(CN)2分子中碳原子杂化轨道类型为;1mol(CN)2分子中含有σ键的数目为 .
(3)O ![]() 与CN﹣互为等电子体,则O
与CN﹣互为等电子体,则O ![]() 的电子式为 .
的电子式为 .
(4)Fe3C的晶胞结构中碳原子的配位数为6,碳原子与紧邻的铁原子组成的空间构型为 .
查看答案和解析>>
科目: 来源: 题型:
【题目】硫﹣氨热化学循环制氢示意图如下: 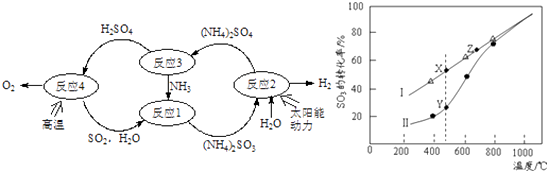
(1)反应1的离子方程式为 .
(2)反应2能量转化主要方式为 .
(3)反应3中控制反应条件很重要,不同条件下硫酸铵分解产物不同.若在400℃时分解,产物除水蒸气外还有A、B、C三种气体,A是空气中含量最多的单质,B能使湿润的红色石蕊试纸变蓝,C能使品红溶液褪色.则400℃时硫酸铵分解的化学方程式为 .
(4)反应4是由(a)、(b)两步反应组成:
H2SO4(l)=SO3(g)+H2O(g),△H=+177kJmol﹣1…(a)
2SO3(g)2SO2(g)+O2(g),△H=+196kJmol﹣1…(b)
①则H2SO4(l)分解为SO2(g)、O2(g)及H2O(g)的热化学方程式为: .
②在恒温密闭容器中,控制不同温度进行SO3分解实验.以SO3起始浓度均为cmolL﹣1 , 测定SO3的转化率,结果如图2,图中Ⅰ曲线为SO3的平衡转化率与温度的关系,Ⅱ曲线表示不同温度下反应经过相同反应时间且未达到化学平衡时SO3的转化率.
(i)图中点X与点Z的平衡常数K:
K(X)K(Z)(选填:>,<,=);
(ii)Y点对应温度下的反应速率:
v(正)v(逆)(选填:>,<,=);
(iii)随温度的升高,Ⅱ曲线逼近Ⅰ曲线的原因是: .
查看答案和解析>>
科目: 来源: 题型:
【题目】门捷列夫编制的第一张元素周期表,为元素的发现和研究元素性质铺平了道路,当时门捷列夫编排元素先后顺序的依据是( )
A. 原子半径B. 原子序数
C. 相对原子质量D. 质子数
查看答案和解析>>
科目: 来源: 题型:
【题目】丹参酮ⅡA是一种治疗心血管疾病的药物,其中的一种合成路线如下: 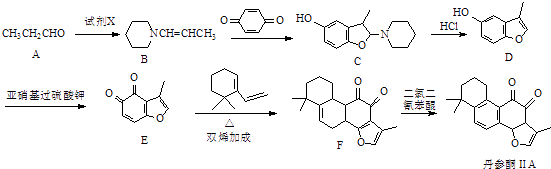
(1)丹参酮ⅡA中含氧官能团为和(写名称).
(2)试剂X的分子式为C5H11N,则X的结构简式为 .
(3)C→D的反应类型为 .
(4)写出同时满足下列条件的E的一种同分异构体的结构简式: .
Ⅰ.能发生银镜反应
Ⅱ.分子中除苯环外不含其它环状结构,分子中含有4种不同化学环境的氢
(5)写出以CH3CH=CHCH3和CH2=CHCHO为原料制备 ![]() 的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂可任选).合成路线流程图示例如下:
CH3CHO ![]() CH3COOH
CH3COOH ![]() CH3COOCH2CH3 .
CH3COOCH2CH3 .
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时加水稀释10mL pH=11的氨水,下列判断正确的是( )
A.原氨水的浓度为10﹣3mol?L﹣1
B.溶液中 ![]() 减小
减小
C.氨水的电离程度增大,溶液中所有离子的浓度均减小
D.再加入10 mL pH=3的盐酸充分反应后混合液的pH值肯定大于7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com