
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 氯气是一种红棕色、有毒的气体,氯气、液氯是同一种物质
B. 铁丝在氯气中燃烧,产生棕褐色的烟,产物溶于水,溶液呈浅绿色
C. 钠在氯气中燃烧,发出黄色的火焰,生成淡黄色固体
D. 氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白雾
查看答案和解析>>
科目: 来源: 题型:
【题目】碳纤维强化塑料是一种新型的高强度复合材料,其强度比钢铁材料大而密度比铝小。据报道,每架波音767飞机使用了1吨碳纤维材料,而一种新型的波音757飞机使用了9吨以上的碳纤维。制取碳纤维的一种方法是将聚丙烯腈纤维在稀有气体中进行高温处理而获得,这种碳纤维的结构可表示如下:
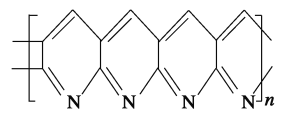
(1)构成这种碳纤维的元素是______,其原子个数比为_________。
(2)用乙炔和HCN为原料合成这种碳纤维的流程可表示如下:
CH≡CH![]() A
A![]() B
B![]() C
C![]() 碳纤维
碳纤维
用化学方程式表示以下过程:
①CH≡CH和HCN反应_______________________;
②A―→B________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列结论中,正确的是( )
A. 摩尔是七个基本物理量之一
B. 1molO2中约含有6.02×1023个氧分子
C. 6.02×1023称为阿伏加德罗常数
D. 标准状况下,22.4 L CO2和O2混合气体中含有的氧原子数为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列表示化学反应的离子方程式,其中正确的是:( )
A.NH4HSO3溶液与足量NaOH溶液共热:NH4++HSO3﹣+2OH﹣ ![]() ?NH3↑+SO32﹣+2H2O
?NH3↑+SO32﹣+2H2O
B.向氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2﹣+4NH4++2H2O
C.大理石溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O
D.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液Fe2++2H++H2O2═Fe3++2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】医用化学杂志曾报道,有一种功能高分子材料为聚乙交酯纤维材料C,用这种功能高分子材料制成的手术缝合线比天然高分子材料的肠线好。它的合成过程如下:
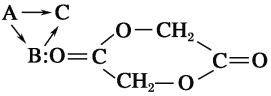
B是A合成C的中间体,它是由两分子A脱去两分子水形成的。
(1)写出由A合成C的化学方程式:____________________。
(2)写出由A制取B的化学方程式:____________________。
(3)医用高分子材料应具备哪些特性?
查看答案和解析>>
科目: 来源: 题型:
【题目】按照下列元素基态原子的电子排布特征判断元素,并回答问题。
A元素的原子中只有一个能层且只含1个电子;B元素的原子3p轨道上得到1个电子后不能再容纳外来电子;C元素的原子的2p轨道上有1个电子的自旋方向与其他电子的自旋方向相反;D元素的原子第三能层上有8个电子,第四能层上只有1个电子;E元素原子的外围电子排布为3s23p6。
(1)写出由A、B、C、D中的三种元素组成的化合物的化学式: (至少写出5个)。
(2)写出用上述元素组成的物质制得A的单质的化学方程式: 、
(3)检验某溶液中是否含有D+,可通过 反应来实现;检验某溶液中是否含有B-,通常所用的试剂是 和 。
(4)写出E的元素符号: ,要证明太阳上是否含有E元素,可采用的方法是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)利用VSEPR推断分子或离子的空间构型。
PO![]() __________;CS2____________;AlBr3(共价分子)__________。
__________;CS2____________;AlBr3(共价分子)__________。
(2)有两种活性反应中间体粒子,它们的粒子中均含有1个碳原子和3个氢原子。请依据下面给出的这两种粒子的球棍模型,写出相应的化学式:
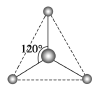 ______________;
______________;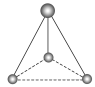 ______________。
______________。
(3)按要求写出第二周期非金属元素构成的中性分子的化学式。
平面三角形分子________,三角锥形分子________,四面体形分子________。
(4)为了解释和预测分子的空间构型,科学家在归纳了许多已知的分子空间构型的基础上,提出了一种十分简单的理论模型——价层电子对互斥模型。这种模型把分子分成两类:一类是____________________;另一类是____________________。
BF3和NF3都是四个原子的分子,BF3的中心原子是________,NF3的中心原子是________;BF3分子的立体构型是平面三角形而NF3分子的立体构型是三角锥形的原因是____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是元素周期表的简略框架图。

(1)请在上图所示的元素周期表中画出金属元素与非金属元素的分界线。按电子排布,可把元素划分成5个区,不全是金属元素的区为 。
(2)根据氢元素最高正化合价与最低负化合价的绝对值相等,你认为还可把氢元素放在元素周期表中的第 族;有人建议将氢元素排在元素周期表的第ⅦA族,请你写出支持这一观点的一个化学事实: 。
(3)上图中元素①②原子的价电子排布式分别为 、 。
比较元素①与元素②的下列性质(填“>”或“<”)。
原子半径:① ②;电负性:① ②;
金属性:① ②;第一电离能:① ②。
(4)某短周期元素最高正化合价为+7,其原子结构示意图为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】在研究原子核外电子排布与元素周期表的关系时,人们发现价电子层相似的元素集中在一起。据此,人们将元素周期表分为5个区,如图所示。
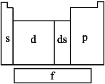
(1)在s区中,族序数最大、原子序数最小的元素是 ,其原子的外围电子的电子云形状为 。
(2)在d区中,族序数最大、原子序数最小的元素是 ,其常见离子的电子排布式为 ,其中较稳定的是 。
(3)在ds区中,族序数最大、原子序数最小的元素是 ,其原子的价电子层为 。
(4)在p区中,第二周期第ⅤA族元素原子的外围电子排布图为 。
(5)当今常用于核能开发的元素是铀和钚,它们在周期表中位于 区。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com