
科目: 来源: 题型:
【题目】已知:W是地壳中含量居第二位的元素,且X、Y、Z、W在元素周期表中的位置如图所示。下列说法正确的是
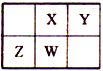
A. 最高正化合价:Z>X=W>Y B. 原子半径:Y>X>W>Z
C. 最高价氧化物对应水化物的酸性:Z<W<X<Y D. 最高价含氧酸的钠盐溶液能与CO2反应的元素:X、Y、Z、W
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E五种主族元素的原子序数依次增大,且均小于18.A原子的最外层电子比B原子的最外层电子少2个,B原子的质子数是其电子层数的4倍.A、B、C三种元素能结合成化合物C2AB3,在lmolC2AB3中共有52mol电子。D元素的单质0.5mol与酸全部反应时,有9.03×1023个电子转移。E元素的单质是一种黄绿色气体,水溶液具有漂白性。试填写下列空白:
(l)写出元素A 和E 的名称:A , E 。
(2)元素B在周期表中的位置为第二周期 族.
(3)由元素B、C形成的一种化合物可以作为呼吸面具的供氧剂,该化合物为含有 键(填“极性”或“非极性”)的 化合物(填“离子”或“共价”) ,写出该化合物的电子式 。
(4)写出C、D两种元素对应的最高价氧化物的水化物相互反应的离子方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】溴化碘(IBr)的化学性质与卤素单质相似,能与大多数金属反应生成金属卤化物,和某些非金属单质反应生成相应的卤化物,跟水反应的方程式为IBr+H2O==HBr+HIO。下列有关IBr的叙述中,不正确的是
A. IBr的电子式:![]()
B. IBr和Zn的反应化学方程式2IBr+2Zn==ZnI2+ZnBr2
C. IBr和NaOH溶液反应生成NaBr和NaIO
D. IBr和水反应时,既是氧化剂又是还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素甲、乙、丙、丁、戊在元素周期表中的相对位置如表所示,其中丁所处的主族序数是其周期序数的三倍。回答下列问题:
乙 | 丙 | 丁 | |
甲 | 戊 |
(1)乙在元素周期表中的位置是___________________。
(2)原子半径:戊______甲(填“>”或“<”)。
(3)乙与戊组成化合物的电子式为______,其中化学键的类型是_____(填“极性”或“非极性”)共价键。
(4)元素的非金属性:甲______丙(填“>”或“<”),下列事实能说明该结论的是_______(填字母)。
A.丙的氢化物稳定,甲的氢化物不稳定
B.丙的最高价氧化物对应的水化物是强酸,甲的是弱酸
C.丙的最高价氧化物对应的水化物易溶于水,甲的难溶
(5)工业上制取甲(粗品)的化学方程式为_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知X的最低负价与Y的最高正价代数和为零,下列说法正确的是
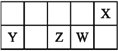
A. 原子半径的大小顺序:r(Y)>r(Z)>r(W)>r(X)
B. Z的最高价氧化物对应水化物的酸性比W的强
C. X的简单气态氢化物的稳定性比W的弱
D. X分别与Y、Z形成的化合物中化学键类型相同
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25℃时Ksp[Al(OH)3]=1.0×10﹣33 , Ksp[Fe(OH)3]=4.0×10﹣38 . 向Fe(NO3)3和Al(NO3)3的混合溶液中逐滴加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积的关系如下图所示.计算表明当Fe3+完全沉淀时,Al3+恰好开始沉淀.下列说法正确的是( ) 
A.原混合溶液中c(Fe3+):c(Al3+)=1:1
B.Fe(NO3)3溶液中混有杂质Al(NO3)3可以加入过量的NaOH溶液除去
C.B点两种沉淀共存,此时上层溶液中c(Al3+):c(Fe3+)=2.5×104
D.C点溶液中的溶质只有NaAlO2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的分类正确的是( )
选项 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | NO |
C | KOH | HNO3 | CaCO3 | CaO | Mn2O7 |
D | NaOH | HCl | CaF2 | Na2O2 | SO2 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 氯气溶于水:Cl2+H2O==2H++Cl-+ClO-
B. 过量HI溶液加入到Fe(NO3)3溶液中:2Fe3++2I-=2Fe2++I2
C. 酸性溶液中KBrO3与KBr反应生成Br2:BrO3-+Br-+6H+=Br2+3H2O
D. NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+ Ba2++OH-=BaCO3↓+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】氨基甲酸铵(NH2COONH4)是重要的氨化剂,在潮湿的空气中能转化为碳酸铵,受热易分解、易被氧化。实验小组对氨基甲酸铵的性质进行了如下探究。请回答下列问题:
(1)氨基甲酸铵在潮湿的空气中转化为碳酸铵的化学方程式为____________________________。
(2)用下图装置探究氨基甲酸铵的分解产物(夹持装置略去,下同)。

①点燃A处的酒精灯之前,需先打开k,向装置中通入一段时间的N2,目的为_________________。
②仪器B的名称为_________________。
③装置D的作用为________________________________________________________。
④能证明分解产物中有NH3的现象为_________________________________________。
⑤试剂A用于检验分解产物中的CO2,该试剂的名称为_______________________。
(3)已知:CuO高温能分解为Cu2O和O2。若用上述装置和下列部分装置进一步检验分解产物中是否有CO,装置E后应依次连接_________________(按从左到右的连接顺序填选项字母)。
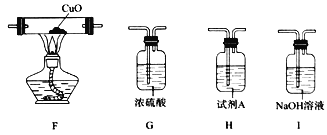
(4)通过实验得出结论:氨基甲酸铵受热分解为NH3和CO2。该反应的化学方程式为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将0.2mol的镁、铝混合物溶于200mL4mol/LHCl溶液中,然后再滴加2mol/LNaOH溶液。
(1) 若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如下图所示。当V1=160mL时,则金属粉末中n(Mg)=______mol,V2=______mL。
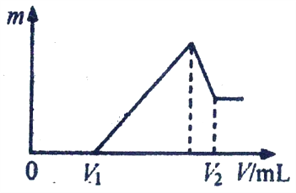
(2) 若在滴加NaOH 溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=______mL。
(3) 若混合物仍为0.2mol。其中Mg粉的物质的量分数为a,用200mL4mol/LHCl溶解此混合物后,再加入450mL2mol/L的NaOH溶液,所得沉淀中无Al(OH)3。满足此条件的a的取值范围是:__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com