
科目: 来源: 题型:
【题目】金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。
(1) 镓(Ga)的原子结构示意图为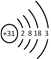 ,镓元素在周期表中的位置是_______。
,镓元素在周期表中的位置是_______。
(2)镓能与沸水剧烈反应生成氢气和氢氧化镓,该反应的化学方程式是______________。
(3)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。
资料:镓的熔点较低(29.8℃),沸点很高(2403℃)。
①传统的氮化镓(GaN)制备方法是采用GaCl3与NH3在一定条件下反应,该反应的化学方程式是____________________。
②当代工业上固态氮化镓(GaN)的制备方法是利用镓与NH3在1000℃高温下合成,同时生成氢气,每生成l mol H2时放出10.27 kJ热量。该可逆反应的热化学方程式是 ____________________________________。
③在密闭容器中,充入一定量的Ga与NH3发生上述反应,实验测得反应平衡体系中NH3的体积分数与压强P和温度T的关系曲线如图1所示。
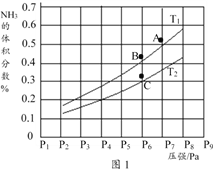
图中A点和C点化学平衡常数的关系是:KA_____ KC (填“>”“=”或“<”),理由是_____________________________。
(4)电解法可以提纯粗镓,具体原理如图2所示:
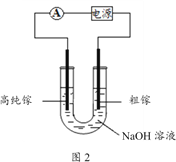
①粗镓与电源____极相连。(填“正”或“负”)
②镓在阳极溶解生成的Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电的电极反应式是
_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为满足不同的需要,人们应用原电池原理制作了多种电池。
(1)有人以化学反应2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作,则该原电池负极的电极反应为___________。
(2)FeCl3溶液常用于腐蚀印刷电路铜板,其反应的离子方程式为________________;若将此反应设计或原电池,则负极所用电极材料为___________,正极反应为_________________。
(3)美国阿波罗宇宙飞船上使用了一种新型发电装置—氢氧燃料电池,其构造如图所示,其中A、B两个电极均由多孔的碳炔组成,该电池的正极反应式为_________________,若该电池工作时溶液中增加1molH2O,则理论上电路中通过电子的物质的量为_______________。

查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在研究前18号元素时发现,可以将它们排成如下图所示的“蜗牛”形状,图中每个“·”代表一种元素,其中O点代表氢元素。下列说法中错误的是

A. 离O点越远的元素原子半径越大 B. 虚线相连的元素处于同一族
C. B元素是图中金属性最强的元素 D. A、B组成的化合物中可能含有共价键
查看答案和解析>>
科目: 来源: 题型:
【题目】学习与研究化学经常要进行实验,请完成以下课题:
(1)玻璃棒的作用主要有以下三种,请回答下列问题: a.搅拌 b.引流 c.蘸取溶液
①实验室配制一定物质的量浓度溶液,将固体溶解时,玻璃棒的作用是(填字母),
②将烧杯中的溶液注入容量瓶时,玻璃棒的作用是(填字母),
③用浓盐酸检验氨气时,玻璃棒的作用是(填字母),
④粗盐提纯时,用过滤的方法除去不溶性的泥沙,玻璃棒的作用是(填字母).
(2)现用98%的浓H2SO4(ρ)=1.84g/cm3)配制浓度为0.5mol/L的稀硫酸500mL. ①选用的玻璃仪器除了量筒、玻璃棒、烧杯,还用到、 .
②将浓H2SO4沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌的目的是 , 若搅拌过程中有液体溅出,会使最终结果(填“偏高”、“偏低”或“无影响”).
③定容时必须使溶液凹液面与刻度线相切,若俯视会使结果(填“偏高”、“偏低”或“无影响”).
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物I是重要有机中间体,其合成路线(部分反应条件已略去)如下图所示:

已知:
R — CN![]() R — COOH
R — COOH
回答下列问题:
(1)A的结构简式是______________。
(2)B中含有的官能团是______________。
(3)D是一种合成高分子,它的结构简式是______________。
(4)I发生缩聚反应的化学方程式是______________。
(5)G→H的反应类型是______________。
(6)E→F反应的化学方程式是______________。
(7)下列说法正确的是________。
①物质I能发生消去反应
②F→G过程产生的副产物 物质G互为同分异构体
物质G互为同分异构体
③B、D均存在顺反异构
(8)结合题给信息,以乙烯、HBr为起始原料制备丙酸,设计合成路线(其他试剂任选)________。(合成路线常用的表示方式为:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】CO和NO都是汽车尾气中的有害物质,它们之间能缓慢地发生如下反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ΔH<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列设计方案可以最有效的提高尾气处理效果的是 ( )
N2(g)+2CO2(g) ΔH<0,现利用此反应,拟设计一种环保装置,用来消除汽车尾气对大气的污染,下列设计方案可以最有效的提高尾气处理效果的是 ( )
①选用适当的催化剂 ②提高装置温度 ③降低装置的压强 ④装置中放入碱石灰
A. ①④ B. ②④ C. ① D. ②③
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关金属腐蚀与防护的说法正确的是
A. 纯银器表面在空气中因电化学腐蚀渐渐变暗
B. 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
C. 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
D. “辽宁号”外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学探究SO2使品红溶液褪色的过程,将SO2通入水中得到pH=2的溶液A,后续操作如下,下列说法不正确的是
实验1 |
|
实验2 |
|
A. 溶液A的pH=2原因是:SO2 + H2O![]() H2SO3
H2SO3 ![]() H+ + HSO3-
H+ + HSO3-
B. 实验1、实验2均体现了SO2的还原性和漂白性
C. 经实验1、2对比可知品红溶液褪色的过程是可逆的
D. 实验2中加入NaOH溶液调节pH =2 的原因是排除H+浓度变化产生的干扰
查看答案和解析>>
科目: 来源: 题型:
【题目】恒容密闭容器中进行反应mX(g)+nY(g) ![]() qZ(g)ΔH>0,m+n<q达到平衡时,下列说法正确的是 ( )
qZ(g)ΔH>0,m+n<q达到平衡时,下列说法正确的是 ( )
A. 通入稀有气体使压强增大,平衡将正向移动
B. X的逆反应速率是Y的正反应速率的n/m倍
C. 降低温度,混合气体的平均相对分子质量变小
D. 增加X的物质的量,X的转化率降低
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com