
科目: 来源: 题型:
【题目】下列有关细胞分子的叙述,正确的是( )
A. 携带遗传信息是核酸的唯一功能
B. 叶肉细胞中缺乏 Mg 元素,则影响叶绿素合成
C. 氨基酸的空间结构是蛋白质多样性的原因
D. 等质量脂肪氧化分解比糖释放能量多是因为脂肪分子中氧含量多
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学一一选修5:有机化学基础]愈创木酚(化合物E)是一种重要的精细化工中间体,广泛应用于医药、香料及染料的合成。其合成路线及某种应用如图(部分产物及条件已略去):

已知:①R1X+R2ONa→R1-O-R2+NaX
②![]()
③化合物F能发生水解反应,不能使FeCl3显色
④化合物G可用于水果催熟
(1)C分子中含有的官能团名称为______________________________。
(2)由B生成C的反应类型为______________________________。
(3)D的结构简式为______________________________。
(4)由A 生成B 的化学方程式为______________________________。
(5)F和足量NaOH溶液反应的化学方程式为______________________________。
(6)化合物M比F的相对分子质量小28,同时满足以下条件的M的同分异构体有_______种(不考虑立体异构)。①遇FeCl3溶液显紫色 ②能发生银镜反应
其中核磁共振氢谱峰面积之比为1:1:2:2的M的结构简式为___________(任写一种)。
(7)参照愈创木酚的合成路线格式,设计一条由化合物G为起始原料经三步合成化合物H的合成路线_____________________。(反应条件需全部标出)
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,已知弱酸的电离常数:K(CH3COOH)=1.8×10﹣5;K1(H2CO3)=4.4×10﹣7;K2(H2CO3)=4.7×10﹣11;K(HClO)=4.0×10﹣8 . 则下列说法正确的是( )
A.25℃时,0.1mol/L的醋酸溶液比0.01mol/L的醋酸溶液的K值小
B.25℃时,甲基橙滴入0.1mol/L的醋酸溶液中,溶液呈黄色
C.新制氯水与碳酸氢钠不反应
D.等物质的量浓度的碳酸钠溶液、醋酸钠溶液、次氯酸钠溶液的pH:pH[Na2CO3(aq)]>pH[NaClO(aq)]>pH[CH3COONa(aq)]
查看答案和解析>>
科目: 来源: 题型:
【题目】反应4A(s)+3B(g)═2C(g)+D(g),经2min,B的浓度减少0.6mol/L.对此反应速率的表示正确的是( )
A.用A表示的反应速率是0.4 mol(Lmin)﹣1
B.分别用B,C,D表示的反应速率其比值是3:2:1
C.在2min末的反应速率,用B表示是0.3 mol(Lmin)﹣1
D.在这2min内用B和C表示的反应速率的值都是逐渐减小的
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学——选修3:物质结构与性质]X、Y、Z、W、R五种短周期非金属元素原子序数依次增大,X、Y、Z、W为同周期元素且未成对电子数之比为1:2:3:2,R和Z同主族。请回答下列问题:
(1)Z的基态原子的价层电子排布图为______________________________。
(2)Z、W、R 三种元素的电负性由大到小的顺序为_____________(用元素符号表示)。
(3)W的常见氢化物的氢键的键能小于HF氢键的键能,但W的常见氢化物常温下为液态而HF常温下为气态的原因是_______________________________。
(4)某种分子式为Y4Z4W8的物质(该物质中同种原子的化学环境完全相同,不含碳碳双键)是一种威力极强的炸药,则可推知其结构简式为_________________________。
(5)XR是一种耐磨材料,可由X的三溴化物和R的三溴化物于高温下在氧气的氛围中合成。
①X的三溴化物分子中X原子的杂化方式为_______________,R的三溴化物分子的空间构型的名称为_____________________。
②合成XR的化学方程式为_____________________。
(6)Y与W形成的某种常见化合物的晶胞如图, 该晶体中分子的配位数为__________________,若晶胞的棱长为a nm,阿伏加德罗常数的值为NA,晶体的密度为______g/cm3。
该晶体中分子的配位数为__________________,若晶胞的棱长为a nm,阿伏加德罗常数的值为NA,晶体的密度为______g/cm3。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应不属于取代反应的是
A. C2H4+Cl2→C2H4Cl2
B. 2C2H5OH![]() C2H5OC2H5+H2O
C2H5OC2H5+H2O
C. C2H5Cl+H2O![]() C2H5OH+HCl
C2H5OH+HCl
D. CH4+4Cl2![]() CCl4+4HCl
CCl4+4HCl
查看答案和解析>>
科目: 来源: 题型:
【题目】乙烯是一种重要的化工原料,可由乙烷为原料制取,回答下列问题。
(1)传统的热裂解法和现代的氧化裂解法的热化学方程式如下:
①C2H6(g)=C2H4(g) +H2(g) ΔH1=+136 kJ/mol
②C2H6(g)+ ![]() O2(g)= C2H4(g)+H2O(g) ΔH2=-110 kJ/mol
O2(g)= C2H4(g)+H2O(g) ΔH2=-110 kJ/mol
已知反应相关的部分化学键键能数据如下:
化学键 | H-H(g) | H-O(g) | O=O(g) |
键能( kJ/mol) | 436 | X | 496 |
由此计算x=_________,通过比较△H1和△H2,说明和热裂解法相比,氧化裂解法的优点是_______________________________(任写一点)。
(2)乙烷的氧化裂解反应产物中除了C2H4外,还存在CH4、CO、CO2等副产物(副反应均为放热反应),图1为温度对乙烷氧化裂解反应性能的影响。乙烷的转化率随温度的升高而升高的原因是______,反应的最佳温度为____________(填选项序号)。
A.700℃ B.750℃ C.850℃ D.900℃
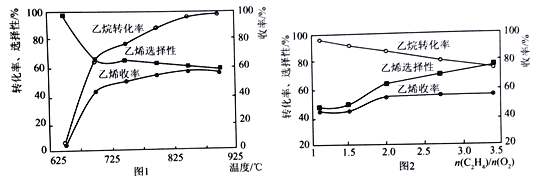
[乙烯选择性=![]() ;乙烯收率=乙烷转化率×乙烯选择性]
;乙烯收率=乙烷转化率×乙烯选择性]
(3)烃类氧化反应中,氧气含量低会导致反应产生积炭,堵塞反应管。图2为n(C2H6)/n(O2)的值对乙烷氧化裂解反应性能的影响。判断乙烷氧化裂解过程中n(C2H6)/n(O2)的最佳值是_______________,判断的理由是__________________________________。
(4)工业上,保持体系总压恒定为100kPa的条件下进行该反应,通常在乙烷和氧气的混合气体中掺混惰性气体(惰性气体的体积分数为70%),掺混惰性气体的目的是___________________________。
反应达平衡时,各组分的体积分数如下表:
C2H6 | O2 | C2H4 | H2O | 其他物质 |
2.4% | 1.0% | 12% | 15% | 69.6% |
计算该温度下的平衡常数Kp=_________(用平衡分压代替平衡浓度,平衡分压=总压×体积分数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com