
科目: 来源: 题型:
【题目】下列平衡体系中,升温或减压都能使平衡向正反应方向移动的是(ΔH<0表示放热)( )
A.N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0
2NH3(g) ΔH<0
B.N2(g)+O2(g) ![]() 2NO(g) ΔH<0
2NO(g) ΔH<0
C.2SO2(g)+O2(g) ![]() 2SO3(g) ΔH<0
2SO3(g) ΔH<0
D.C(s)+2H2O(g) ![]() CO2(g)+2H2(g) ΔH>0
CO2(g)+2H2(g) ΔH>0
查看答案和解析>>
科目: 来源: 题型:
【题目】13.在密闭容器中一定量混合气体发生反应:xA(g)+yB(g) ![]() zC(g)平衡时测得A的浓度为0.5 mol·L-1 , 保持温度不变,将容器的容积扩大到原来的2倍,再达平衡时测得A的浓度为0.2 mol·L-1 , 下列判断正确的是( )
zC(g)平衡时测得A的浓度为0.5 mol·L-1 , 保持温度不变,将容器的容积扩大到原来的2倍,再达平衡时测得A的浓度为0.2 mol·L-1 , 下列判断正确的是( )
A.平衡向正反应方向移动
B.x+y>z
C.C的体积分数保持不变
D.B的转化率降低
查看答案和解析>>
科目: 来源: 题型:
【题目】环境保护要求燃煤污染物控制排放,研究协同脱硫脱硝工艺是大势所趋。
Ⅰ量子化学计算能揭示出化学反应机理。
SO2与ClO2的气态反应中,因接触位置不同,形成了不同反应路径,反应中各驻点(TS为过渡态,RC、IM、PC为中间产物)相对初始反应物的能量关系如图1所示
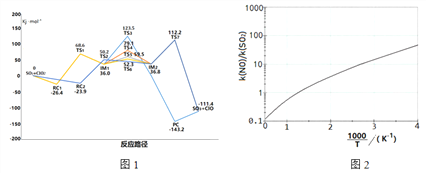
(1)写出该过程的热化学方程式:____________________。
(2)图中IM1→IM2,经历过渡态_____的路径反应速率最慢,其原因是______。
(3)在图中描线指出该反应的最优微观路径。____________
(4)产物ClO也有强氧化性,可以继续氧化SO2。请写出该反应的化学方程式______。
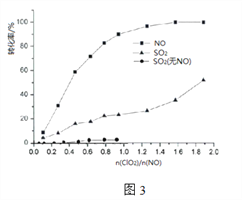
(5)ClO2分别氧化NO和SO2反应速率常数之比与温度关系如图2所示,可推知随温度升高,ClO2氧化NO反应速率_______。
Ⅱ模拟烟气的组成为:0.03%NO、0.1%SO2、6.0%O2、8.0%H2O,在70℃下,当n(C1O2):n(NO)不断增大(其余为氮气)时,SO2和NO的转化率变化如图3所示。
(6)有NO存在时,ClO2氧化SO2______(填“难”、“易”),造成这种情况的可能原因是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应属于氧化还原反应,且HCl既不作氧化剂也不作还原剂的是( )
A.PbO2+4HCl=PbCl2+Cl2↑+2H2OB.NaOH+HCl=NaCl+H2O
C.2FeCl2+H2O2+2HCl=2FeCl3+2H2OD.Zn+2HCl=ZnCl2+H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】已知在稀溶液中,酸跟碱发生中和反应生成1 mol水时的反应热叫做中和热。现利用如图装置进行中和热的测定,请回答下列问题:

(1)图示装置有两处重要组成部分未画出,它们是____________ 、_______________。
(2)烧杯间填满碎泡沫塑料的作用是 ________________。
(3)若操作时分几次注入反应液,求得的反应热数值_____(填“偏大”“偏小”或“无影响”)。
(4)做一次完整的中和热测定实验,温度计需使用__________次。
(5)量取0.5 mol/L的盐酸和0.55 mol/L的NaOH溶液各50 mL进行实验,测得盐酸和NaOH溶液起始平均温度为t1℃,混合反应后最高温度为t2℃,设溶液密度均为1 g/mL,生成溶液的比热容c= 4.18 J/(g℃)。请列式计算中和热:△H= ______________kJ/mol(不用化简)。
查看答案和解析>>
科目: 来源: 题型:
【题目】TiO2和CaTiO3都是光电转化材料,某研究小组利用钛铁矿(主要成分为FeTiO3,还含有少量SiO2等杂质)来制备,并利用黄钾矾(KFe3(SO4)2(OH)6)回收铁的工艺流程如下:

回答下列问题:
(1)“氧化酸解”的实验中,控制反应温度为150℃,不同氧化剂对钛铁矿酸解率的影响如图所示。50min时,要求酸解率大于85%,所选氧化剂应为____________;采用H2O2做氧化剂时,其效率低的原因可能是_______________________。
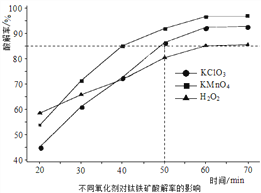
(2)“氧化酸解”的滤液①中加入尿素CO(NH2)2, TiO2+转化为TiO2,写出相应的离子方程式_____________________,使用尿素而不直接通入NH3的原因是_____________。
(3)写出“高温煅烧”中由TiO2制备CaTiO3的化学方程式________________。
(4)使Fe3+恰好沉淀完全时,溶液中c(Fe3+)=1.0×10-5mol·L-1,列式计算此时溶液的pH________。(Fe(OH)3的Ksp=1.0×10-39、水的Kw=1.0×10-14 mol2·L-2)
(5)黄钾钒为沉淀为晶体,含水量很少。回收Fe3+时,不采用加入氨水调节pH制得Fe(OH)3的原因是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在理论上可用于设计原电池的化学反应是 ( )
A.2Al(s)十2NaOH(aq)+2H2O(1)=2NaAlO2(ag)+3H2(g);△H <0
B.Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(aq)+2NH3·H2O(aq)+8H2O(1);△H >0
C.CaC2(s)+2H2O(1)→Ca(OH)2(s)+C2H2(g);△H <0
D.FeCl3(aq)十3H2O(1) ![]() Fe(OH)3(s)+3HCl(aq);△H >0
Fe(OH)3(s)+3HCl(aq);△H >0
查看答案和解析>>
科目: 来源: 题型:
【题目】锌元素对婴儿及青少年的智力和身体发育有重要的作用,被称为生命火花。利用恒电势电解NaBr溶液间接将葡萄糖[CH2OH(CHOH)4CHO]氧化为葡萄糖酸[CH2OH(CHOH)4COOH],进而制取葡萄糖酸锌,装置如图所示,下列说法错误的是

A. 钛网与直流电源的正极相连
B. 石墨电极的反应为:2H2O+2e-=H2↑+2OH-
C. 电解过程中硫酸钠溶液浓度保持不变
D. .生成葡萄糖酸的方程式为:CH2OH(CHOH)4CHO+Br2+H2O=CH2OH(CHOH)4COOH+2HBr
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com