
科目: 来源: 题型:
【题目】微量元素硼和镁对植物的叶的生长和人体骨骼的健康有着十分重要的作用。请回答下列问題:
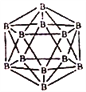
(1)区分晶体硼和无定形硼最可靠的科学方法为________。晶体硼的结构单元是正二十面体,每个单元中有12个硼原子(如图)。若每个单元中有两个原子为10B,其余为11B,则该单元结构的类型有___种。
(2)NaBH4是一种重要的储氢载体,阴离子结构式为________。
(3)图1表示多硼酸根的一种无限长的链式结构,其化学式可表示为____(以n表示硼原子的个数)。
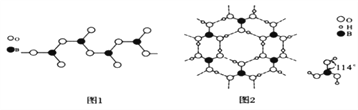
(4)硼酸晶体是片层结构,有与石墨相似的层状结构,图2表示的是其中一层的结构。硼酸晶体中存在的作用力有共价键、________、________。与H3BO3酸性最接近的是________(填字母)。
A.H4SiO4 B.H3PO4 C.HNO2
硼酸晶体在冷水中溶解度很小,但在热水中较大,原因是____________________。
(5)镁的堆积方式为________________,配位数为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以硅孔雀石(主要成分为 CuCO3·Cu(OH)2、CuSiO3·2H2O,含 SiO2、FeCO3、 Fe2O3等杂质)为原料制备CuCl2的工艺流程如下:
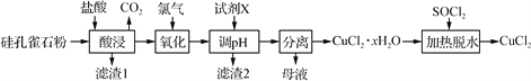
(1)为提高“酸浸”时铜元素的浸出率,可以采取的措施有:
①适当加快搅拌速率;②______________。(任答一点即可)
(2)“氧化”时发生反应的离子方程式为__________。
(3)“滤渣1”的主要成分为SiO2和H2SiO3等,“滤渣2”的主要成分为______(填化学式);试剂X可选择_____(填字母)。
a. Cu b. NaOH c. Cu(OH)2 d.氨水
(4)“调pH”时,pH不能过高,其原因是_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列过程中属于人工固氮的是( )
A.雷雨天气时产生少量NO
B.往农田中施放铵态氮肥
C.豆科植物等根部的根瘤菌吸收空气中的氮气转变为氨
D.N2和H2在高温、高压和催化剂存在下合成氨
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应原理对生产有重大的指导意义。回答下列问题:
(1)有两个温度相同的密闭容器A和B,容器A保持容积不变,容器B保持压强不变,起始时向容积相等的A、B中分别充入等量的C(碳)和H2O(g),发生反应:C(s)+H2O(g)![]() CO(g)+ H2(g) (正反应为吸热反应),并分别达到平衡。
CO(g)+ H2(g) (正反应为吸热反应),并分别达到平衡。
①H2O的体积分数:V(A)%_____V(B)%。(填“>”、“<” “=”)
②达到平衡后,在两容器中分别通入等量的氦气,则A中H2O的转化率_______(填“增大” “减小”、“不变”);B中化学平衡_________移动(填“不”“向正反应方向”“向逆反应方向”)。
(2)某温度下,测得0.01mol·L-1 NaOH溶液的pH=10,则在该温度下Kw=______;在此温度下,将pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合,若所得溶液为中性,则a:b=_______(假设混合时体积不变)。
查看答案和解析>>
科目: 来源: 题型:
【题目】环保部门每天通过新闻媒体向社会发布以污染物浓度为标准确定空气质量的信息.这些污染物是( )
A.二氧化硫、氮氧化物、悬浮微粒
B.二氧化硫、氮氧化物、一氧化碳
C.三氧化硫、氮氧化物、悬浮微粒
D.稀有气体、氮氧化物、悬浮微粒
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A是来自石油的重要有机化工原料,其产量用来衡量一个国家石油化工发展水平,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。

(1) A的名称为____;C分子中的官能团名称为_________。
(2)反应③的化学方程式为_________;该反应的反应类型为_________。
(3)反应④的化学方程式为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家在研究生物体的化学成分时,发现组成生物体的元素在非生物界都存在,这一事实说明 ( )
A. 生物界和非生物界没有区别 B. 组成生物的物质来源于非生物
C. 生物界和非生物界具有统一性 D. 生物界和非生物界具有差异性
查看答案和解析>>
科目: 来源: 题型:
【题目】已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4![]() 2AsH3↑+6ZnSO4+3H2O。
2AsH3↑+6ZnSO4+3H2O。
(1)请用双线桥法标出电子转移的方向和数目____________________________________。
(2)As2O3在上述反应中显示出来的性质是____________(填序号)。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物是__________,还原产物是________。
(4)若生成0.2 mol AsH3,则转移的电子数为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在标准状况下,将224 L氯化氢气体溶于635 mL的水(密度为1.00 g/cm3)中,所得盐酸的密度为1.18 g/cm3。求:
(1)该盐酸的溶质质量分数是多少?______________
(2)取这种盐酸10.0 mL,稀释到1.00 L,所得的稀盐酸的物质的量浓度多少?____________
查看答案和解析>>
科目: 来源: 题型:
【题目】苯乙烯是工业上是合成树脂、离子交换树脂及合成橡胶等的重要单体,工业上可用乙苯催化脱氢方法制备苯乙烯:![]() (g)
(g)![]()
![]() (g)+H2(g) △H=+QkJ·mol-1
(g)+H2(g) △H=+QkJ·mol-1
请回答下列问题:
(1)已知乙苯(g)、苯乙烯(g)的燃烧热分别为a kJ·mol-1、bkJ·mol-1,则氢气的燃烧热为________kJ·mol-1(用含有Q、b、c的表达式表示,其中Q、b、c均大于0)。
(2)673 K时,在一恒容密闭容器中充入5 mol乙苯(g),反应达到平衡后容器内气体的压强为p1;若再充入amol的乙苯(g),重新达到平衡后容器内气体的压强为2p1,则a________5。
(3)在实际生产中,在恒压条件下常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),此时乙苯的平衡转化率与水蒸气的用量、压强(p)的关系如图所示。
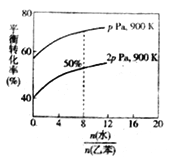
①加入水蒸气稀释剂能提高乙苯转化率的原因是___________________________。
②用平衡分压代替平衡浓度计算,其中,分压=总压×物质的量分数,则900K时的平衡常数Kp=________。
③改变下列条件,能使乙苯的反应速率和转化率一定增大的是________(填标号)。
A.恒容时加入稀释剂水蒸气 B.压强不变下,温度升至1500 K
C.在容积和温度不变下充入Ar D.选用催化效果更好的催化剂
(4)已知苯乙烯可催化氧化生成苯乙醛:![]() (g)+2O2→
(g)+2O2→![]() + CO2+H2O,若把该反应设计为酸性燃料电池,则电池负极的电极反应式为_________________,若该电池消耗标准状况下11.2 L的O2,则外电路中理论上应转移电子的物质的量为________mol。
+ CO2+H2O,若把该反应设计为酸性燃料电池,则电池负极的电极反应式为_________________,若该电池消耗标准状况下11.2 L的O2,则外电路中理论上应转移电子的物质的量为________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com