
科目: 来源: 题型:
【题目】下列各组离子中,能在溶液里大量共存的是
A.K+、Na+、OH-、Cl-B.Mg2+、Na+、SO42-、OH-
C.Cu2+、Ba2+、SO42-、Cl-D.H+、Ca2+、CO32-、Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】装置a、b、c中分别盛有试剂1、2、3,用如图所示的装置进行实验(夹持仪器略去,必要时可加热),能达到相应实验目的的是
选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 | 装置 |
A | 浓 | Cu片 | KI-淀粉溶液 | 验证 |
|
B | 盐酸 | 石灰石 | 饱和 | 制备 | |
C | 稀硫酸 | 溶液X | 澄清石灰水 | 验证溶液X中是否有 | |
D | 70%硫酸 |
| 酸性 | 证明 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】将氢气通入10 g 氧化铜粉末加热片刻,冷却后剩余固体的质量为8.4 g,下列计算正确的是
A. 有1.6 g 水生成
B. 有8.4 g 铜生成
C. 有80%的氧化铜被还原
D. 实验时所消耗的氢气不足0.2 g
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.Fe的摩尔质量是56g/mol
B.0.1mol/LKCl溶液中含有0.1molK+
C.1molN2中含有的原子数约为6.02×1023
D.常温常压下,1molCO的体积是22.4L
查看答案和解析>>
科目: 来源: 题型:
【题目】白钠镁矾(mNa2SO4·nMgSO4·xH2O)俗称硝板,工业上用白钠镁矾制备碱式碳酸镁[4MgCO3·Mg(OH)2·4H2O]晶须的过程如下:向碳酸钠溶液中加入白钠镁矾,保持50℃加热0.5h,有大量的5MgCO3·3H2O生成,然后升高温度到85℃加热2h发生热解反应,过滤得碱式碳酸镁晶体。
(1)热解反应的方程式为________________。
(2)碱式碳酸镁可用作化学冷却剂,原因是________________。
(3)为测定白钠镁矾的组成,进行下列实验:
①取白钠镁矾3.340 g溶于水配成100.00 mL溶液A;
②取25.00 mL溶液A,加入足量的氯化钡溶液,得BaSO4 1.165 g;
③另取25.00 mL溶液A,调节pH=10,用浓度为0.1000 mol·L-1的EDTA标准溶液滴定Mg2+(离子方程式为Mg2+ + H2Y2-=MgY2-+ 2H+),滴定至终点,消耗标准溶液25.00 mL。通过计算确定白钠镁矾的化学式(写出计算过程)。___________________
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如下表所示。下列判断正确的是( )

A. 原子半径:丙<丁<戊 B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊 D. 最外层电子数:甲>乙
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关物质用途的说法中,不正确的是
A.Cl2用于自来水消毒B.NaOH用于治疗胃酸过多
C.HClO用于棉、麻和纸张的漂白剂D.Na2O2用作供氧剂
查看答案和解析>>
科目: 来源: 题型:
【题目】某恒温密闭容器发生可逆反应Z(?)+W(?)![]() X(g)+Y(?),t1时刻达到平衡,t2时刻缩小容器体积,t3时刻再次达到平衡后未再改变条件,如图所示。下列说法正确的是
X(g)+Y(?),t1时刻达到平衡,t2时刻缩小容器体积,t3时刻再次达到平衡后未再改变条件,如图所示。下列说法正确的是
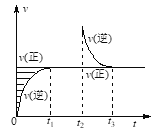
A. Z和W在该条件下至少有一种为气态
B. t1~ t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量不可能相等
C. 若在该温度下此反应平衡常数表达式为K=c(X),则t1~ t2时间段与t3时刻后的X浓度不相等
D. 若该反应只在某温度T以上自发进行,则该反应的平衡常数K随温度升高而增大
查看答案和解析>>
科目: 来源: 题型:
【题目】分类法是一种简单易行、行之有效的科学方法,人们在认识事物时可以采取多种分类方法.下列关于“H2CO3”的分类不正确的是( )
A.二元酸
B.强电解质
C.含氧酸
D.弱酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com