
科目: 来源: 题型:
【题目】离子反应、氧化还原反应都是中学化学中重要的反应类型。请回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有_____________。
A.单质 B.氧化物 C.电解质 D.盐 E.化合物
(2)人们常用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。右图为离子反应、氧化还原反应和置换反应三者之间的关系,则表示离子反应、氧化还原反应、置换反应的字母依次是_____________

(3)将NaBr溶液加入AgC1沉淀中,产生AgBr黄色沉淀。从离子反应发生的条件分析,AgCl与AgBr相比较,溶解度较大的是_____________。
(4)已知某氧化还原反应Au2O3 + 4Na2S2O3 + 2H2O =Au2O+ 2Na2S4O6 +4NaOH
① 用单线桥标出电子转移的方向和数目________________。
② 反应中,被氧化的元素是______________,氧化剂是_________________。
③ 比较该反应中氧化剂和氧化产物的氧化性相对强弱_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对伞花烃(图I)常用作染料、医药、香料的中间体。下列说法错误的是

A. 常温对伞花烃呈液态且难溶于水
B. 图Ⅱ物质的一氯代物有5种结构
C. 对伞花烃最多有9个碳原子共平面
D. 图中氢化反应既是加成反应又是还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】生活中的一些问题常涉及化学知识,下列叙述正确的是
A.棉花的主要成分是纤维素
B.过多食用糖类物质如淀粉等不会致人发胖
C.淀粉在人体内直接水解生成氨基酸,供人体组织的营养需要
D.纤维素在人体消化过程中起重要作用,纤维素可以作为人类的营养物质
查看答案和解析>>
科目: 来源: 题型:
【题目】资料表明:赤热铜能与NO2反应。某小组设计了如下实验装置进行探究,探究固体产物的成分,气体产物是N2还是NO。
已知:酸性KMnO4溶液能氧化NO生成NO3ˉ;
NO和FeSO4溶液反应:NO+FeSO4=[Fe(NO)]SO4(棕色);
Cu2O+2H+=Cu+Cu2++H2O
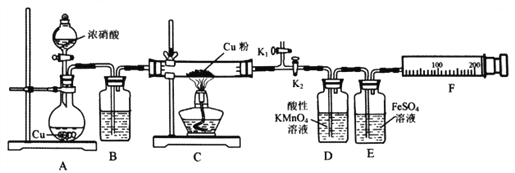
请回答下列问题:
(1)A中反应的化学方程式为________________________。
(2)检查装置气密性,装好药品,然后实验的正确操作顺序是____________
①关闭K1,打开K2 ②打开分液漏斗活塞
③打开K1,关闭K2 ④点燃C处酒精灯
(3)实验过程中,D装置中的现象是____________,能否根据D装置中的现象确认C中有无NO生成? ______,理由是________________________。
(4)E装置的作用是____________。
(5)当铜粉完全反应后,实验小组对反应后的固体成分提出以下猜想:①只有CuO;②只有Cu2O;有同学认为可通过简单的定性实验即可判断猜想①是否成立,其实验方法是_____________________。
(6)实验中E装置自始至终未显棕色,小组最后通过定量实验得到如下数据。
C装置质量 | F装置气体的体积(已折算为标准状况) | ||
玻管质量 | Cu质量 | 反应后(玻管+生成物) | |
mg | 1.92g | (m+2.24)g | 112mL |
据此写出实验时实际发生反应的化学方程式________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2018年大部分地区爆发了流感流感常伴随发热高烧等症状。布洛芬是一种常用的儿童退热药,它的BHC合成法如下
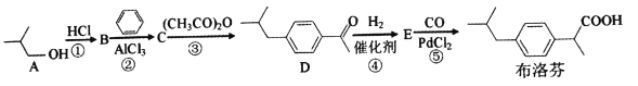
(1)A的名称是__________,B的核磁共振氢谱有__________种吸收峰。
(2)①反应需用浓盐酸而不用稀盐酸,其原因是______________________________。
(3)E的分子式是__________,官能团的名称是__________。
(4)③反应的化学方程式是____________________,反应类型是__________。
(5)满足下列条件的布洛芬的同分异构体有__________种
a遇FeCl3溶液显紫色 b.分子中有5种不同化学环境的氢 c.能发生银镜反应
(6)请写出由苯和( CH3COOCH2CO)2O为原料合成![]() 的线路图(其他试剂任选)___________
的线路图(其他试剂任选)___________
查看答案和解析>>
科目: 来源: 题型:
【题目】下面的排序错误的是( )
A. 晶体熔点由高到低:MgO>H2O>NH3
B. 熔点由高到低:金刚石>生铁>纯铁>钠
C. 硬度由大到小:金刚石>碳化硅>晶体硅
D. 晶格能由大到小:NaF>NaCl>NaBr>NaI
查看答案和解析>>
科目: 来源: 题型:
【题目】温度为T时,向2.0 L恒容密闭容器中充入2.0 mol X,反应X(g) ![]() Y(g)+Z(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
Y(g)+Z(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(Y)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
下列说法不正确的是
A. 反应在前250 s的平均速率为v(Y)=0.000 8 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(Y)=0.21 mol·L-1,则反应的ΔH>0
C. 相同温度下,起始时向容器中充入4.0 mol Y、4.0 mol Z,达到平衡时,则此反应的化学平衡常数为1/20
D. 相同温度下,若起始时向容器中充入2.0 mol X、0.40 mol Y和0.80 mol Z,则达到平衡前v(正)>v(逆)
查看答案和解析>>
科目: 来源: 题型:
【题目】向盛有氯化铁溶液的烧杯中加入过量的铜粉,反应结束后,溶液中大量存在的金属离子是( )
A.Fe2+、Fe3+
B.Fe2+、Cu2+
C.Fe3+、Cu2+
D.Cu+、Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com