
科目: 来源: 题型:
【题目】钛冶炼厂与氯碱厂、甲醇厂组成一个产业链(如图所示),将大大提高资源的利用率,减少环境污染。

请回答下列问题:
(1)Fe位于元素周期表中的位置是__________。
(2)写出流程中电解池里发生反应的离子方程式: __________。
(3)写出流程中“氯化”的化学方程式: __________。
(4)写出TiCl4完全水解生成TiO2·H2O的化学方程式: __________。
(5)高温炉中通入Ar的作用是___________。
(6)上述流程中可循环利用的物质有__________。
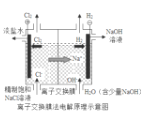
(7)下图为氯碱工业的装置示意图,使用______(填“阴”或“阳”)离子交换膜,目的除了降低分离氢氧化钠的成本外还可以________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关Na2CO3和NaHCO3性质的说法中,正确的是( )
A. 热稳定性:Na2CO3<NaHCO3
B. Na2CO3和NaHCO3均可与澄清石灰水反应
C. 相同温度下,在水中Na2CO3的溶解度小于NaHCO3
D. 106 g Na2CO3和84 g NaHCO3分别与过量盐酸反应,放出CO2的质量:Na2CO3>NaHCO3
查看答案和解析>>
科目: 来源: 题型:
【题目】烟气中主要污染物SO2、NOx,为消除排放,保护环境,实现绿色可持续发展。
处理方法一:烟气经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NO的主要反应的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H1
NO(g)+1/2O2(g)=NO2(g) △H2
SO2(g)+O3(g)![]() SO3(g)+O2(g) △H3
SO3(g)+O2(g) △H3
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_________。
(2) 室温下,进入反应器的NO、SO2的物质的量恒定,改 变通入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):nNO)的变化见图。说明预处理过程中NO2的物质的量变化的原因_______,在反应中SO2的物质的量几乎不发生变化的原因是_______________。

(3)在一定条件下,SO2(g)+O3(g)![]() SO3(g)+O2(g) △H3<0,在一定温度下,向2L某恒容密闭容器中充入4molSO2(g)和1molO3(g),5min时,测得容器中SO3(g)的物质的量为0.5mol。
SO3(g)+O2(g) △H3<0,在一定温度下,向2L某恒容密闭容器中充入4molSO2(g)和1molO3(g),5min时,测得容器中SO3(g)的物质的量为0.5mol。
①0-5min内,用SO2表示的平均反应速率v(SO2)________。
②下列说法中能判断该反应达到平衡状态的是________
a.单位时间内生成nmolSO2同时生成nmolSO3
b.SO3和O2的物质的量浓度之比1:1
C.容器内压强保持不变
d.混合气体的密度不变
e.混合气体的平均相对分子质量不变
处理方法二: 也可采用NaClO2溶液作为吸收剂对烟气进行处理。在不同温度下,NaClO2溶液脱硫(S)、脱硝(N)的反应中,SO2和NO的平衡分压Pe如图所示。

(4) 由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均_______(填“增大”、“不变”或“减小”)。
(5) 反应ClO2-+2SO32-![]() 2SO42-+Cl-的平衡常数K表达式为_______。
2SO42-+Cl-的平衡常数K表达式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.难溶于水的化合物是非电解质
B.某化合物的水溶液可以导电,所以该化合物是电解质
C.硫酸是电解质,所以硫酸在熔化和溶于水时都能导电
D.液态氯化氢不能导电,但氯化氢是电解质
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W、J是元素周期表前四周期中的五种常见元素![]() 其相关信息如下表:
其相关信息如下表:
元素 | 相关信息 |
X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
Y | M层上有2对成对电子 |
Z | Z和Y同周期,Z的电负性大于Y |
W | W的一种核素的质量数为63,中子数为34 |
J | J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐 |
![]() 元素X的一种同位素可测定文物年代,这种同位素的符号是 ______ ;
元素X的一种同位素可测定文物年代,这种同位素的符号是 ______ ;
![]() 元素Y位于元素周期表第 ______ 周期第 ______ 族;
元素Y位于元素周期表第 ______ 周期第 ______ 族;
![]() 元素Z的原子最外层共有 ______ 种不同运动状态的电子;
元素Z的原子最外层共有 ______ 种不同运动状态的电子;
![]() 的基态原子核外价电子排布图是 ______ ;
的基态原子核外价电子排布图是 ______ ;
![]() 的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐的化学式为______________ 。
的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐的化学式为______________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】反应3Fe(s)+4H2O(g)![]() Fe3O4(s)+4H2(g)在一密闭容器中进行,下列条件的改变能使反应速度变快的是①体积不变,增加Fe的量; ②体积不变,增加H2O的量;③体积不变,充入N2使压强增大;④压强不变,充入N2使体积增大
Fe3O4(s)+4H2(g)在一密闭容器中进行,下列条件的改变能使反应速度变快的是①体积不变,增加Fe的量; ②体积不变,增加H2O的量;③体积不变,充入N2使压强增大;④压强不变,充入N2使体积增大
A. ①②③B. ②④C. ②③D. ②
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、实验室常用MnO2与浓盐酸反应制备Cl2(MnO2+4HCl(浓)→MnCl2+Cl2↑+2H2O反应装置如图所示)。
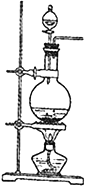
(1)装置图中的主要玻璃仪器有酒精灯、________、__________等。产生的氯气通入水中制得氯水备用。氯水含有的离子除H+、Cl-外还有___________等离子,氯水中因含有__________而具有漂白性。
Ⅱ、某氯化铁样品含有少量FeCl2杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
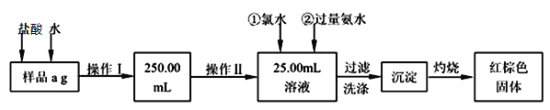
请根据上面流程,回答以下问题:
(2)样品溶解时加盐酸的作用是___________________________________。加入氯水所发生反应的离子方程式___________________________________。
(3)证明Fe3+离子已经沉淀完全的操作是___________________________________。将沉淀物加热灼烧过程中,为使实验结果准确,必须的操作为___________________。
(4)若原样品质量a 为40.00g,加热后红棕色固体质量b为2.200g,则样品中铁元素的质量分数是_________;若称量准确,最终测量的结果偏大,则造成误差的原因可能是_____________(写出一种原因即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在常温常压下,24mLH2S和O2的混合气体点燃后,生成6mLSO2,则原混合气体中H2S的体积可能为
A. 10mLB. 12mLC. 16mLD. 18mL
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研小组模拟“人工树叶”电化学装置如下图所示,该装置能将H2O和CO2转化为糖类(C6H12O6)和O2,X、Y是特殊催化剂型电极,下列说法正确的是
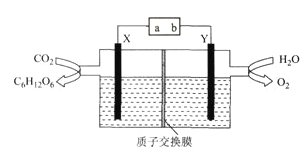
A. 电源a极为正极
B. 该装置中Y电极发生还原反应
C. X电极的电极反应式为6CO2+24H++24e-=C6H12O6+6H2O
D. 理论上,每生成22.4L(标准状况下)O2,必有4mol H+由X极区向Y极区迁移
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com