
科目: 来源: 题型:
【题目】以甲醛和苯酚为主要原料,经如图所示系列转化可合成酚醛树脂和重要有机合成 中间体 D(部分反应条件和产物略去):
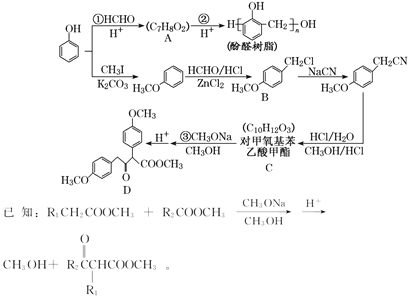
(1)CH3OH 的名称为_____。
(2)C 中所含官能团的名称是_____。
(3)反应②的化学方程式是_____。
(4)下列关于 A 的性质,能反映支链对苯环结构产生影响的是_____(填字母)。
a.能与氢氧化钠溶液反应 b.能使酸性高锰酸钾溶液褪色 c.稀溶液中加浓溴水产生沉淀
(5)E(C8H10O2)与 B 的水解产物互为同分异构体,1 mol E 可与 2 mol NaOH 反应,其核磁共振氢谱显示有 3 种峰且峰面积之比为 3∶1∶1,符合条件的 E 共有_____种。
(6) 完成下面以 CH3OH 和 CH3ONa 为 原 料 ( 其 他 无 机 试 剂 任 选 ) 制 备 化 合 物CH3COCH2COOCH3 的合成路线。 CH3OH――△→… ___________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式碳酸镍[Nix(OH)y(CO3)z·nH2O]是一种绿色粉末,常用作催化剂和陶瓷着色剂,300 ℃以上时分解生成 3 种氧化物。为确定其组成,某同学在实验室进行了有关的探究。 请回答下列问题:
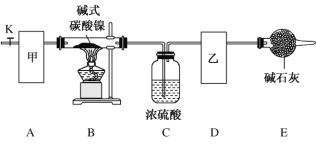
(1)装置 E 中仪器的名称是_____。
(2)甲、乙两装置可分别选取下列装置_____、_____(填字母,装置可重复选取)。

(3) 安装好实验仪器,检查装置气密性;称取一定量的碱式碳酸镍样品,放入硬质玻璃管内; 加热硬质玻璃管,当装置 C 中_____(填实验现象)时,停止加热;打开活塞 K,缓缓通入一段时间空气后,结束实验。
(4)装置 A 的作用是______________________________________________________________________。
(5)实验前后测得下表所示数据:
装置 B 中样品质量/g | 装置 C 质量/g | 装置 D 质量/g | |
实验前 | 3.77 | 132.00 | 41.00 |
实验后 | 2.25 | 133.08 | 41.44 |
已知碱式碳酸镍中 Ni 化合价为+2 价,则该碱式碳酸镍的化学式为_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】质量为ag的铜丝,在空气中灼热变黑,趁热放入下列物质中,铜丝不变红,质量大于a g的是( )
A. 盐酸B. CH3COOHC. C2H5OHD. NaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】已知X、Y、Z、W四种元素是短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W是该元素所在周期原子半径最大的元素,W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键,该分子中含有10个电子。Z原子最外层电子数是次外层电子数的3倍,试判断:
(1)X、Z两种元素的元素符号为X________,Z________。
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物的电子式为________________。
(3)①由X、Y、Z所形成的常见离子化合物是__________________(写化学式)。
②该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为_______。
③化合物WY3的晶体结构中含有的化学键为________(选填序号)。
A.只含离子键 B.只含共价键 C.既含离子键又含共价键
④X与W形成的化合物与水反应生成X2,其中水作________(填“氧化剂”或“还原剂”)。
(4)用电子式表示化合物W2Z的形成过程:______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于化学反应的理论是一个经过简化的概念模型,合理简化的概念模型是研究化学反应原理的基础。反应速率的碰撞理论提出:能引发化学反应的碰撞称为有效碰撞。
(1)图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(填“a”“b”或“c”)。
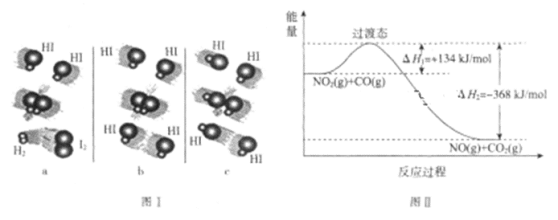
(2)过渡态理论是在碰撞理论的基础上提出的:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。根据图Ⅱ写出相应的热化学方程式:_____________________________________________ 。
(3)过渡态理论认为,催化剂改变反应速率的原因是改变了活化能从而改变了反应的途径。请在图Ⅱ中画出该反应在其他条件不变,仅使用催化剂而使反应速率加快的能量变化示意图。________
查看答案和解析>>
科目: 来源: 题型:
【题目】从石油和煤中提炼出化工原料A和B,A是一种果实催熟剂,它的产量用来衡量一个国家的石油化工发展水平。B是一种比水轻的油状液体,B仅由碳氢两种元素组成,碳元素与氢元素的质量比为12:1,B的相对分子质量为78。回答下列问题:
(1)A的结构简式_______________,B的结构简式_________________;
(2)与A相邻的同系物C使溴的四氯化碳溶液褪色的化学反应方程式:_____________;反应类型:___________。
(3)B与浓硫酸和浓硝酸在50~60℃反应的化学反应方程式: ______________________ 反应类型:___________。
(4)等质量的A、B完全燃烧时消耗O2的物质的量________(填A>B、A<B或A=B”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质在水溶液中的电离方程式书写错误的是( )
A.CaCl2===Ca2++2Cl-B.NaHSO4===Na++H++SO42-
C.HNO3===H++NO3-D.KClO3===K++Cl++3O2-
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨对工、农业生产和国防都有重要意义。 已知:N2(g)+3 H2(g)2NH3(g) △H= -92.4kJ/mol,请回答:
(1)合成氨工业中采取的下列措施可以用平衡移动原理解释的是________(填字母)。
a. 用铁触媒加快化学反应速率
b. 采用较高压强(20MPa~50MPa)
c. 采用较高温度(500℃左右)
d. 将生成的氨液化并及时从体系中分离出来
(2)一定温度下,在密闭容器中充入1mol N2和3mol H2并发生反应。
①若容器容积恒定,达到平衡时,N2的转化率α1 =25%,此时,反应放热______kJ,容器内气体压强与开始时气体压强之比是________。
②若容器压强恒定,则达到平衡时,容器中N2的转化率α2______α1(填“>”“<”或“=”)。
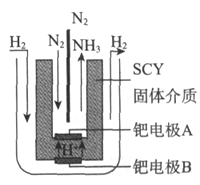
(3)随着对合成氨研究的发展,希腊科学家采用高质子导电性的SCY陶瓷(能传递![]() )为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。钯电极A为_________极(填“阴”或“阳”),该极上的电极反应式是_______。
)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。钯电极A为_________极(填“阴”或“阳”),该极上的电极反应式是_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于化学反应与能量的说法正确的是( )
A.古文说“冰,水为之,而寒于水”说明等量的水和冰相比,冰的能量更高
B.化学反应遵循质量守恒定律的同时,也遵循能量守恒定律
C.已知C(石量,s)=C(金刚石,s) H>0,则金刚石比石墨稳定
D.任何化学反应都伴随着能量变化,其表现形式只有吸热和放热两种
查看答案和解析>>
科目: 来源: 题型:
【题目】现有甲、乙两个化学小组利用两套相同装置,通过测定产生相同体积气体所用时 间长短来探究影响 H2O2 分解速率的因素(仅一个条件改变)。甲小组有如下实验设计方 案。
实验编号 | 温度 | 催化剂 | 浓度 |
甲组实验Ⅰ | 25 ℃ | 三氧化二铁 | 10 mL 5% H2O2 |
甲组实验Ⅱ | 25 ℃ | 二氧化锰 | 10 mL 5% H2O2 |
甲、乙两小组得出如下图数据。

(1)甲小组实验得出的结论是_____。
(2) 由乙组研究的酸、碱对 H2O2 分解影响因素的数据分析,相同条件下 H2O2 在______(填“酸”或“碱”)性环境下放出气体速率较快;由此,乙组提出可以用BaO2 固体与硫酸溶液反应制 H2O2,其反应的离子方程式为___________________________;支持这一方案的理由是_____。
(3)已知过氧化氢是一种极弱的二元酸:H2O2![]() H++HO2- (Ka1=2.4×10-12)。当稀 H2O2溶液在碱性环境下分解时会发生反应 H2O2+OH-
H++HO2- (Ka1=2.4×10-12)。当稀 H2O2溶液在碱性环境下分解时会发生反应 H2O2+OH-![]() HO2-+H2O,该反应中,正反应速率为 v 正=k正·c(H2O2)·c(OH-),逆反应速率为 v 逆=k 逆·c(H2O)·c(HO2- ),其中 k 正、k 逆为速率常数,则 k 正与 k 逆的比值为_________________________________________(保留 3 位有效数字)。
HO2-+H2O,该反应中,正反应速率为 v 正=k正·c(H2O2)·c(OH-),逆反应速率为 v 逆=k 逆·c(H2O)·c(HO2- ),其中 k 正、k 逆为速率常数,则 k 正与 k 逆的比值为_________________________________________(保留 3 位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com