
科目: 来源: 题型:
【题目】中国科学家用蘸墨汁书写后的纸张作为空气电极,设计并组装了轻型、柔性、能折叠的可充电锂空气电池如下左图,电池的工作原理如下右图。下列有关说法正确的是
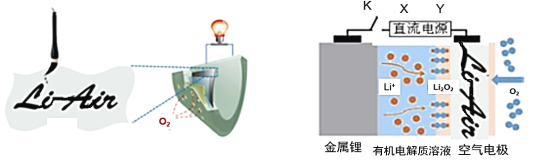
A. 放电时,纸张中的纤维素作为锂电池的负极
B. 充电时,若阳极放出1 mol O2,则有4 mol e-回到电源正极
C. 开关K闭合给锂电池充电,X为直流电源负极
D. 放电时,Li+由正极经过有机电解质溶液移向负极
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是重要的工业原料。煤化工可以利用煤炭制取水煤气从而合成甲醇:
CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
已知①常压下反应的能量变化如图所示。

②
化学键 | H—H | H—O | O=O |
键能kJ/mol | 436 | x | 496 |
③CO(g)+1/2O2(g)=CO2(g)ΔH=-280 kJ/mol;
H2(g)+1/2O2(g)=H2O(l) ΔH=-284 kJ/mol
H2O(l)=H2O(g) ΔH=+44 kJ/mol
请回答下列问题:
(1)请写出表示气态甲醇燃烧热的热化学方程式_______________________。
(2)H—O键的键能x为________ kJ/mol。
(3)在____(填“高温”或“低温”)情况下有利于CO和H2制备甲醇的反应自发进行。
(4)某兴趣小组同学利用甲醇燃料电池探究电浮选法处理污水的一种方式:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3具有吸附性,可吸附污物而沉积下来,具有净化水的作用。装置如图所示。

甲 乙
①写出甲池的A极电极反应式:__________________________。
②若乙池实验时污水中离子浓度较小,导电能力较差,净水效果不好,此时应向污水中加入适量的________。
A.H2SO4 B.BaSO4 C.Na2SO4 D.NaOH E.CH3CH2OH
(5)下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
①乙中A极析出的气体在标准状况下的体积为____。
②丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则图中②线表示的是__________离子的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要__________mL 5.0 mol/L NaOH溶液。

查看答案和解析>>
科目: 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。
(1)利用下图装置电解制备NaOH,两电极区电解液分别为NaOH和NaCl溶液。
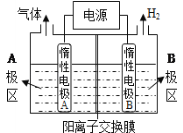
①B极区电解液为__________溶液(填化学式),A极要连接电源的________(填“正”或“负”)极。
②阳极电极反应式为______________________________________,电解过程中Na+向____________电极迁移(填“A”或“B”)。
③电解总反应的离子方程式是_____________________________________________。
(2)利用下图装置,可以模拟铁的电化学防护。
①若X为碳电极,为减缓铁的腐蚀,开关K应置于________处。(填“A”、“B”或“C”)
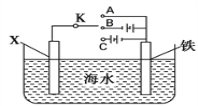
②若X为锌电极,开关K置于A处,该电化学防护法称为______________________。
(3)钒电池是以溶解于一定浓度硫酸溶液中的不同价态的钒离子(V2+、V3+、VO2+、VO2+)为正极和负极电极反应的活性物质,电池总反应为VO2++V3++H2O![]() V2++VO2++2H+。放电时的正极反应式为___________________________充电时的阴极反应式为______________________________。放电过程中,电解液的pH________(选填“升高”“降低”或“不变”)。
V2++VO2++2H+。放电时的正极反应式为___________________________充电时的阴极反应式为______________________________。放电过程中,电解液的pH________(选填“升高”“降低”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质都是由分子构成,且都是共价化合物的一组是( )
A. 干冰、蔗糖水、液氧 B. 硫酸、液氨、酒精
C. 浓硫酸、氮气、葡萄糖 D. C60、 酒精、碳酸氢铵
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素A、B、C、D的原子序数依次增大。甲、乙、丙、丁、戊是这四种元素组成的常见化合物,己是元素C 的单质。已知甲、乙的焰色均为黄色且水溶液均呈碱性,它们之间的转化关系如图所示。下列说法不正确的是

A. 甲和乙加入水中都能促进水的电离平衡
B. 乙和戊都是离子化合物
C. 离子半径:C>D>A
D. A、B、C形成化合物的水溶液一定呈酸性
查看答案和解析>>
科目: 来源: 题型:
【题目】二羟基甲戊酸是合成青蒿素的原料之一,其结构如图a所示。下列有关二羟基甲戊酸的说法正确的是

A. 含有羟基和酯基两种官能团
B. 不能使酸性KMnO4溶液褪色
C. 等量的二羟基甲戊酸消耗Na和NaHCO3的物质的量之比为3:1
D. 是乳酸(结构如图b)的同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列判断正确的是
A. 标准状况下,2.8 g 14C18O中质子数为1.4NA
B. 常温下,0.3 mol NO2通入水中完全反应,转移的电子数为0.2NA
C. CO燃烧热为283.0 kJ/mol,若一定量的CO完全燃烧放出热量为283.0 kJ,则消耗O2分子数为NA
D. 62.0 g乙二醇中含有的羟基数目为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】用惰性电极电解一定量的硫酸铜溶液,实验装置如图①。电解过程中的实验数据如图②,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。则下列说法正确的是( )

A.电解过程中,b电极表面先有红色物质析出,后有气泡产生
B.a电极上发生的反应方程式为:2H+ +2e- = H2↑和 4OH--4e- = 2H2O + O2↑
C.从P到Q点时收集到的混合气体的平均摩尔质量为12g·mol-1
D.曲线0~P段表示H2和O2混合气体的体积变化,曲线P~Q段表示O2的体积变化
查看答案和解析>>
科目: 来源: 题型:
【题目】工业采用氯化铵焙烧菱锰矿制备高纯碳酸锰。已知:菱锰矿的主要成分是MnCO3,其中含Fe、Ca、Mg、Al等元素。焙烧后的产物用浓盐酸酸浸,再对浸出液净化除杂,得到的净化液加入碳酸氢铵溶液生成沉淀,洗涤干燥后即可得到产品。回答:
(1)焙烧过程中产生两种气体,一种可使湿润的蓝色石蕊试纸变红,另一种可使湿润的红色石蕊试纸变蓝。请写出焙烧过程中主要反应的方程式______________。
(2)对浸出液净化除杂时,需先加入MnO2将Fe2+转化为Fe3+,写出该反应的离子方程式______________________。检验Fe3+所用试剂的名称是__________。
(3)净化液加入碳酸氢铵溶液时反应的离子方程式为_____________________。
(4)上述生产过程中可循环使用的物质是________。
A.MnCO3 B. HCl C. NH4Cl D. 碳酸氢铵
(5)用滴定法测定浸出液中Mn2+的含量时,需向其中加入稍过量的磷酸和硝酸,加热会生成NO2-。加入稍过量的硫酸铵可以将其转化成无污染的物质而除去,该反应的离子方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com