
科目: 来源: 题型:
【题目】绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得到各种铁的氧化物和硫的氧化物。已知SO3是一种无色 晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性强于浓硫酸,能漂白某些有机染料,如品红等。回答下列问题:

(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置C的作用是_______________。装置B中可观察到的现象是__________________________,甲组同学由此得出绿矾的分解产物中含有SO2。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中_____(填字母)。
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解所得气态产物的装置:

丙组同学的实验装置中,依次连接的合理顺序为A→_________________→H。能证明绿矾分解产物中有O2的检验方法是________________________。
(4)为证明绿矾分解产物中含有三价铁的操作及现象__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知乙烯能发生以下转化:

(1)乙烯的结构简式为:___________________________
(2)写出B、D化合物中官能团(写化学式):
B中含官能团________________;D中含官能团_____________;
(3)写出反应的化学方程式
①:___________________________________________反应类型:___________________
②:___________________________________________ 反应类型:____________________
③:___________________________________________ 反应类型:________________
查看答案和解析>>
科目: 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是( )

A. 分子式为C7H6O5
B. 分子中含有2种官能团
C. 可发生加成和取代反应
D. 在水溶液中羧基和羟基均能电离出H+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列装置或操作能达到目的的是
|
|
|
|
A. 只用装置①的仪器可以测定生成氢气的速率(mL/s)
B. 装置②可依据单位时间内颜色变化来比较浓度对反应速率的影响
C. 装置③进行中和反应反应热的测定实验
D. 装置④依据出现浑浊的快慢比较温度对反应速率的影响
查看答案和解析>>
科目: 来源: 题型:
【题目】LiOH常用于制备锂离子电池正极材料。工业上常利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。下列说法正确的是

A. a是电源的负极
B. A电极的电极反应式为4OH--4e-===2H2O+O2↑
C. B极区电解液为LiOH溶液
D. 外电路中每通过0.1 mol电子,生成1.12 L氢气
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质,按氧化物、混合物、单质、电解质顺序排列的是 ( )
A.二氧化硫、碘酒、液态臭氧、烧碱B.硫酸钾、纯碱、白磷、生石灰
C.氧化铜、氯化氢、钠、干冰D.氧化钙、胆矾、氮气、空气
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.控制变量法是化学实验的一种常用方法。下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m5 |
6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
(1)化学反应速率本质上是由物质的性质决定的,但外界条件也会影响反应速率的大小。本实验中实验2和实验3对比得出的结论是______________________________。
(2)我们最好选取实验________(填3个实验序号)研究锌的形状对反应速率的影响。
(3)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快。原因是______________________________。
(4)利用表中数据,可以求得:硫酸的物质的量浓度是________mol/L。
Ⅱ.某温度时,在5 L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:
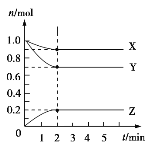
(5)反应开始至2 min,Y的平均反应速率______________________。
(6)分析有关数据,写出X、Y、Z的反应方程式_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表中是各组反应的反应物和反应温度,反应刚开始时,放出H2速率最快的是( )
编号 | 金属(粉末状) | 物质的量(mol) | 酸的浓度及体积 | 反应温度(℃) |
A | Al | 0.1 | 2mol.L-1盐酸10mL | 60 |
B | Fe | 0.1 | 1mol.L-1盐酸10mL | 50 |
C | Mg | 0.1 | 1mol.L-1盐酸10mL | 60 |
D | Mg | 0.1 | 1mol.L-1硫酸10mL | 60 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com