
科目: 来源: 题型:
【题目】下列说法正确的是

A. 用上图所示方法可保护钢闸门不被腐蚀
B. SiO2(s)+2C(s)=Si(s)+2CO(g)在常温下不能自发进行,则该反应的△H>0
C. 常温下,NH4Cl溶液加水稀释,![]() 增大
增大
D. C(s)+H2O(g)![]() CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动
CO(g)+H2(g)(△H>0),其它条件不变时,升高温度,正反应速率增大、逆反应速率减小,平衡正向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】赤泥是铝土矿提取氧化铝过程中产生的固体废弃物,其主要成分为Fe2O3、Al2O3、CaO、TiO2、SiO2等,属于强碱性废渣。从赤泥中回收钛的工艺流程如下:
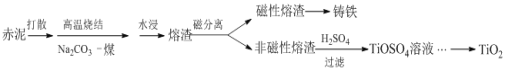
请回答以下问题:
(1)赤泥颗粒孔隙大,具有较大的比表面积,可作为废气SO2的吸收剂,研究表明该过程中主要利用了化学中和反应,其次是______。
(2)赤泥加一定量水打散的目的是______。
(3)已知高温烧结时,TiO2发生的反应是Na2CO3+TiO2 ![]() Na2TiO3+CO2↑,且Na2TiO3不溶于水。则Al2O3在烧结中发生的反应是______,水浸液里的主要溶质有______。
Na2TiO3+CO2↑,且Na2TiO3不溶于水。则Al2O3在烧结中发生的反应是______,水浸液里的主要溶质有______。
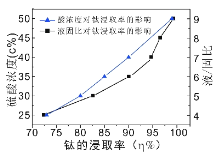
(4)酸浸时,若使钛的浸出率(η%)达到90%,则根据右图工业上应采取的适宜条件是:酸浓度和液固比的取值分别约为______、______。同时浸出温度过高可能造成的环境污染是__________。
(5)TiO2在一定条件下可转化为TiCl4而获得精制提纯,控制TiCl4水解的条件还可以制得TiO2·xH2O纳米材料,该水解过程的化学方程式是______。
(6)赤泥中含钛(以TiO2的质量分数表示)一般为4% ~12%,假设在上述工艺中钛的总回收率为75%,则1t赤泥获得TiO2的最大质量为______kg。
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家发现,普通盐水在无线电波的照射下可以降低盐水中所含元素之间的结合力,释放出氢原子,点火时氢原子会在该频率下持续燃烧。上述“结合力”的实质是( )
A.离子键B.共价键C.金属键D.分子间作用力
查看答案和解析>>
科目: 来源: 题型:
【题目】臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性.实验室可将氧气通过高压放电管来制取臭氧:3O2 ![]() 2O3 。
2O3 。
(1)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为________L。
(2)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g.则原混合气中臭氧的体积分数为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.2 L由NaCl溶液、MgCl2溶液、CuCl2溶液组成的混合溶液中,部分离子的浓度如图所示。
(1)混合液中,NaCl的物质的量为_______mol,MgCl2的质量为_______g。
(2)该混合溶液中CuCl2的物质的量浓度为_____molL﹣1,将该混合溶液加水稀释至体积为1 L,稀释后溶液中Cu2+的物质的量浓度为_______molL﹣1。

查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下发生反应:I2(g)+H2(g) ![]() 2HI(g); △H<0并达平衡。HI的体积分数随时间变化如下图曲线(II)所示,若改变反应条件,在甲条件下HI的体积分数的变化如曲线(I)所示。在乙条件下HI的体积分数的变化如曲线(III)所示。则甲条件、乙条件分别是
2HI(g); △H<0并达平衡。HI的体积分数随时间变化如下图曲线(II)所示,若改变反应条件,在甲条件下HI的体积分数的变化如曲线(I)所示。在乙条件下HI的体积分数的变化如曲线(III)所示。则甲条件、乙条件分别是

①恒容条件下,升高温度 ②恒容条件下,降低温度 ③恒温条件下,缩小反应容器体积 ④恒温条件下,扩大反应容器体积 ⑤恒温恒容条件下,加入适当的催化剂
A. ①⑤, ③ B. ②⑤, ④ C. ③⑤, ② D. ③⑤, ④
查看答案和解析>>
科目: 来源: 题型:
【题目】结合图回答问题:
(1)学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容如图Ⅰ,现欲用此硫酸配制配制成浓度为0.50molL﹣1的稀硫酸100mL.①所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外还需________。
②所取浓硫酸的体积为________ mL。
(2)写出上述装置中仪器的名称:②________;③________。
(3)若利用装置Ⅱ分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有________,将仪器补充完整后进行的实验操作的名称为________。
(4)实验室常用装置Ⅲ分离碘水中的碘, 进行该操作时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:________(填序号)。①常温下为液态 ②I2在其中溶解程度大 ③与水互不相容 ④密度要比水大。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol.若阿伏加德罗常数的值用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为________个。
(3)该气体在标准状况下的体积为________L。
(4)该气体溶于水形成VL溶液,其溶液的物质的量浓度为________mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知2NaHCO3![]() Na2CO3 + H2O+CO2 ,现把14.8g Na2CO310H2O和NaHCO3组成的固体混合物溶于水配成100mL溶液,其中c(Na+)=1.2molL﹣1,若把等质量的固体混合物加热至恒重,残留固体质量是( )
Na2CO3 + H2O+CO2 ,现把14.8g Na2CO310H2O和NaHCO3组成的固体混合物溶于水配成100mL溶液,其中c(Na+)=1.2molL﹣1,若把等质量的固体混合物加热至恒重,残留固体质量是( )
A. 6.36gB. 3.18gC. 4.22gD. 5.28g
查看答案和解析>>
科目: 来源: 题型:
【题目】在2A+3B===2C+D的反应中,表示反应速率最快的是( )
A. v(A)=0.5 mol·L-1·min-1B. v(B)=0.6 mol·L-1·min-1
C. v(C)=0.35 mol·L-1·min-1D. v(D)=0.4 mol·L-1·min-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com