
科目: 来源: 题型:
【题目】在一定条件下,在容积不变的密闭容器内进行反应:2NO+2CO![]() N2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是
N2+2CO2 △H<0.曲线a表示NO的转化率与反应时间的关系,若改变初始条件,使反应过程按照曲线b进行,可采取的措施是

A. 加催化剂 B. 降低温度
C. 增大NO的浓度 D. 缩小容器体积
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)0.4 mol某气体的体积为9.8L,则该气体的摩尔体积为_____。
(2)标准状况下,测得1.92克某气体的体积为672mL,则此气体的相对分子质量为___。
(3)实验室用Na2CO3·10H2O晶体配制0. 5mol/L的Na2CO3溶液970mL,应称取Na2CO3·10H2O的质量是____。
(4)某学生欲用12mol·L-1浓盐酸和蒸馏水配制500 mL 0.3 mol·L-1的稀盐酸。
①该学生需要量取____mL上述浓盐酸进行配制。
②下列实验操作会导致所配制的稀盐酸的物质的量浓度偏小的是____(填序号)。
a.用量筒量取浓盐酸时俯视观察凹液面
b.将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中
c.稀释浓盐酸时,未冷却到室温即转移到容量瓶中
d. 定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
e.容量瓶洗涤干净后未干燥
查看答案和解析>>
科目: 来源: 题型:
【题目】对于在一个密闭容器中进行的反应C(s)+H2O(g) ![]() CO(g)+H2(g) ,下列条件的改变对反应速率几乎没有影响的是
CO(g)+H2(g) ,下列条件的改变对反应速率几乎没有影响的是
①增加C的量; ②增加CO的量;
③将容器的体积缩小一半; ④保持体积不变,充入N2以增大压强;
⑤升高反应体系的温度; ⑥保持压强不变,充入N2以增大体积。
A. ②③ B. ①④ C. ①⑥ D. ④⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】下列条件一定能使反应速率加快的是
①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积
④加入生成物 ⑤加入MnO2
A. 全部 B. ①②⑤ C. ② D. ②③
查看答案和解析>>
科目: 来源: 题型:
【题目】为除去粗盐中的CaCl2、MgCl2、硫酸盐以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
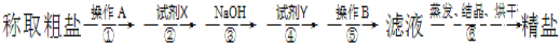
(1)第①步中,操作A是__________,第⑤步中,操作B是__________。
(2)判断试剂X过量的方法是________________________。
(3)写出第④步中涉及反应的化学方程式____________________。
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、__________(填化学式)。
(5)此实验方案尚需完善,具体步骤是__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】计算填空:
(1)4.5 g水与____ g 硫酸所含的分子数相等,它们所含氧原子数之比是____,氢原子数之比是____。
(2)已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量的D,现将16 g A与70 g B的混合物充分反应后,生成2 mol D和一定量的C,则D的摩尔质量是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列十种物质:①O2 ②铝 ③Na2O ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨盐酸 ⑩CaCO3
(1)按物质的树状分类法填写表格的空白处:
_________ | 氧化物 | _________ | _________ | 电解质 | |
属于该类的物质 | ② | _________ | ⑧ ⑨ | ⑦ | _________ |
(2)写出实验室制备①的化学方程式:____________________。
(3)上述十种物质中,有两种物质之间可发生H++OH-=H2O,该离子反应对应的化学方程式为_________________。
(4)写出制备⑦的化学方程式:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知钠、氯及其化合物间有如下转化关系,
请按要求填空:

(1)实验室中金属钠通常保存在_______中,一小块金属钠投入水中反应的化学方程式是________________。
(2)Na2O2常用于呼吸面具中,有关反应的化学方程式为_____________________________,_________________________________。
(3)新制的氯水滴入紫色石蕊试液中,观察到的现象是___________________________。
请写出氯气与水反应的化学方程式_______________________________。
(4)工业上用氯气和石灰乳反应制漂白粉,其化学方程式为_____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知反应 2HI(g)![]() H2(g)+I2(g)的 ΔH=+11kJ/mol, 1mol H2(g)、 1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为_________kJ。
H2(g)+I2(g)的 ΔH=+11kJ/mol, 1mol H2(g)、 1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为_________kJ。
(2)Bodensteins 研究了下列反应:2HI(g) ![]() H2(g)+I2(g)在 716 K 时,气体混合物中碘化氢的物质的量分数 x(HI)与反应时间 t 的关系如下表:
H2(g)+I2(g)在 716 K 时,气体混合物中碘化氢的物质的量分数 x(HI)与反应时间 t 的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为__________。
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为__________(以K和k正表示)。若 k正=0.0027 min-1,在 t=40min 时,v正=_________ min-1。
③由上述实验数据计算得到v正~x(HI)和 v逆~x(H2)的关系如图所示。当升高到某一温度时,反应重新达到平衡,相应的点依次为__________(填字母)和__________(填字母)。

查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,同温度下涉及如下反应:
①2NO(g)+Cl2(g)2ClNO(g) 平衡常数为K1;
②2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g) 平衡常数为K2。
(1)4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=____(用K1、K2表示)。
(2)若反应①在温度T下达到平衡时,平衡常数为K1,升高温度后K1增大,则正反应的焓变△H____0(填“>”、“<”或“=”)。若平衡后在其他条件不变的情况下,充入少量Cl2,Cl2的转化率___________(填“变大”、“变小”或“不变”,下同),![]() 的值___________。
的值___________。
Ⅱ.近年,科学家研究了乙醇催化合成乙酸乙酯的新方法:2C2H5OH(g)![]() CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是________。
CH3COOC2H5(g)+2H2(g)在常压下反应,冷凝收集,测得常温下液态收集物中主要产物的质量分数如图3所示。关于该方法,下列推测合理的是________。

A.反应温度不宜超过300℃
B.增大体系压强,有利于提高乙醇平衡转化率
C.在催化剂作用下,乙醛是反应历程中的中间产物
D.提高催化剂的活性和选择性,减少乙醚、乙烯等副产物是工艺的关键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com