
科目: 来源: 题型:
【题目】Q、X、Y、Z是原子序数依次增大的短周期主族元素,Q原子的最外层电子数是内层电子数的2倍,X、Y、Z在周期表中的位置关系如图所示。下列说法正确的是

A. Q和Z可能形成化合物QZ2
B. Y的最高价氧化物的水化物一定是强酸
C. X、Z和氢三种元素不可能组成离子化合物
D. 最简单气态氢化物的沸点:Q>X
查看答案和解析>>
科目: 来源: 题型:
【题目】某含铜化合物的化学式为Cux(OH)y(CO3)z(Cu为+2价)。取该样品22.2 g,充分加热后,得到黑色固体氧化铜16.0 g,则该物质的化学式为
A.Cu2(OH)4CO3B.Cu3(OH)4CO3
C.Cu2(OH)2CO3D.Cu4(OH)2(CO3)3
查看答案和解析>>
科目: 来源: 题型:
【题目】用石墨烯锂硫电池电解制备Fe(OH)2的装置如图所示。电池放电时的反应为16Li+xS8==8Li2Sx(2≤x≤8),电解池两极材料分别为Fe和石墨,工作一段时间后,右侧玻璃管中产生大量的白色沉淀。下列说法不正确的是
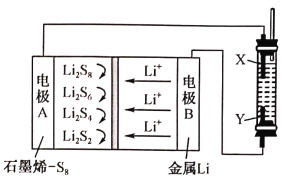
A. X是铁电极,发生氧化反应
B. 电子流动的方向:B→Y,X→A
C. 正极可发生反应:2Li2S6+2Li++2e-=3Li2S4
D. 锂电极减重0.14g时,电解池中溶液减重0.18g
查看答案和解析>>
科目: 来源: 题型:
【题目】阿司匹林( )是常用的解热镇痛药,下列说法不正确的是( )
)是常用的解热镇痛药,下列说法不正确的是( )
A. 分子中含有两种含氧官能团
B. 阿司匹林与 互为同分异构体
互为同分异构体
C. 阿司匹林可以发生取代反应、加成反应、酯化反应
D. 1 mol阿司匹林可以与5mol H2发生加成反应,也可与1 mol碳酸氢钠反应
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,下列说法不正确的是( )


A.反应过程(1)的热化学方程式为A2(g)+B2(g)C(g)ΔH1=-Q1 kJ/mol
B.反应过程(2)的热化学方程式为C(g)A2(g)+B2(g)ΔH2=+Q2 kJ/mol
C.Q1与Q2的关系:Q1>Q2
D.ΔH2>ΔH1
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 1LpH=5的醋酸溶液中含有的H+数目小于10-5NA
B. 9.2g14CO2与N218O的混合物中所含中子数为4.8NA
C. 硝酸与铜反应生成0.1 mol NOx时,转移电子数为0.2NA
D. 1 molSO2和0.5molO2充分反应,生成SO3的分子数为NA
查看答案和解析>>
科目: 来源: 题型:
【题目】【题目】已知:①H2(g)+ ![]() O2(g)=2H2O(g) △H1=akJ/mol
O2(g)=2H2O(g) △H1=akJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=b kJ/mol
③H2(g)+ ![]() O2(g)=H2O(l) △H3=ckJ/mol;
O2(g)=H2O(l) △H3=ckJ/mol;
④2H2(g)+O2(g)=2H2O(l) △H4=dkJ/mol。
下列关系正确的是
A. a<c<0 B. b>d>0 C. 2a=b<0 D. 2c=d>0
查看答案和解析>>
科目: 来源: 题型:
【题目】I.钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成淡黄色的__________ (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种___________(填“酸性”、“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的化学方程式:_____________。
II.氮、硫的化合物与人类生活和生产有着密切的联系。请回答下列问题:
(1)在空气质量报告的各项指标中,有SO2和NO2的指数,SO2是一种无色有毒气体,NO2是一种_________(填“无色”或“红棕色”)有毒气体;
(2)氨气极易溶于水,其水溶液显__________(填“酸”、“碱”或“中”)性;
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________(填“吸水”、“脱水”或“氧化”)性。
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________(填“吸水”、“脱水”或“氧化”)性。
III.乙醇和乙酸是生活中两种常见的有机物。请回答下列问题:
(1)乙醇的结构简式为CH3CH2OH,乙醇分子含有的官能团为__________;
(2)生活中常用食醋除去暖瓶内的水垢(主要成分是CaCO3),反应的化学方程式为2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O。通过这个事实,你得出醋酸与碳酸的酸性强弱关系是:醋酸_____碳酸(填“>”或“<”);
(3)在浓硫酸的催化作用下,加热乙酸和乙醇的混合溶液,可发生酯化反应。请完成化学方程式:CH3COOH + CH3CH2OH![]() CH3COOCH2CH3+________。
CH3COOCH2CH3+________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钼酸钠晶体(Na2MoO4·2H2O)可抑制金属腐蚀。以钼精矿(主要成分为MoS2,含少量杂质)为原料,制备钼酸钠晶体的主要流程图如下图。

回答下列问题
(1)完成下列反应:_____MoS2+ _____O2![]() _____SO2+ _____MoO3
_____SO2+ _____MoO3
在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是_____________。
(2)浓氨水浸取粗产品获得(NH4)2MoO4溶液,其化学反应方程式为___________;该反应说明MoO3______(填“有”或“没有”)酸性氧化物的性质。
(3)常温下,沉钼阶段所得废液为(NH4)2SO4稀溶液。若(NH4)2SO4稀溶液的pH=a,则![]() =_______(用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,
=_______(用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,![]() 将_________(填“变大”“不变”或“变小”)。
将_________(填“变大”“不变”或“变小”)。
(4)操作X为_________________ ,已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,则在操作X中应控制温度的最佳范围为________________。
温度(℃) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 | >100 |
析出物质 | Na2MoO4·10H2O | Na2MoO4·2H2O | Na2MoO4 | ||||||
溶解度 | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 |
| |
结晶得到的母液可以在下次结晶时重复使用,但达到一定次数后必须净化处理,原因是___。
(5)Li、MoS2 可充电电池的工作原理为![]() [Lix(MOS2)n附着在电极上],则电池充电时阳极的电极反应式为_________________________ 。
[Lix(MOS2)n附着在电极上],则电池充电时阳极的电极反应式为_________________________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com