
科目: 来源: 题型:
【题目】下列说法正确的是
A. 0.1molFe溶于硝酸,电子转移数目一定为0.3![]()
B. 标准状况下,14.4g正戊烷(![]() )中含C-C键数目为0.8N
)中含C-C键数目为0.8N
C. 18g重水(![]() )中含中子数目为10
)中含中子数目为10![]()
D. 12g熔融![]() 中含离子总数目为0.3
中含离子总数目为0.3![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】一种合成囧烷(E)的路线如下:

⑴ A中所含官能团的名称是_______________;E的分子式为_________。
⑵ A→B、B→C的反应类型分别是___________、___________。
⑶ 在一定条件下,B与足量乙酸可发生酯化反应,其化学方程式为______________。
⑷ F是一种芳香族化合物,能同时满足下列条件的F的同分异构体有_____种。
① 1个F分子比1个C分子少两个氢原子
② 苯环上有3个取代基
③ 1molF能与2molNaOH反应
写出其中核磁共振氢谱图有5组峰,且面积比为3∶2∶2∶2∶1的一种物质的结构简式:__________。
⑸ 1,2-环己二醇(  )是一种重要的有机合成原料,请参照题中的合成路线,以
)是一种重要的有机合成原料,请参照题中的合成路线,以 和
和![]() 为主要原料,设计合成1,2-环己二醇的合成路线。______________
为主要原料,设计合成1,2-环己二醇的合成路线。______________
查看答案和解析>>
科目: 来源: 题型:
【题目】铜及其化合物在人们的日常生活中有着广泛的用途。回答下列问题:
⑴ 铜或铜盐的焰色反应为绿色,该光谱是________(填“吸收光谱”或“发射光谱”)。
⑵ 基态Cu原子中,核外电子占据的最低能层符号是________,其价电子层的电子排布式为___________,Cu与Ag均属于IB族,熔点:Cu________Ag(填“>”或“<”)。
⑶ [Cu(NH3)4]SO4 中阴离子的立体构型是_______;中心原子的轨道杂化类型为_____,[Cu(NH3)4]SO4 中Cu2+与NH3之间形成的化学键称为_______________。
⑷ 用Cu作催化剂可以氧化乙醇生成乙醛,乙醛再被氧化成乙酸,等物质的量的乙醛与乙酸中σ键的数目比为_____________。
⑸氯、铜两种元素的电负性如表:
元素 | Cl | Cu |
电负性 | 3.2 | 1.9 |
CuCl属于________(填“共价”或“离子”)化合物。

⑹Cu 与Cl 形成某种化合物的晶胞如图所示,该晶体的密度为ρ g·cm-3,晶胞边长为a cm,则阿伏加德罗常数为_____(用含ρ、a的代数式表示,相对原子质量:Cu-64,Cl-35.5)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)将金属钠置于空气中加热,可以观察到有淡黄色固体生成,试写出该反应的方程式:__________________________________。
(2)在实验室模拟侯氏制碱法制备碳酸钠:一定温度下,往一定量饱和NaCl溶液中通入氨气(NH3)达到饱和后,再不断通入CO2,一段时间后,出现沉淀,过滤得到NaHCO3晶体和氯化铵溶液。该过程的总的化学方程式为:____________________________________________。
(3)加热NaHCO3得到纯碱制品,实验室进行此操作的装置可以是_____________(填选项)。

(4)某实验小组通过下列实验探究过氧化钠与水的反应:

加入MnO2后,反应的化学方程式为____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】清洁能源的开发、废水的处理都能体现化学学科的应用价值。
Ⅰ. 工业上可利用CO2来制备清洁燃料甲醇,有关化学反应如下:
反应A:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1=-49.6kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.6kJ·mol-1
反应B:CO2(g)+H2![]() H2O(g)+CO(g) △H2=+41kJ·mol-1
H2O(g)+CO(g) △H2=+41kJ·mol-1
⑴ 写出用CO(g)和H2(g)合成CH3OH(g)反应的热化学方程式: __________________。
⑵ 反应A可自发进行的温度条件是________(填“低温”或“高温”) 。
⑶ 写出两个有利于提高反应A中甲醇平衡产率的条件___________。
⑷ 在Cu-ZnO/ZrO2催化下,CO2和H2混和气体,体积比1∶3,总物质的量amol进行反应,测得CO2转化率、CH3OH和CO选择性随温度、压强变化情况分别如图所示(选择性:转化的CO2中生成CH3OH或CO的百分比)。

温度对反应的影响 压强对反应的影响
① 由上图可知,影响产物选择性的外界条件是______。
A. 温度 B. 压强 C. 催化剂
② 如图中M点温度为250℃,CO2的平衡转化率为25%,该温度下反应B的平衡常数为________________(用分数表示)。
Ⅱ.实验室模拟“间接电化学氧化法”处理氨氮废水中NH4+的装置如图所示。以硫酸铵和去离子水配制成初始的模拟废水,并以NaCl调节溶液中氯离子浓度,阳极产物将氨氮废水中的NH4+氧化成空气中的主要成分。

⑸ 阳极反应式为__________________________________。
⑹ 除去NH4+的离子反应方程式为________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol·L-1的NaOH溶液,乙为0.1 mol·L-1的盐酸,丙为未知浓度的FeCl2溶液,试回答下列问题:
(1)甲溶液的pH=________。
(2)甲、乙、丙三种溶液中由水电离出的c(OH-)的大小关系为________。
(3)某化学兴趣小组认为在隔绝空气的环境中,用酸性KMnO4溶液能测定丙溶液的浓度(已知:5Fe2++MnO+8H+===5Fe3++Mn2++4H2O)。
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需________(填写仪器名称)。
②滴定实验要用到酸式滴定管或碱式滴定管,使用该仪器的第一步操作是_______。
③某同学设计的下列滴定方式中,最合理的是________(夹持部分略去,填字母序号),达到滴定终点的现象是__________________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】由含碘废水制取碘酸钾的一种工艺如下:
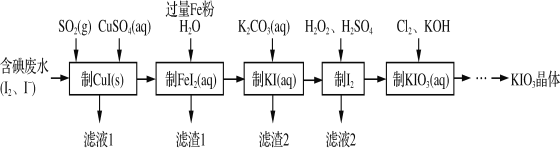
⑴ 写出KIO3在日常生活中的一个重要应用________________________。
⑵ 检验“含碘废水”中是否含有单质I2的常用试剂是________(写试剂名称)。
⑶ 通入SO2的目的是将I2还原为I-,该反应的离子方程式为______________________。
⑷ 工艺中五种物质的制备反应中,不涉及氧化还原反应的步骤是“制________”。
⑸ “制KI(aq)”时,该温度下水的离子积为Kw=1.0×10-13,Ksp[Fe(OH)2]=9.0×10-15。
为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成胶状物吸附I-,起始加入K2CO3必须保持溶液的pH不大于______。
⑹ “制KIO3溶液”反应的离子方程式为__________________。

⑺ KCl、KIO3的溶解度曲线如图所示。流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在水溶液中Fe3+和I-存在可逆反应:2Fe3++2I-![]() 2Fe2++I2,平衡常数为K。已知氢氧化铁和氢氧化亚铁的溶度积如下:Ksp[Fe(OH)2]=4.87×10-17,Ksp[Fe(OH)3]=2.64×10-39。下列判断不正确的是
2Fe2++I2,平衡常数为K。已知氢氧化铁和氢氧化亚铁的溶度积如下:Ksp[Fe(OH)2]=4.87×10-17,Ksp[Fe(OH)3]=2.64×10-39。下列判断不正确的是
A. 反应的平衡常数K=![]()
B. 该可逆反应只能在酸性条件下存在
C. 加入AgNO3,平衡右移,溶液黄色变浅
D. 加入CCl4,平衡右移,水溶液层黄色变浅
查看答案和解析>>
科目: 来源: 题型:
【题目】制备N2H4·H2O(水合肼)和无水Na2SO3主要实验流程如下:

已知:① 氯气与烧碱溶液的反应是放热反应;
② N2H4·H2O有强还原性,能与NaClO剧烈反应生成N2。
⑴从流程分析,本流程所用的主要有机原料为_______________(写名称)。
⑵步骤Ⅰ制备NaClO溶液时,若温度为41℃,测得产物中除NaClO外还含有NaClO3,且两者物质的量之比为5∶1,该反应的离子方程式为____________________。
⑶实验中,为使步骤Ⅰ中反应温度不高于40 ℃,除减缓Cl2的通入速率外,还可采取的措施是_________________。
⑷步骤Ⅱ合成N2H4·H2O(沸点约118 ℃)的装置如图。NaClO碱性溶液与尿素[CO(NH2)2](沸点196.6℃)水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。

① 使用冷凝管的目的是_________________。
② 滴液漏斗内的试剂是_______;
将滴液漏斗内的液体放入三颈烧瓶内的操作是______________________________;
③ 写出流程中生成水合肼反应的化学方程式________________________________。
⑸ 步骤Ⅳ制备无水Na2SO3(水溶液中H2SO3、HSO3-、SO32-随pH的分布如图所示)。

① 边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定停止通SO2的pH值为____(取近似整数值,下同);
②用制得的NaHSO3溶液再制Na2SO3溶液的pH应控制在________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组的同学对Zn.Cu、稀硫酸组成的原电池进行了探究,其中甲同学利用下图I装置进行探究,乙同学经过查阅资料后设计了图II装置进行探究(盐桥内含有某种电解质的饱和溶液,起到连通电路的作用)。

(1)实验表明,图I中两个电极上均有气泡产生,锌电极上有气泡产生,说明反应中有一部分化学能转化为______能;铜电极上有气泡产生,说明反应中有一部分化学能转化为____能。
(2)图II中的X、Y是ZnSO4溶液及稀硫酸中的一种,实验过程中只有正极上产生气泡,则X是_________,正极上的电极反应式为__________。
(3)当图I装置的溶液质量增加63g时,生成的氢气共有______L(标准状况);当图II中锌电极质量减少65g时,电路中转移的电子数为______NA。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com