
科目: 来源: 题型:
【题目】根据如图所示示意图,下列说法不正确的是

A. 反应的热化学方程式可表示为C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=(b-a) kJ·mol-1
CO(g)+H2(g) ΔH=(b-a) kJ·mol-1
B. 该反应过程反应物断键吸收的能量大于生成物成键放出的能量
C. a mol C和a mol H2O反应生成a mol CO和a mol H2吸收的热量一定为131.3a kJ
D. 1 mol C(g)、2 mol H、1 mol O转变成1 mol CO(g)和1 mol H2(g)放出的热量为a kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】海水占地球总储水量的97.2%,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。
(1)海水中存在大量的氯化钠,氯化钠中的金属元素位于元素周期表第________族。
(2)目前,国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸气,蒸气经冷却而得高纯度淡水。由此可判断蒸馏法是________________(填“物理变化”或“化学变化”)。
(3)工业上利用电解饱和食盐水可制得重要化工产品,反应式:食盐+H2O―→NaOH+H2↑+Cl2↑(未配平),该反应中食盐的化学式是________________________;利用电解所得气体制36.5%的浓盐酸1 000 t,最少需消耗食盐________ t。
(4)近年来,有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法。该方法流程如下:

请写出②④的化学反应方程式:______,________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是应用最广泛的金属,自远古时代人类就学会了炼铁,到目前为止,人类研制出了很多炼铁的方法。某研究性学习小组同学在实验室中模拟工业炼铁的过程,实验装置如下:
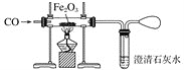
(1)写出得到单质铁的化学方程式:_________________________。
(2)实验过程中看到玻璃管内的粉末由红棕色逐渐变黑,请设计一个实验来验证生成了单质铁:______。
(3)装置末端气球的作用为_____________________________。实验结束时,应该先停止加热还是先停止通入CO?原因是什么?_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是 ( )
①增加水的量或温度,都可以加快镁跟水的反应速率。
②增加硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率。
③对反应3H2(g) + N2(g) ![]() 2NH3(g),在一密闭容器中进行,充入氦气,则化学反应速率一定不改变。
2NH3(g),在一密闭容器中进行,充入氦气,则化学反应速率一定不改变。
④对于反应3KSCN(aq) + FeCl3(aq)![]() Fe(SCN)3(aq)+ 3KC l(aq),加入KCl固体,逆反应速率瞬时增大,随后正反应速率增大
Fe(SCN)3(aq)+ 3KC l(aq),加入KCl固体,逆反应速率瞬时增大,随后正反应速率增大
A. ①② B. ①④ C. ②④ D. 无
查看答案和解析>>
科目: 来源: 题型:
【题目】CCl3CHO是一种药物合成的中间体,可通过CH3CH2OH + 4Cl2 → CCl3CHO+5HCl进行制备。制备时可能发生的副反应为C2H5OH + HCl→C2H5Cl + H2O、CCl3CHO+HClO—CCl3COOH+HCl。合成该有机物的实验装置示意图(加热装 置未画出)和有关数据如下:


(1)A中恒压漏斗的作用是______;A装置中发生反应的化学方程式为_____。
(2)装置B的作用是____;装置F在吸收气体时,为什么可以防止液体发生倒吸现象______。
(3)装置E中的温度计要控制在70℃,三口烧瓶采用的最佳加热方式是______。如果要在球形冷凝管中注入冷水增加冷凝效果,冷水应该从_____(填“a”或“b”)口通入。实验使用球形冷凝管而不使用直形冷凝管的目的是________。
(4)实验中装置C中的试剂是饱和食盐水,装置中D的试剂是浓H2SO4。如果不使用D装置,产品中会存在较多的杂质_______(填化学式)。除去这些杂质最合适实验方法是______。
(5)利用碘量法可测定产品的纯度,反应原理如下:
CCl3CHO+NaOH→CHC13+HCOONa
HCOONa+I2=HI+NaI+CO2
I2+2Na2S2O3=2NaI+Na2S4O8
称取该实验制备的产品5.00 g,配成100.00 mL溶液,取其中10.00 mL,调节溶液 为合适的pH后,加入30.00 mL 0.100 mol L-1的碘标准液,用0 100 mol L-1的 Na2S2O3溶液滴定,重复上述3次操作,消耗Na2S2O3溶液平均体积为20.00 mL,则该次实验所得产品纯度为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性。回答下列问题:

(1)按照如图装置进行实验时,首先进行的操作是________。
(2)写出装置A中所发生反应的离子方程式 ___________。
(3)装置B中最适宜的试剂是_______(填序号)。
a. NaOH溶液 b. 水 c. 澄清石灰水 d. 饱和NaHCO3 溶液
(4)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是_______。
(5)装置D中黑色固体为木炭,反应的化学方程式为__________________________。
(6)根据实验中的__________________现象,可证明CO具有还原性。
(7)若要根据装置F中澄清石灰水变浑浊的现象确认CO具有还原性,应在上图装置____与_____之间连接下图中的_____装置(填序号)。

查看答案和解析>>
科目: 来源: 题型:
【题目】2001年是伟大的化学家、1954年诺贝尔化学奖得主、著名的化学结构大师、20世纪的科学怪杰鲍林(L.Pauling)教授的诞辰100周年。1994年这位老人谢世后,人们打开他的办公室,发现里面有一块黑板,画得满满的,其中一个结构式如图所示。老人为什么画这个结构式?它能合成吗?它有什么性质?不得而知。这是鲍林留给世人的一个谜,也许这是永远无法解开的谜,也许有朝一日你就能解开它。不管结果如何,让我们先对这个结构作一番了解。

(1)它的分子式是__________________________________________________________。
(2)它的所有原子是否可能处于同一个平面上?________(填“可能”或“不可能”)。
(3)它是否带有电荷?________(填“是”或“否”)。
(4)该分子中sp杂化的氮原子有___个;sp2杂化的氮原子有___个;sp3杂化的氮原子有_____个。
(5)为什么人们推测它是炸药?______________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,浓度均为0.1 mol·Lˉ1的NaOH溶液和氨水,下列说法正确的是
A. c(NH3H2O) + c(NH4+) = c(Na+)
B. NH3的水溶液能导电,所以NH3是电解质
C. 氨水的pH大于NaOH溶液
D. 将浓度为0.1 mol·Lˉ1的盐酸和氨水等体积混合后,所得溶液中:c(OH-) > c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】研究和深度开发CO、CO2的应用具有重要的社会意义.回答下列问题:
I.CO可用于高炉炼铁,已知:
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2 (g) △H1=akJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2 (g) △ H2=bkJ/mol
则反应Fe2O3(s)+3CO(g)=2Fe(s)++3CO2 (g)的△H=______kJ/mol
Ⅱ.—定条件下,CO2和CO可以互相转化
(1)某温度下,在容积为2 L的密闭容器按甲、乙两种方式投入反应物发生反应:
CO2 (g)+H2(g) ![]() CO(g)+H2O(g)
CO(g)+H2O(g)

甲容器15 min后达到平衡,此时CO2的转化率为75%。则015 min内平均反应速率_______,此条件下该反应的平衡常数K= ____。欲使平衡后乙与甲中相同组分气体的体积分数相等,则w、x、y、z需满足的关系是: y____z(填或“>”“<”“ = ”),且y=_________(用含的等式表示)。
(2)研究表明,温度、压强对反应“C6H5CH2CH3 (g)+CO2(g) ![]() C6H5CH=CH2(g)+CO(g) + H2O(g)”中乙苯的平衡转化率影响如图所示:
C6H5CH=CH2(g)+CO(g) + H2O(g)”中乙苯的平衡转化率影响如图所示:

则△H_____(填“>”、“<”或“ = ”),压强p1、p2、p3从大到小的顺序是_____。
(3)CO可被NO2氧化:CO+NO2 =CO2+ NO。当温度高于225℃时,反应速率![]() 正=k正 c(CO) c(NO2),
正=k正 c(CO) c(NO2), ![]() 逆=k逆 c(CO2) c(NO), k正、k逆分别为正、逆反应速率常数。在上述温度范围内, k正、k逆与该反应的平衡常数K之间的关系为___________。
逆=k逆 c(CO2) c(NO), k正、k逆分别为正、逆反应速率常数。在上述温度范围内, k正、k逆与该反应的平衡常数K之间的关系为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质投入溶液中,溶液质量减轻的是( )
A.CaCO3投入到HCl溶液中
B.Na2CO3投入稀硫酸中
C.Fe粉投入CuSO4溶液中
D.Fe粉投入稀HCl溶液中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com