
科目: 来源: 题型:
【题目】M、N、O、P、Q是元素周期表中原子序数依次递增的前四周期元素.M原子最外层电子数为内层电子数的3倍;N的焰色反应呈黄色;O的氢化物是一种强酸,其浓溶液可与M、Q的化合物反应生成O的单质;P是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题:
(1)元素Q的名称为______________,P的基态原子价层电子排布式为__________________。
(2)O的氢化物的沸点比其上一周期同族元素的氢化物低,是因为___________________。
(3)M、O电负性大小顺序是__________(用元素符号表示),O的最高价含氧酸根的空间构型为_____________,其中心原子的杂化类型为_______________。
(4)M、N形成的化合物的晶胞如图所示,该晶胞的化学式为__________________,其中M离子的配位数为_____________,该晶体类型为____________________。
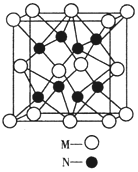
(5)该晶胞的边长为 a pm,则该晶体的密度为____________________g/cm3
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为____________反应(选填吸热、放热)。
(2)能判断该反应是否达到化学平衡状态的依据是_________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 _________℃。
Ⅱ、向一体积不变的密闭容器中充入2 mol A、0.6 mol C和一定量的B三种气体,一定条件下发生反应2A(g)+B(g) ![]() 3C(g),各物质的浓度随时间变化的关系如图1所示,其中如t0~t1阶段c(B)未画出。图2为反应体系中反应速率随时间变化的情况,且t2、t3、t4各改变一种不同的条件。
3C(g),各物质的浓度随时间变化的关系如图1所示,其中如t0~t1阶段c(B)未画出。图2为反应体系中反应速率随时间变化的情况,且t2、t3、t4各改变一种不同的条件。
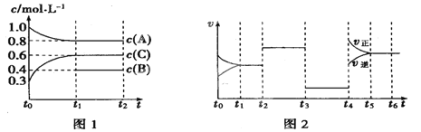
(1)若t1=15 min,则t0~t1阶段以C的浓度变化表示的反应速率V(C)=_____。
(2)t3时改变的条件为___________,B的起始物质的量为_______。
(3)t4~t5阶段,若A的物质的量减少了0.01 mol,而此阶段中反应体系吸收能量为a kJ,写出此条件下该反应的热化学方程式___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】锆(Zr)是40号元素,位于第五周期ⅣB族,锆可溶于氢氟酸和王水,锆及其化合物在陶瓷、耐火材料等多个领域有着重要用途。请回答下列相关问题。
(1)基态锆原子的价电子排布图(轨道表示式)是___。
(2)ZrSiO4和ZrSiO3是锆的两种硅酸盐,二者含有的阳离子Zr4+和Zr2+中比较稳定的是____,原因是___。SiO32-的空间构型是____,SiO42-中的Si原子的杂化类型是____。
(3)[Zr(C2H5O)2]2+是Zr4+形成的一种配离子,其中的配位原子是___(填元素符号),该离子中含有的化学键种类不包括___(填选项序号)。
A.极性键 B.非极性键 C.σ键 D.π键
(4)立方氧化锆是一种人工合成的氧化物,由于硬度极高且外观接近钻石常被用作钻石的替代品,其晶胞结构如图所示,立方氧化锆的化学式是___,锆原子的配位数是____。若晶胞中距离最近的两个氧原子间的距离为anm,则立方氧化锆的密度为__g/cm3。
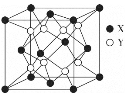
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,容器底部是培养基(含有植物生长所需的全部养分),如果有人在配制培养基的化学元素中使用了NH4NO3、KNO3、CaCl2、KH2PO4、铁溶液、微量元素溶液,但仍需补充缺少了的必需元素,应添加的化合物是

A.MgSO4B.MgCl2C.K2SO4D.Ca(NO3)2
查看答案和解析>>
科目: 来源: 题型:
【题目】为配制480mL0.1mol·L-1Na2SO4溶液。回答下列问题。
(1)配制Na2SO4溶液时需用的主要仪器有托盘天平、药匙、烧杯、玻璃棒、___、___。
(2)用托盘天平称十水硫酸钠(Na2SO4·10H2O)晶体__g。
(3)下列操作对所配溶液的浓度有何影响(填“偏高、偏低或无影响”)
A.误用“左码右物”的称量方法称该晶体___
B.容量瓶未经干燥即使用___
C.溶解后没有冷却便进行定容___
D.忘记将洗涤液转入容量瓶___
E.定容时俯视刻度线定容___
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A.质量数是将原子核内所有的质子和中子的相对质量取整数值之和
B.![]() X表示一种X元素的一种原子,中子数为A-Z
X表示一种X元素的一种原子,中子数为A-Z
C.![]() X中,A为该原子的相对原子质量的近似值
X中,A为该原子的相对原子质量的近似值
D.原子都是质子和中子、电子组成,原子不带电
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A.物质的量是研究物质所含微粒集体的多少,单位为mol
B.物质的量把微观粒子数目与宏观物质的质量联系起来
C.1molNaCl晶体中含有NA个NaCl分子
D.12gC-12中所含的原子数为阿伏加德罗常数,NA近似为6.02×1023mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】柠檬烯(结构如图1所示)是食品行业中常用的一种香精,柠檬烯熔点为-74.3℃,沸点为177℃,难溶于水,在接近100℃时有一定的挥发性。柠檬、橙子和柚子等水果果皮中存在较多的柠檬烯,实验室通常用水蒸气蒸馏(装置如图2所示)的方法将柠檬烯从果皮中提取出来并进行后续的分离提纯。
水蒸气蒸馏:将60g橙子皮剪成碎片投入仪器B中,加入30mL蒸馏水,打开T形管活塞,点燃酒精灯加热水蒸气发生装置,待T形管支管口有大量水蒸气冒出时关闭活塞并开始通入冷凝水,当D中收集到约60~70mL馏出液时停止蒸馏。
分离提纯:将馏出液倒入分液漏斗,每次用10mL二氯甲烷(沸点39.95℃)萃取三次,萃取液合并后置于锥形瓶中,加入适量无水硫酸镁,半小时后过滤,将滤液进行蒸馏除去二氯甲烷,蒸馏烧瓶中得到主要成分是柠檬烯的橙油。
请回答相关问题。

(1)仪器A的名称是____。安全管下端不能抵住仪器A的底部,原因是__。仪器B中水蒸气导入管管口接近瓶底,目的是___。
(2)直形冷凝管填能否更换为球形冷凝管___(“能”或“否”),原因是___。
(3)分离提纯过程中加入无水硫酸镁的作用是____。对滤液进行蒸馏时合适的加热方法是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】在实验室里,用足量的浓盐酸与一定量的MnO2反应,来制取氯气。
⑴用“双线桥法”标出电子转移情况
MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
⑵若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
①理论上需要多少克MnO2参加反应?
②被氧化的HCl的物质的量为多少?
查看答案和解析>>
科目: 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有CaCl2、MgCl2、Na2SO4以及泥沙等杂质,以下是制备精盐的实验方案,步骤如下图:
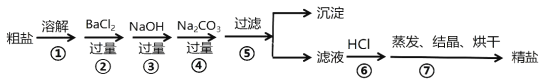
(1)第②步操作的目的是除去粗盐中的______________;( 填化学式,下同)
(2)图中“沉淀”的成分是:____________、_____________、____________、_____________;
(3)第④步操作的目的是除去________________、_________________;写出相应的离子反应方程式:_______________________;_________________________;
(4)第⑥步操作的目的是_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com