
科目: 来源: 题型:
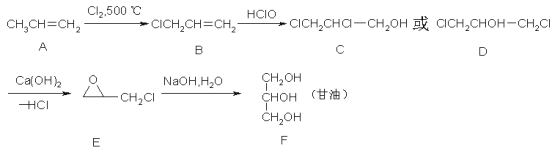
【题目】甘油(丙三醇)在纺织、医药、化妆品工业及日常生活中用途很广,可以通过以下方法合成:
完成下列填空:
(1)A中官能团的名称是____________,A→B的反应类型是__________;
(2)写出A发生加聚反应后产物的结构简式__________________;
(3)B→C的反应类型是______________,C与D互为______________;
(4)写出A→B的化学方程式:__________________________________;
查看答案和解析>>
科目: 来源: 题型:
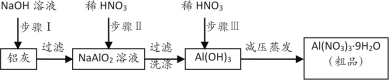
【题目】硝酸铝[Al(NO3)3]是一种常用媒染剂。工业上用铝灰(主要含Al、Al2O3、Fe2O3等)制取硝酸铝晶体[Al(NO3)3·9H2O]的流程如下:
完成下列填空:
(1)常温下,铝遇浓硫酸、浓硝酸时在表面生成致密的氧化膜,这种现象称为__________,铝粉常用来还原一些金属氧化物以冶炼某些难熔的金属,这类氧化还原反应叫__________反应;
(2)步骤Ⅰ的离子方程式是_________________,_________________;
(3)若在实验室中完成步骤Ⅱ,为提高铝元素的利用率,可用__替换稀硝酸;
a.稀硫酸 b.稀盐酸 c.醋酸 d.二氧化碳
(4)在步骤Ⅲ的实际操作过程中,待沉淀完全溶解后还会加入稍过量稀硝酸,用平衡移动原理解释此时加入稀硝酸的目的:_______________________;
(5)温度高于200℃时,硝酸铝完全分解成氧化铝、二氧化氮和氧气,写出该反应的化学方程式:_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】配制400 mL 0.5 mol·L-1的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为______。
(2)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放在标尺的零刻度处,天平静止时发现 指针在分度盘的偏右位置,此时左边的托盘将______(填“高于”或“低于”)右边的托盘。欲使天平平衡,所进行的操作为_______。假定最终称得小烧杯的质量为______(填“32.6 g”或“31.61 g”),
(3)配制方法:设计五个操作步骤:
① 向盛有NaOH的烧杯中加入200 mL蒸馏水使其溶解,并冷却至室温;
② 继续往容量瓶中加蒸馏水至液面接近刻度线1~2 cm处;
③ 将NaOH溶液沿玻璃棒注入500 mL容量瓶中;
④ 在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移入容量瓶;
⑤ 改用胶头滴管加蒸馏水至刻度线,加盖摇匀。
试将以上操作排出先后顺序______。
(4)某学生实际配制NaOH溶液的浓度为0.48 mol·L-1,原因可能是______。
A.使用滤纸称量氢氧化钠固体 |
B.容量瓶中原来存有少量蒸馏水 |
C.溶解NaOH的烧杯未经多次洗涤 |
D.胶头滴管加水后定容时仰视刻度 |
(5)在下列配制0.5 mol·L-1NaOH溶液过程示意图中有错误的是(填序号)______。

查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,氧化剂与还原剂的物质的量之比为1∶2的是( )
①2Na2O2+2H2O=4NaOH+O2 ②3S+6NaOH![]() 2Na2S+Na2SO3+3H2O ③SiO2+3C
2Na2S+Na2SO3+3H2O ③SiO2+3C![]() SiC+2CO↑ ④4HCl(浓)+MnO2
SiC+2CO↑ ④4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
A.仅有②B.仅有②④C.仅有③④D.①②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。

完成下列填空(填元素符号或化学式):
(1)元素B在元素周期表中的位置是第____周期第_____族,A、B、C三种元素原子半径从大到小的顺序是_________________;
(2)D简单离子的结构示意图为_____________,D、E中金属性较强的元素是________。D单质在空气中燃烧可生成淡黄色粉末X(D2O2),X常用作呼吸面具和潜水艇中的供氧剂,可选用合适的化学试剂和下图所示实验装置证明X有提供氧气的作用。
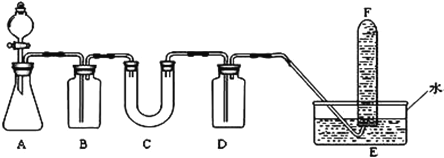
(3)装置A使用石灰石与浓盐酸反应制取CO2,装置B中饱和NaHCO3溶液的作用是除去_____________;
(4)装置C中X与CO2反应的化学方程式是_____________________,装置D盛放NaOH溶液的作用是除去____________;
(5)为检验试管F收集的气体,进行____________操作,出现_________现象,即证明X可作供氧剂。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定体积的含有Al3+、Mg2+、Ba2+的混合溶液中逐滴加入NaOH和Na2SO4的混合溶液(除上述离子外,其他离子不与所加试剂反应,假设Al3+、Mg2+结合OH-的能力相同),产生沉淀的物质的量与所加溶液的体积的关系如图所示。下列说法正确的是:
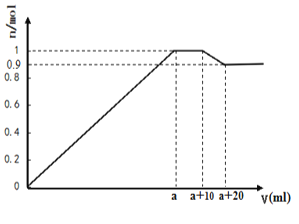
A. 当a<V<a+10时,不再生成难溶物
B. 上述含Al3+、Mg2+、Ba2+的混合溶液中3c(Al3+)+2c(Mg2+)=c(Ba2+)
C. 上述含Al3+、Mg2+、Ba2+的混合溶液中n(Al3+) = 0.2mol
D. NaOH和Na2SO4的混合溶液中c(NaOH)>c(Na2SO4)
查看答案和解析>>
科目: 来源: 题型:
【题目】某强酸性溶液X中含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、S![]() 、Cl-、N
、Cl-、N![]() 。中的一种或几种,取该溶液进行连续实验,实验过程如下:(已知气体D在常温常压下呈红棕色)
。中的一种或几种,取该溶液进行连续实验,实验过程如下:(已知气体D在常温常压下呈红棕色)

(1)上述离子中,溶液X中除H+外肯定还含有的离子是_,一定不含的离子是__,不能确定是否含有的离子是_______,检验其中阳离子的方法是________。
(2)沉淀G的化学式为______。
(3)写出生成A的离子方程式:________。
(4)写出溶液H中通入过量CO2的离子方程式:________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A.1 mol S和O2的摩尔质量都是32 g
B.23g NO2和N2O4的混合气体中所含的O原子数为NA
C.1 mol任何气体中都含有相同的原子数
D.22.4 L CO2气体中含有3NA个原子
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值。下列有关叙述正确的是
A.16g由O2和O3组成的混合气体中的氧原子数为2NA
B.1molN2与足量H2充分反应生成NH3的分子数为2NA
C.1mol Fe溶于过量稀硝酸,转移的电子数为3NA
D.标准状况下,2.24L苯中含有的原子数为1.2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com