
科目: 来源: 题型:
【题目】(1)已知:①N2(g)+O2(g)=2NO(g) ΔH=180.5 kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ· mol-1
③2C(s)+O2(g)= 2CO(g) ΔH=-221 kJ· mol-1
若某反应Ⅰ的平衡常数表达式为K=![]() 请写出此反应的热化学方程式:________,该反应自发进行的条件是_________。
请写出此反应的热化学方程式:________,该反应自发进行的条件是_________。
(2)一定温度下,向体积为V L的密闭容器中充入一定量的NO和CO,发生反应Ⅰ。
①下列说法正确的是____。
A 当容器内气体压强不再发生变化时,说明反应已达到平衡状态
B 当v(CO2)=v(CO)时,说明反应已达到平衡状态
C 达到平衡后,若向容器中再充入一定量NO,则NO转化率将减小
D 达到平衡后,若再升高温度,由于逆反应速率增大,正反应速率减小,因此平衡向逆反应方向移动
②若反应在t1时刻达到平衡状态,在其他条件不变的情况下,t2时刻通过缩小容器体积使压强增大到原来的2倍,t3时刻达到新的平衡状态。请在图中补充画出t2~t4时段c(NO)的变化曲线: ____

(3)分离高炉煤气得到的CO与空气可设计成燃料电池而除去(以KOH溶液为电解质溶液)。写出该电池的负极反应式:_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法正确的是

A.用澄清的石灰水可鉴别NaHCO3和Na2CO3
B.溴元素在第③、⑤中被氧化,在第④中被还原
C.工业上一般用金属钠与无水MgCl2反应制取Mg单质
D.海水中还含有碘元素,只需将海水中的碘升华就可以得到碘单质
查看答案和解析>>
科目: 来源: 题型:
【题目】根据所学内容填空
(1)1mol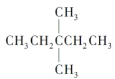 在氧气中充分燃烧,需要消耗氧气___________mol,它在光照的条件下与氯气反应,能生成_____种不同的一氯取代物。
在氧气中充分燃烧,需要消耗氧气___________mol,它在光照的条件下与氯气反应,能生成_____种不同的一氯取代物。
(2)现有三种有机物A.![]() B.CH3CH2CH2CH2CH3C.
B.CH3CH2CH2CH2CH3C.![]() ,其中A与B互称为__________________;B与C互称为___________________.
,其中A与B互称为__________________;B与C互称为___________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%,结构中有三种位置不同的氢原子。
(1)X的分子式是________;官能团名称________。
(2)X与金属钠反应放出氢气,反应的化学方程式是________________________。
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是________;X还可以被高锰酸钾溶液直接氧化成________(填写名称)。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用下图所示装置进行液体石蜡分解及其产物性质实验。下列操作或叙述错误的是
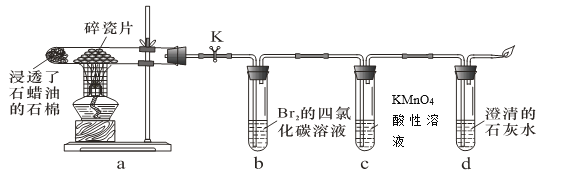
A.装置b、c中发生反应的基本类型不同B.d中溶液变浑浊证明石蜡分解产生了CO2
C.实验中可以看到b、c中溶液褪色D.停止加热后立即关闭K可以防止液体倒吸
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20.00 mL 0.100 0 mol·L-1 (NH4)2SO4溶液中逐滴加入0.200 0 mol·L-1 NaOH溶液时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑NH3·H2O的分解)。下列说法不正确的是( )
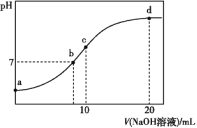
A.点a所示溶液中:c(![]() )>c(
)>c(![]() )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.点b所示溶液中:c(![]() )=c(Na+)>c(H+)=c(OH-)
)=c(Na+)>c(H+)=c(OH-)
C.点c所示溶液中:c(![]() )+c(H+)+c(Na+)=c(OH-)+2c(
)+c(H+)+c(Na+)=c(OH-)+2c(![]() )
)
D.点d所示溶液中:c(![]() )+c(NH3·H2O)=0.100 0 mol·L-1
)+c(NH3·H2O)=0.100 0 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】立方烷(C8H8)其八个碳原子对称地排列在立方体的八个角上。以下相关说法错误的是
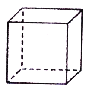
A.立方烷是苯(C6H6)的同系物
B.立方烷一氯代物1种、二氯代物有3种
C.立方烷在空气中可燃,燃烧有黑烟产生
D.立方烷三氯代物和五氯代物种类相同
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,甲、乙是电化学实验装置,请回答下列问题:

(1)若甲、乙两个烧杯中均盛放饱和NaCl溶液。
①甲中石墨棒上的电极反应式是____________。
②将湿润的淀粉KI试纸放在乙烧杯的上方,发现试纸先变蓝后褪色,这是因为电解生成的某种气体A氧化了I-生成了I2。若A气体和I2按物质的量之比为5∶1反应,且生成两种酸,该反应的化学方程式为_________。
③如果不考虑气体产物与烧杯中溶液之间的反应,当乙反应有0.01 mol电子转移后停止实验,烧杯中溶液的体积为100 mL,则溶液混匀后的c(OH-)=_____。
(2)若甲、乙两烧杯中均盛放CuSO4溶液。
①甲中铁棒上的电极反应式为_______________。
②乙中总反应的离子方程式为_________________。
③如果起始时乙中盛放100 mL pH=5的CuSO4溶液(25℃),一段时间后溶液的c(H+)=0.1mol/L,若要使溶液恢复到起始时的浓度(忽略溶液体积的变化),可向溶液中加入_____ (填写物质的化学式)______g。
查看答案和解析>>
科目: 来源: 题型:
【题目】人体吸入CO后在肺中发生反应CO+HbO2![]() O2+HbCO导致人体缺氧。向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L],氧合血红蛋白 HbO2浓度随时间变化曲线如图所示。下列说法正确的是( )
O2+HbCO导致人体缺氧。向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L],氧合血红蛋白 HbO2浓度随时间变化曲线如图所示。下列说法正确的是( )

A.反应开始至4s内用HbO2表示的平均反应速率为2×l0-4mol/(L·s)
B.反应达平衡之前,O2与HbCO的反应速率逐渐减小
C.将CO中毒病人放入高压氧舱治疗是利用了化学平衡移动原理
D.该温度下反应CO+HbO2 ![]() O2+HbCO的平衡常数为107
O2+HbCO的平衡常数为107
查看答案和解析>>
科目: 来源: 题型:
【题目】根据能量示意图,下列判断正确的是( )
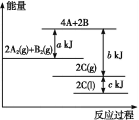
A.化学反应中断键要放出能量,形成化学键要吸收能量
B.该反应的反应物总能量小于生成物总能量
C.2A2(g)+B2(g)= 2C(g)ΔH=-(b+c-a)kJ·mol-1
D.由图可知,生成1 mol C(l),放出![]() (b+c-a)kJ热量
(b+c-a)kJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com