
科目: 来源: 题型:
【题目】聚合物F的合成路线图如下:
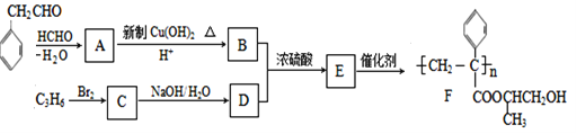
已知:![]()
![]()
请据此回答:
(1)A中含氧官能团名称是_____,D的系统命名为_____。
(2)检验B中含氧官能团所用的试剂是____;E→F的反应类型是_____。
(3)C生成D的反应化学方程式为_______,E合成F的反应化学方程式为________。
(4)G物质与![]() 互为同系物,且G物质的相对分子质量比
互为同系物,且G物质的相对分子质量比![]() 大14,则符合下列条件的G的同分异构体有____种。
大14,则符合下列条件的G的同分异构体有____种。
①分子中含有苯环,且苯环上有两个取代基 ②遇氯化铁溶液变紫色 ③能与溴水发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某些物质的转化可用下图表示,且x,y,z都含有相同的一种元素。图示中有部分生成物未列出来
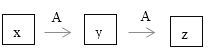
(1)①若x是AlCl3,则y的化学式是________________
②若x的阴离子含有铝元素,写出此阴离子与过量盐酸反应的离子方程式:___________________
(2)若x是一种黄绿色有毒单质气体,A是世界使用量最大的一种金属单质。
①写出A元素原子的电子排布式:__________________
②配制y的溶液,一般不是把Y的晶体溶于水,而是把y的晶体先溶解于_________(填化学式)溶液中。
③如何检验z物质中的阳离子:________________________________________________。
(3)①若x是能使湿润红色石蕊试纸变蓝的气体,该气体的中心原子轨道杂化类型是______________
②下列各组组合,不符合上图反应的是______________(填序号)
Ⅰ x: N2 A: O2 Ⅱ x: Al A: NaOH Ⅲ x: Ba(OH)2 A: CO2
Ⅳ x: S A: O2 Ⅴ x: HNO3 A: Fe Ⅵ x: SiO2 A: C
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酰氯(SO2Cl2)熔点-54.1℃、沸点69.2℃,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。
(1)SO2Cl2中S的化合价为___________,SO2Cl2在潮湿空气中因水解“发烟”的化学方程式为__________。
(2)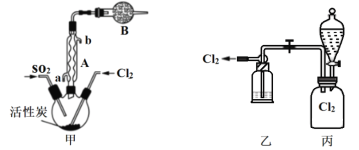
①仪器A的名称为___________,装置B的作用是____________。
②装置乙中装入的试剂是浓硫酸,装置丙分液漏斗中盛装的最佳试剂是________(选填字母)。
A.蒸馏水 B.10.0 molL1浓盐酸 C.浓氢氧化钠溶液 D.饱和食盐水
③滴定法测定硫酰氯的纯度:取1.800g产品,加入到100mL 0.5000mol·L1 NaOH溶液中加热充分水解,冷却后加蒸馏水准确稀释至250mL,取25mL溶液于锥形瓶中,滴加2滴甲基橙,用0.1000mol·L1标准HCl滴定至终点,重复实验三次取平均值,消耗10.00mL滴定终点的判断为___________,产品的纯度为_________。
(3)探究硫酰氯在催化剂作用下加热分解的产物,实验装置如图所示(部分夹持装置未画出)。

①加热时A中试管出现黄绿色,装置B的作用是_________。
②装置C中反应的离子方程式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇制烯烃(MTO)是煤制烯烃工艺路线的核心技术。煤制烯烃主要包括煤的气化、液化、烯烃化三个阶段。
(1)煤的液化发生的主要反应之一为2H2(g)+CO(g)=CH3OH (g) ΔH=a kJ·mol1,在不同温度下,K(500℃)=2.5 L2·mol2,K(700℃)=0.2 L2·mol2。
①ΔH________0(填“>”、“<”、“=”)。
②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内H2、CO、CH3OH物质的量分别为2 mol、1 mol、3mol,则此时生成CH3OH的速率____消耗CH3OH的速率(填“>”、“<”、“=”)。
(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
i 2CH3OH(g)=C2H4(g)+2H2O(g) ΔH1=-20.9 kJ·mol1
ii3CH3OH(g)=C3H6(g)+3H2O(g) ΔH2=-98.1 kJ·mol1
iii 4CH3OH(g)=C4H8(g)+4H2O(g) ΔH3=-118.1 kJ·mol1
①C3H6转化为C2H4的热化学方程式为iv:2C3H6(g)![]() 3C2H4 (g) ΔH4=____。
3C2H4 (g) ΔH4=____。
②加入N2作为稀释剂,反应i中C2H4的产率将_____(增大、减小、不变)。
(3)为研究不同条件对反应的影响,测得不同温度下平衡时C2H4、C3H6和C4H8的物质的量分数变化,如图所示:
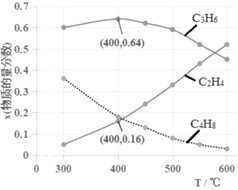
①随着温度的升高,C3H6的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是_____________________________;当温度低于400℃时,原因是________________________。
②体系总压为0.1MPa,400℃时反应iv的平衡常数Kp=________(列式计算,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③为了获得更高的C2H4在产物中的比例,除控制较高温度的条件外,以下较适宜的是______。
A.增加水醇比 B.降低水醇比
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃时,在含CH3COOH和CH3COO-的溶液中, CH3COOH、CH3COO-二者中各自所占的物质的量分数(a)随溶液pH变化的关系如图所示。

下列说法不正确的是
A. 在pH<4.76的溶液中,c(CH3COO-)<c(CH3COOH)
B. 在pH=7的溶液中,a(CH3COOH)=0,a(CH3COO-)=1.0
C. 在pH>4.76的溶液中,c(CH3COO-)与c(OH-)之和可大于c(H+)
D. 在pH=4.76的溶液中加盐酸,a(CH3COOH)与a(CH3COO-)之和保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化镁常用于制备其它超硬、高导热、耐高温的氮化物,实验室用以下装置制取氮化镁。已知:Mg+2NH3![]() Mg(NH2)2+H2,Mg3N2是一种浅黄色粉末,易水解。下列说法不正确的是
Mg(NH2)2+H2,Mg3N2是一种浅黄色粉末,易水解。下列说法不正确的是
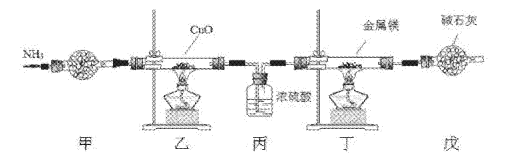
A. 实验开始时应先点燃乙处酒精灯,再点燃丁处酒精灯
B. 装置乙的目的是制备N2
C. 装置丙与装置戊可以对调
D. 取装置丁所得固体少许,滴入少量蒸馏水,可检验是否有Mg3N2
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E五种有机物,它们的分子分别由—CH3、—OH、—COOH、—CHO、—C6H5( 代表苯基)中的两种组成,这些化合物的性质如下所述:
①A能够发生银镜反应,且相对分子质量为44;
②B溶液加入氯化铁溶液中,溶液显紫色;
③C和E在有浓硫酸存在并加热的条件下,能发生酯化反应,C和E的相对分子质量之比为8:15;
④B和E都能跟氢氧化钠溶液反应,而A、C、D则不能;
⑤D属于烃类,且D能使酸性高锰酸钾溶液褪色,还能发生硝化反应。
请回答下列问题:
(1)B、D的结构简式是:B_____D______
(2)写出A发生银镜反应的化学方程式:________
(3)C和E发生酯化反应的化学方程式:_______
查看答案和解析>>
科目: 来源: 题型:
【题目】已知有机物A、B、C、D、E、F、G有如下转化关系,其中C是最简单的烯烃,G的分子式为C9H10O2,试回答下列有关问题。
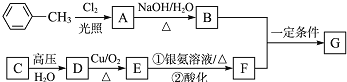
(1)G的名称为_____。
(2)指出下列反应的反应类型:A转化为B:____;C转化为D:___。
(3)写出下列反应的化学方程式:G与足量NaOH溶液反应的化学方程式:____。
(4)符合下列条件的G的同分异构体数目为____种。
①苯环上有3个取代基,且有两个取代基相同;
②能够与新制的银氨溶液反应产生光亮的银镜。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上由黄铜矿(主要成分为 CuFeS2)冶炼铜的主要流程如下。下列说法不正确的是
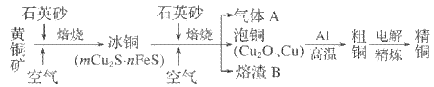
A. 气体A中的大气污染物可用氨水吸收并回收利用
B. 由泡铜冶炼粗铜的化学方程式为3Cu2O+2Al ![]() Al2O3+6Cu
Al2O3+6Cu
C. 加入石英砂作为添加剂熔剂,生成更稳定、更容易分离的硅酸盐
D. 用过量稀H2SO4可全部溶解熔渣B
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备1,2-二溴乙烷,可用足量的乙醇先制备乙烯,再用乙烯和少量的溴制备1,2-二溴乙烷,装置如下图所示:
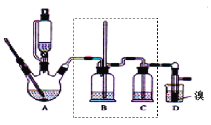
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是____;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置A中除了浓硫酸和乙醇外,还应加入___,其目的是_____,装置A中生成副产物乙醚的化学反应方程式 ______。
(3)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4反应生成少量的二氧化硫,为了验证二氧化硫的存在并除去二氧化硫对后续反应的干扰,某同学在A和D之间加入了B、C两个装置,其中B和C中可分别盛放_____
a.酸性KMnO4和水 b.品红和NaOH溶液
c.酸性KMnO4和NaOH溶液 d.品红和酸性KMnO4
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在____层(填“上”、“下”);若产物中有少量副产物乙醚。可用_____的方法除去。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com