
科目: 来源: 题型:
【题目】K2FeO4在酸性或中性溶液中能快速产生O2,在碱性溶液中较稳定。如图是制备高铁酸钾的一种装置,制取实验完成后,取C中紫色溶液,加入稀盐酸,产生气体。下列说法不正确的是( )
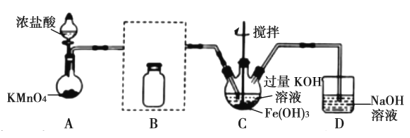
A.B瓶应盛放饱和食盐水除去混有的HCl
B.C瓶中KOH过量更有利于高铁酸钾的生成
C.加盐酸产生气体可说明氧化性:K2FeO4>Cl2
D.高铁酸钾是集氧化、吸附、絮凝等特点为一体的优良的水处理剂
查看答案和解析>>
科目: 来源: 题型:
【题目】现有①Na2CO3溶液 ②NaOH固体 ③CO2 ④石墨 ⑤熔融BaCl2五种物质,按要求回答下列问题:
(1)属于电解质的是____________(填代号,下同);属于非电解质的是____________;能导电的是______________。
(2)上述物质中有些物质在一定条件下可以反应,请按要求写出相应的化学方程式:
①是化合反应,也是氧化还原反应_________________________________。
②是化合反应,不是氧化还原反应_________________________________。
③是复分解反应,且有沉淀生成__________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是s能级和p能级的电子云轮廓图,试回答问题。


(1)s电子云轮廓图呈________形,每个s能级有________个原子轨道;p电子云轮廓图呈________状,每个p能级有________个原子轨道,其能量关系为____________(填“相同”或“不相同”)。
(2)元素X的原子最外层的电子排布式为nsnpn+1,原子中能量最高的是________电子;元素X的名称是____,它的氢化物的电子式是________。
(3)若元素Y的原子最外层的电子排布式为nsn-1npn+1,那么Y的元素符号应为________,原子的电子排布图为______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】0.1mol以CnHmCOOH所表示的羧酸加成时需50.8g碘,0.1mol该羧酸完全燃烧时,产生CO2和H2O共3.4mol,该羧酸是( )
A. C15H27COOHB. C15H31COOH
C. C17H31COOHD. C17H33COOH
查看答案和解析>>
科目: 来源: 题型:
【题目】某相对分子质量小于200的芳香族含氧衍生物中氧的质量分数约为13.1%(仅含碳、氢、氧三种元素),已知其分子中含有2个-CH3,且该物质遇FeCl3溶液显紫色,则该有机物的结构式共有
A. 2种B. 4种C. 6种D. 8种
查看答案和解析>>
科目: 来源: 题型:
【题目】最早的麻醉药是从南美洲生长的古柯植物提取的可卡因,目前人们已实验并合成了数百种局部麻醉剂,多为羧酸酯类。F是一种局部麻醉剂,其合成路线:
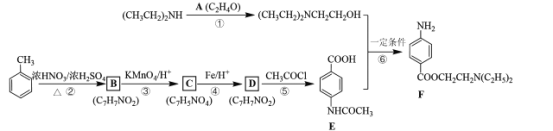
回答下列问题:
(1)已知A的核磁共振氢谱只有一个吸收峰,写出A的结构简式____。
(2)B的化学名称为________。
(3)D中的官能团名称为____,④和⑤的反应类型分别为________、____。
(4)写出⑥的化学方程式____。
(5)C的同分异构体有多种,其中-NO2直接连在苯环上且能发生银镜反应的有_____种,写出其中苯环上一氯代物有两种的同分异构体的结构简式____________。
(6)参照上述流程,设计以对硝基苯酚钠、乙醇和乙酰氯(CH3COCl)为原料合成解热镇痛药非那西丁(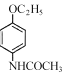 )的合成路线(无机试剂任选)。已知:
)的合成路线(无机试剂任选)。已知: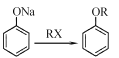 __________
__________
查看答案和解析>>
科目: 来源: 题型:
【题目】在分析化学的电位法中,甘汞电极常做参比电极,它是由金属汞及其难溶盐Hg2Cl2和KCl溶液组成的电极。Hg2Cl2(甘汞)毒性较小,而HgCl2(升汞)有剧毒。
(1)K元素的基态原子的电子填充于_____个不同的能级。
(2)Hg的价层电子排布式为5d106s2,Hg元素位于元素周期表的_______区。
(3)Hg2Cl2在400~500℃时升华,由此推测Hg2Cl2的晶体类型为____。
(4)KCl和NaCl相比,____ 的熔点更高,原因是________。
(5)把NH4Cl和HgCl2按一定比例混合,在密封管中加热时,生成某种晶体,其晶胞如图所示。用X-射线衍射法测得该晶体的晶胞为长方体(晶胞参数a=b =419pm、c=794pm),每个NH4+可视为被8个Cl-围绕,距离为335pm,Cl-与Cl-尽可能远离。
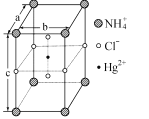
①该晶体的化学式为________。
②晶体中Cl-的空间环境_____________(填“相同”或“不相同”)。用题中数据说明理由_______________
③设阿伏加德罗常数的值为NA,则该晶体的密度为_______g/cm3(列出计算表达式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)如图进行实验,将a溶液逐渐加入盛b溶液的试管中,写出试管中观察到的现象及对应的离子方程式___。
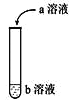
a | b | 试管中现象 | 离子方程式 |
Na2CO3 | 稀盐酸 | ||
稀盐酸 | Na2CO3 |
(2)工业上利用NaIO3和NaHSO3反应来制取单质I2。配平下列化学方程式并用单线桥法表示电子转移的方向和数目:___。
NaIO3+NaHSO3=I2+Na2SO4+H2SO4+H2O
(3)ClO2常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并用双线桥法表示电子转移的方向和数目___。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮是地球上含量比较丰富的一种元素,氮的化合物在工业生产和生活中有重要的作用。
I.已知298K时,发生反应:N2O4(g) ![]() 2NO2(g)
2NO2(g)
(1)反应达到平衡后,压缩容器的体积,再次达到平衡时混合气体的颜色 ____(填“变深”、“变浅”或“不变”)。
(2)恒容密闭容器中发生上述反应,已知v正=k正·p(N2O4),v逆=k逆·p2(NO2),Kp=___________(用k正、k逆表示)。若初始压强为100kPa,k正=2.8×104s-1,当NO2的体积分数为40%时,v正=__________kPa·s-1。[其中p(N2O4)和p(NO2)分别是N2O4和NO2的分压,分压=p总×气体体积分数,k正、k逆为速率常数]
Ⅱ.在催化剂作用下,H2可以还原NO消除污染,反应为:2NO(g)+2H2(g)![]() N2(g)+2H2O(g) △H=akJ·mol-1
N2(g)+2H2O(g) △H=akJ·mol-1
(3)若每生成7g N2放出166kJ的热量,则a=____。
(4)该反应分两步进行:
①2NO(g)+H2(g)![]() N2(g)+H2O2(g) △H1
N2(g)+H2O2(g) △H1
②H2O2(g)+H2(g)![]() 2H2O(g) △H2
2H2O(g) △H2
已知:i.总反应分多步进行时,较慢的一步决定总反应速率;
III.总反应的速率表达式v=kc2(NO)·c(H2)(k为速率常数,只和温度有关)。由上述信息可知,正反应的活化能较低的是____(填“①”或“②”)。
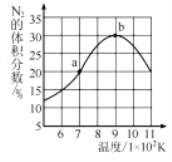
(5)将2molNO和1molH2充入一个恒容的密闭容器中,经相同时间测得N2的体积分数与温度的关系如图所示。低于900K时,N2的体积分数_____(填“是”或“不是”)对应温度下平衡时的体积分数,原因是_____。高于900K时,N2的体积分数降低的可能原因是____。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种由明矾石[主要成分:KAl3(SO4)2(OH)6]和地开石[主要成分:Al4(Si4O10)(OH)8]提取K2SO4和Al的工艺流程:

已知:K2SO4在不同温度下的溶解度
温度/℃ | 10 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 9.3 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
回答下列问题:
(1)硫酸熟化工艺是指浓硫酸在矿物颗粒表面均匀分布并向内扩散的过程,该过程中矿物颗粒_____(填“是”或“不是”)越细越好。
(2)完成并配平还原焙烧时明矾石与硫反应的化学方程式:________
![]() KAl3(SO4)2(OH)6+
KAl3(SO4)2(OH)6+![]() S→
S→![]() K2SO4+
K2SO4+![]() Al2O3+
Al2O3+![]() ___________+
___________+![]() H2O
H2O
(3)从水浸后的滤液中得到K2 SO4晶体的操作a是 _____,写出K2SO4的一种用途 _____ .
(4)碱浸过程中发生的主要反应的离子方程式为____、 ____ 。
(5)流程中制Al的化学方程式为________________________
(6)现利用还原焙烧产生的SO2来生产硫酸。若明矾石的质量为41.4t,主要成分含量为50%,SO2的利用率为96%,则可生产质量分数为98%的硫酸____t。[KAl3(SO4)2(OH)6的相对分子质量为414]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com