
科目: 来源: 题型:
【题目】在隔绝空气的情况下,9.2 g铜、镁混合物溶解在一定量某浓度的稀硝酸中,当金属完全溶解后收集到标准状况下4.48 LNO气体。向反应后的溶液中加入足量的烧碱溶液,可生成氢氧化物沉淀的质量为
A.19.4 gB.18.6 gC.20 gD.24 g
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计如下实验装置探究硫酸与金属、非金属的反应、验证其产物,并探究随着反应的进行,硫酸性质发生的变化。根据实验要求回答相关问题:

F装置用于检验二氧化碳。供选择的试剂有:只含碳的生铁、18 mol·L-1的硫酸、品红溶液、无水硫酸铜粉未、酸性高锰酸钾溶液、氧化铜、澄清的石灰水、碱石灰。(供选择的试剂可重复使用)
(1)打开分液漏斗的活塞,A装置中发生的反应6H2SO4(浓)+2Fe![]() Fe2(SO4)3+6H2O↑+3SO2↑和(用化学方程式表示)_____,随反应的进行,硫酸的浓度变稀,又发生反应(用化学方程式表示)____
Fe2(SO4)3+6H2O↑+3SO2↑和(用化学方程式表示)_____,随反应的进行,硫酸的浓度变稀,又发生反应(用化学方程式表示)____
(2)B装置中的试剂是__________。
(3)E装置中的试剂是____________作用是______________。
(4)G装置中的试剂是__________,现象是______________。
(5)制备SO2的适宜药品为___________(填代号)。
①Na2SO3固体;②Na2SO3溶液;③20%硫酸;④70%硫酸;⑤铜片
(6)对SO2与氯水的反应进行探究。用注射器吸入一定量的饱和氯水和SO2,振荡,静置,再吸入少量品红溶液,发现品红溶液不褪色,用化学反应方程式解释其原因____________
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。

(1)实验室制取氨气选用图中a发生装置进行实验,反应的化学方程式为___________。实验室制取氨气选用图中b发生装置进行实验,反应的化学方程式为_________。

(2)B装置中的干燥剂可选用________(填“碱石灰”或“浓硫酸”)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是____(填“C”或“D”)。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________
(5)F装置中倒置漏斗的作用__________
(6)工业上硝酸的制备和自然界中的硝酸的生成既有相同的地方,又有区别。路线Ⅰ、Ⅱ、Ⅲ是雷电高能固氮过程中硝酸的生成途径:

写出①③步变化的化学方程式:
①____________;
③____________;
(7)将11.2 g的Mg-Cu混合物完全溶解于足量的硝酸中,收集反应产生的气体x(假定产生的气体全部逸出)。再向所得溶液中加入足量的NaOH溶液,产生21.4g沉淀。根据题意推断气体x的成分可能是______________。
A.0.3 mol NO2和0.3 mol NO B.0.2 mol NO2和0.1 mol N2O4
C.0.6 mol NO D.0.1molNO、0.2 mol NO2和0.05 mol N2O4
查看答案和解析>>
科目: 来源: 题型:
【题目】已知有机物A、B、C、D、E、F有以下转化关系。A的产量可以衡量一个国家的石油化工发展水平;E是不溶于水且具有香味的无色液体,相对分子质量是C的2倍;F为高分子化合物。结合如图关系回答问题:
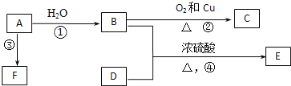
(1)写出C的结构简式:___________
(2)写出B、D中官能团的名称:B____________,D_____________.
(3)写出下列反应的化学方程式:
②____________
④____________
(4)有机化合物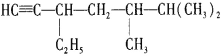 的名称是____________,将其在催化剂存在下完全与H2加成,所得烷烃的名称是___________
的名称是____________,将其在催化剂存在下完全与H2加成,所得烷烃的名称是___________
(5)相对分子质量为72且沸点最低的烷烃的结构简式为________
(6)乙醇的分子结构为: ,分子内脱水生成乙烯时,断开的键是______(填编号。下同);在铜催化作用下发生催化氧化反应时,断开的键是____;酯化反应时,断开的键是______
,分子内脱水生成乙烯时,断开的键是______(填编号。下同);在铜催化作用下发生催化氧化反应时,断开的键是____;酯化反应时,断开的键是______
查看答案和解析>>
科目: 来源: 题型:
【题目】取 1LFeCl3 溶液腐蚀铜板制作电路板,反应后在此残留液中慢慢加入铁粉,溶液中 Fe2+的浓度变化如图所示(加入固体引起的体积变化忽略不计),下列说法错误的是
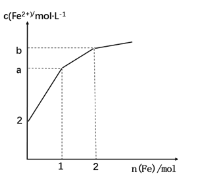
A.当n(Fe)=0.5mol 时,发生的离子反应为 Fe+2Fe3+=3Fe2+
B.当 n(Fe)=1.5mol 时,溶液中发生的总反应离子方程式为4Fe3++Cu2++3Fe=7Fe2++Cu
C.当n(Fe)=1mol 时,溶液中 c(Fe2+)=5 mol·L-1
D.腐蚀之前原溶液中n(Fe3+)=4 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列反应属于吸热反应的是_________________________
①铝粉与氧化铁粉末反应 ②酸碱中和反应 ③硝酸铵溶于水 ④碳酸钙分解 ⑤H2在Cl2中燃烧 ⑥灼热的碳与CO2的反应 ⑦NH4Cl晶体与Ba(OH)28H2O混合搅拌
(2)在25℃、101kPa的条件下,断裂1mol H—H键吸收436 kJ能量,断裂1 mol Cl—Cl键吸收243 kJ能量,形成1mol H—Cl键放出431 kJ能量。该条件下H2+Cl2=2HCl反应中的能量变化可用如图表示:
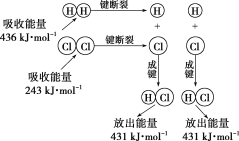
现有1 mol H2和1 mol Cl2在25℃、101 kPa下完全反应。请根据上述信息回答下列有关问题:
①该反应的热化学方程式为_____________
②反应物的总能量___________(填“>”或“<”)生成物的总能量。
(3)直接排放含SO2的烟气会形成酸雨,危害环境。工业上常采用催化还原法和碱吸收法处理SO2气体。如图所示:

1 mol CH4完全燃烧生成气态水的能量变化和1 mol S(g)燃烧的能量变化。在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式____________。
(4)几种含硅元素的物质之间的相互转化关系如图所示:
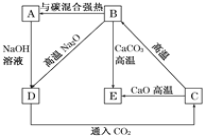
①写出下列反应的化学方程式:
B→A:_________;
B→E:_________。
②写出下列溶液中反应的离子方程式:D→C_________。
(5)Mg6Si4O10(OH)8用氧化物的形式可表示为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质中,满足表中图示物质在一定条件下能一步转化的组合有
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Al | AlCl3 | Al(OH)3 | Al2O3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A.①②③B.①③④C.①②④D.②③④
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示。下列叙述正确的是

A. 所用盐酸的浓度是0.09mol·L-1,NaOH溶液浓度为0.03mol·L─1
B. 在B点,溶液中离子浓度关系为:c(Cl─)>c(Na+)>c(OH-)>c(H+)
C. A、B、C三点水的电离程度大小依次为:A>B>C
D. 滴定前,锥形瓶用待测液润洗,导致盐酸浓度偏低
查看答案和解析>>
科目: 来源: 题型:
【题目】用石油和煤可以得到有机化工生产中需要的众多原料,例如由石油得到的乙烯和由煤得到的苯可制聚苯乙烯。生产过程如下:
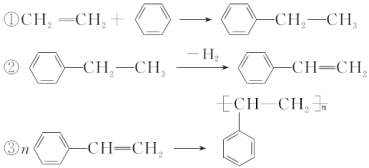
下列说法不正确的是( )
A. 通过裂解可以从石油中获得更多的乙烯
B. 通过煤的干馏不能直接得到纯净的苯
C. 制聚苯乙烯的反应①为加成反应
D. 反应①②③的原子利用率都达到了100%
查看答案和解析>>
科目: 来源: 题型:
【题目】对于苯乙烯的下列叙述
![]()
①能使酸性KMnO4溶液褪色;②可发生加聚反应;③可溶于水;④可溶于苯中;
⑤苯环能与溴水发生取代反应;⑥所有的原子可能共面,且最多有5个原子共线。其中完全正确的是
A. ①②④B. ①②④⑥C. ①②④⑤⑥D. ①②③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com