
科目: 来源: 题型:
【题目】(1)烃是一类重要的有机化合物,其结构与性质密切相关。
①下列有机化合物与甲烷互为同系物的是______(填字母) 。
a.乙烯 b.乙烷 c.乙炔
②下列试剂可用于鉴别乙烷和乙烯的是______(填字母) 。
a.水 b.四氯化碳 c.酸性KMnO4溶液
③下列有机化合物易溶于水的是________。
a..苯 b.乙烷 c.乙醇
(2) CH2=CH2、![]() 、CH3CH2OH、CH3COOCH2CH3、CH3COOH、葡萄糖,其中:
、CH3CH2OH、CH3COOCH2CH3、CH3COOH、葡萄糖,其中:
①能通过化学反应使溴水褪色的是____________。
②能发生水解反应的是____________。
③能与新制Cu(OH)2悬浊液反应生成砖红色沉淀的是____________。
(3)以淀粉为主要原料合成一种具有果香味的物质C合成路线如图所示。
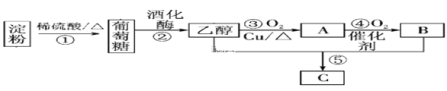
请回答下列问题:
①A的结构简式为____________,
②B分子中的官能团名称为________。
③反应⑤方程式___________________________;
(4)乙烯是石油化工的重要基础原料,工业上可由乙烯与水反应制乙醇,该反应类型为_______,其化学方程式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为实现随处可上网,中国发射了“中星16号”卫星。NH4ClO4是火箭的固体燃料,发生反应为2NH4ClO4![]() N2↑+Cl2↑+2O2↑+4H2O,NA代表阿伏加德罗常数,下列说法正确的是
N2↑+Cl2↑+2O2↑+4H2O,NA代表阿伏加德罗常数,下列说法正确的是
A.1 mol NH4ClO4溶于水含NH4+和ClO4-离子数均为NA
B.产生6.4g O2反应转移的电子总数为1.4NA
C.反应中还原产物分子数与氧化产物分子总数之比为3:1
D.0.5mol NH4ClO4分解产生的气体体积为44.8L
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物W可用作高分子膨胀剂,一种合成路线:
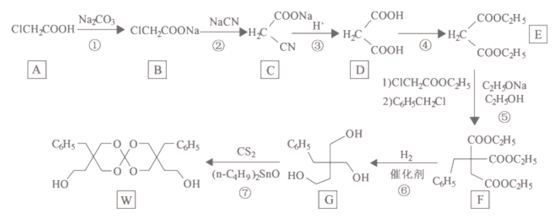
回答下列问题
(1)②的反应类型是________________。
(2)D的系统命名为____________________。
(3)反应④所需试剂,条件分别为__________________。
(4)G的分子式为___________,所含官能团的名称是_______________。
(5)写出与E互为同分异构体且满足下列条件的酯类化合物的结构简式__________(核磁共振氢谱为两组峰,峰面积比为1∶1)。
(6)苯乙酸苄酯(![]() )是花香型香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线___________________(无机试剂任选)。
)是花香型香料,设计由苯甲醇为起始原料制备苯乙酸苄酯的合成路线___________________(无机试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】I:已知:反应aA(g)+bB(g) ![]() cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
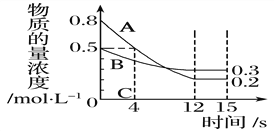
(1)经测定前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为_______________________
(2)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1; 乙:v(B)=0.12 mol·L-1·s-1; 丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为__________________(用甲、乙、丙表示)。
Ⅱ: 某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
氢气体积/mL | 50 | 120 | 224 | 392 | 472 | 502 |
(3)哪一时间段反应速率最大__(填0~1、1~2、2~3、3~4、4~5、5~6 min,下同),原因是_______________________________________________________
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是__________(填字母)
A.CH3COONa B.NaNO3溶液 C.KCl溶液 D.Na2CO3溶液
Ⅲ:(5)下列说法可以证明H2(g)+I2(g)![]() 2HI(g)已达平衡状态的是______________________
2HI(g)已达平衡状态的是______________________
A.单位时间内生成n mol H2的同时,生成n mol HI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=![]() v(HI)
v(HI)
E.温度和体积一定时,容器内压强不再变化
F.温度和体积一定时,混合气体的密度不再变化
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下反应2SO2(g)+O2(g)![]() 2SO3(g)在恒容密闭容器中进行,从反应开始至10s时,O2的浓度减少了0.3 mol·L-1。则0~10s内平均反应速率为
2SO3(g)在恒容密闭容器中进行,从反应开始至10s时,O2的浓度减少了0.3 mol·L-1。则0~10s内平均反应速率为
A. ![]()
B. ![]()
C. ![]()
D. ![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
I.CO2可以被NaOH溶液捕获,若所得溶液c(HCO3-)∶c(CO32-)=2∶1,溶液pH=_____。(室温下,H2CO3的K1=4×10-7;K2=5×10-11)
II.CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)
2CO(g)+2H2(g)
(1)已知上述反应中相关的化学键键能数据:
化学键 | C-H | C=O | H-H |
|
键能/kJ/mol | 413 | 745 | 436 | 1075 |
则该反应的ΔH=___________。分别在V L恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1 mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是___________(填“A”或“B”)。
(2)按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图1所示。此反应优选温度为900℃的原因是____________。
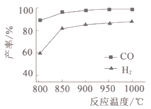
(3)在T1温度时,将CH4和CO2各1.0 mol充入2 L密闭恒容容器中,充分反应达到平衡后,若CH4转化率为40%,则
①容器内的压强与起始压强之比为___________;
②此温度下,若该容器中含有CH4、CO2、H2、CO各1.0 mol,则此时反应所处的状态为___________(填“向正反应方向进行中”“向逆反应方向进行中”或“平衡状态”)
③欲使甲烷的平衡转化率提高,应采取的措施是___________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
查看答案和解析>>
科目: 来源: 题型:
【题目】已知有机物 A、B、C、D、E、F、G 有如下转化关系,其中 C 的产量可用来衡量一个国家的石油化工发展水平,G 的分子式为 C9H10O2,试回答下列有关问题。
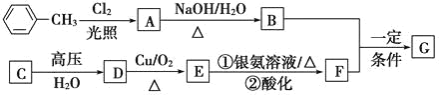
(1)G 的结构简式为_______。
(2)指出下列反应类型:B+F→G_________,
(3)写出下列反应的化学方程式:A→B:________________
(4)符合下列条件的 G 的同分异构体有____种
①苯环上有 3 个取代基,且有两个取代基相同;
②能够与新制的银氨溶液反应产生光亮的银镜。
其中共有四种不同化学环境氢原子的同分异构体的结构简式为__________、___________
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组同学对乙醛与新制的Cu(OH)2反应的实验进行探究。
实验Ⅰ:取2mL 10%的氢氧化钠溶液于试管中,加入5滴2%的CuSO4溶液和5滴5%的乙醛溶液,加热时蓝色悬浊液变黑,静置后未发现红色沉淀。
实验小组对影响实验Ⅰ成败的因素进行探究:
(1)探究乙醛溶液浓度对该反应的影响。
编号 | 实验Ⅱ | 实验Ⅲ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变红棕色,静置后底部有大量红色沉淀 | 加热,蓝色悬浊液变红棕色,静置后上层为棕黄色油状液体,底部有少量红色沉淀 |
已知:乙醛在碱性条件下发生缩合反应:CH3CHO+CH3CHO![]() CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
CH3CH=CHCHO+H2O ,生成亮黄色物质,加热条件下进一步缩合成棕黄色的油状物质。
① 能证明乙醛被新制的Cu(OH)2 氧化的实验现象是______。
② 乙醛与新制的Cu(OH)2 发生反应的化学方程式是______。
③ 分析实验Ⅲ产生的红色沉淀少于实验Ⅱ的可能原因:______。
(2)探究NaOH溶液浓度对该反应的影响。
编号 | 实验Ⅳ | 实验Ⅴ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,蓝色悬浊液变红棕色, 静置后底部有红色沉淀 |
依据实验Ⅰ→Ⅴ,得出如下结论:
ⅰ. NaOH溶液浓度一定时,适当增大乙醛溶液浓度有利于生成Cu2O。
ⅱ. 乙醛溶液浓度一定时,______。
(3)探究NaOH溶液浓度与乙醛溶液浓度对该反应影响程度的差异。
编号 | 实验Ⅵ | 实验Ⅶ |
实验方案 |
|
|
实验现象 | 加热,蓝色悬浊液变黑 | 加热,静置后底部有红色沉淀 |
由以上实验得出推论: ______。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组对m g无水三草酸合铁酸钾(K3[Fe(C2O4)3]]受热分解产物进行探究,并对所得气体产物和固体产物进行验证(查阅资料得知:三草酸合铁酸钾热分解的气体产物中含有CO和CO2)。利用如图装置进行实验(夹持仪器已略去)。
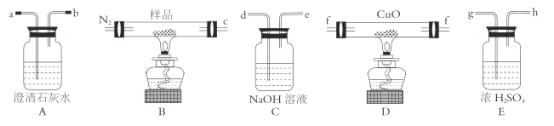
回答下列问题:
(1)按气流方向各装置依次连接的合理顺序为______;(填接口代号,装置可重复使用)
(2)反应开始前依次进行如下操作:组装仪器、_______、加药品、通氮气一段时间后点燃酒精灯。反应结束后的操作包括:①停止通氮气②熄灭酒精灯③冷却至室温。正确的顺序为___________________;
(3)通入氮气的目的是_____________________。
(4)实验中观察到第一个澄清石灰水变浑浊,则说明气体产物中有____________(写化学式)。能证明分解产物中有CO气体生成的实验现象是_________________。
(5)样品完全分解后,装置B中的残留物含有FeO和Fe2O3。
(6)测定三草酸合铁酸钾中铁的含量。
①将装置B中完全分解后的残留物置于锥形瓶中,溶解后加稀H2SO4酸化的x mol/LKMnO4溶液滴定至终点。滴定终点的现象是______。该过程发生反应的离子方程式为______。
②向上述溶液中加入过量KI-淀粉溶液,充分反应后,用y mol/LNa2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液V mL(已知I2+2S2O32-=2I-+S4O62-)。该晶体中铁的质量分数的表达式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】向0.1 mol/L二元弱酸H2A溶液中逐滴滴加0.1 mol/L NaOH溶液,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知![]() ]。下列叙述错误的是
]。下列叙述错误的是

A.lg[K1(H2A)]=-1.2
B.pH=2.7时,c(HA-)>c(H2A)=c(A2-)
C.0.05 mol/L的NaHA溶液中一定存在:c(Na+)>c(HA-)>c(A2-)>c(H2A)
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com