
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是()
A.Ca(HCO3)2溶液与少量NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
B.用铜作电极电解食盐水:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.向氧化铁中加入氢碘酸:Fe2O3+6H+=2Fe3++3H2O
D.向一定量明矾溶液中滴加Ba(OH)2溶液至生成沉淀的物质的量最多:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目: 来源: 题型:
【题目】某氨气燃料电池,如图所示,下列说法不正确的是
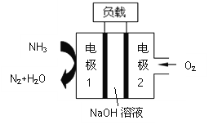
A.正极的电极反应式为O2+4e-+4H+=2H2O
B.电子流向:电极1→负载→电极2
C.Na+由左向右移动
D.NH3在电极1上发生氧化反应
查看答案和解析>>
科目: 来源: 题型:
【题目】关于小苏打水溶液的表述正确的是( )
A. 存在的电离平衡为HCO3-+H2O![]() H2CO3+OH-
H2CO3+OH-
B. c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
C. HCO3-的电离程度大于HCO3-的水解程度
D. c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,已知下列三种金属硫化物的溶度积常数(Ksp)分别为Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24。下列关于常温时的有关叙述正确的是( )
A. 硫化锌、硫化铜、硫化亚铁的溶解度依次增大
B. 将足量的ZnSO4晶体加入到0.1 mol·L-1的Na2S溶液中,Zn2+的浓度最大只能达到1.6×10-23mol·L-1
C. 除去工业废水中含有的Cu2+,可采用FeS固体作为沉淀剂
D. 向饱和FeS溶液中加入FeSO4溶液后,混合液中c(Fe2+)变大、c(S2-)变小,Ksp(FeS)变大
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.100g质量分数为17%的H2O2水溶液中含氧原子数目为NA
B.0.1molH2(g)与0.1molI2(g)于密闭容器中充分反应生成HI(g)后,其分子总数小于0.2NA
C.8.0gCH4与足量Cl2在光照下反应生成的HCl分子数最多为2NA
D.标准状况下,将54g铝片投入足量冷的浓硝酸中生成134.4LNO2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知下列热化学方程式:
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH=-24.8 kJ·mol-1
Fe2O3(s)+![]() CO(g)===
CO(g)===![]() Fe3O4(s)+
Fe3O4(s)+![]() CO2(g) ΔH=-15.73 kJ·mol-1
CO2(g) ΔH=-15.73 kJ·mol-1
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH=640.4 kJ·mol-1
则14gCO气体还原足量FeO固体得到Fe固体和CO2气体时对应的ΔH约为( )
A. -218 kJ·mol-1B. -109 kJ·mol-1
C. 218 kJ·mol-1D. 109 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】已知反应:A2(g)+2B2(g)![]() 2AB2(g) ΔH<0,下列说法正确的是( )
2AB2(g) ΔH<0,下列说法正确的是( )
A. 达到平衡后,升高温度有利于该反应平衡正向移动
B. 达到化学平衡时,v正(A2)=2v逆(B2)
C. 升高温度,正向反应速率增加,逆向反应速率减小
D. 达到平衡后,降低温度A2气体的转化率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】根皮素J (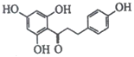 )是一种新型天然美白剂,主要分布于苹果、梨等多汁水果的果皮及根皮.其中一种合成J的路线如下:
)是一种新型天然美白剂,主要分布于苹果、梨等多汁水果的果皮及根皮.其中一种合成J的路线如下:
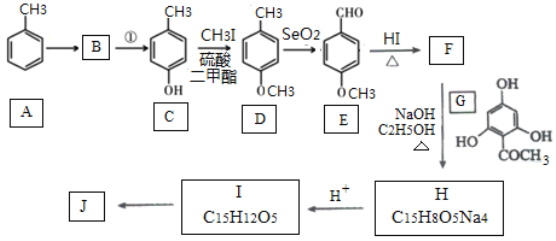
已知:
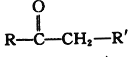 +R"CHO
+R"CHO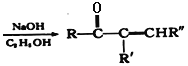 +H2O
+H2O
回答下列问题:
(1)C的化学名称是___________.E中官能团的名称为_______________.
(2)B为溴代烃,请写出A→B的反应试剂___________.
(3)写出由C生成D的反应类型___________
(4)F→H的化学方程式为______________________.
(5)M是E的同分异构体,同时符合下列条件的M的结构有___________种(不考虑立体异构)
①能与FeCl3溶液发生显色反应
②能发生银镜反应
(6)设计以丙烯和1,3-丙二醛为起始原料制备![]() 的合成路线_______(无机试剂任选).
的合成路线_______(无机试剂任选).
查看答案和解析>>
科目: 来源: 题型:
【题目】无水四氯化锡(SnCl4)是一种用途广泛的锡化工中间体,实验室可用熔融的锡(熔点231℃)与Cl2反应制备SnCl4,装置如图所示,请回答下列问题:
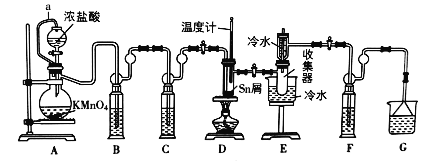
已知,SnCl4在潮湿的空气中极易水解生成SnO2xH2O。
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
(1)导管a的作用是______,装置A中发生反应的化学方程式为______。
(2)装置B、C、F、G中盛放的最佳试剂依次为______(填序号,试剂可重复使用),
①饱和Na2CO3溶液②NaOH溶液③浓H2SO4④饱和NaCl溶液⑤H2O
(3)点燃酒精灯前需要进行的一步操作是______。
(4)若撤去装置C,则D中发生的主要副反应化学方程式为______。
(5)得到的产物中常含有SnCl2,某实验小组用碘氧化法滴定分析产品中SnCl4的含量(Sn2++I2=Sn4++2I-)。准确称取该样品mg放入锥形瓶中,用少量浓盐酸溶解,再加水稀释,淀粉溶液作指示剂,用0.1molL-1碘标准溶液滴定至终点时锥形瓶内溶液颜色变化是______,若消耗标准液20.00mL,则产品中SnCl4的质量含量为______(用含m的代数式表示)
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是________,基态D原子价电子的轨道表达式为________________。
(2)DA2分子的VSEPR模型是____________。
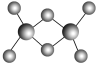
(3)实验测得C与氯元素形成的化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
①C2Cl6属于________(填晶体类型)晶体,其中C原子的杂化轨道类型为________杂化。
②[C(OH)4]-中存在的化学键有____________________________________________。
(4)单质A有两种同素异形体,其中沸点高的是__________ (填分子式),原因是______________________________________________________________
(5)D与E所形成化合物晶体的晶胞如图所示 。
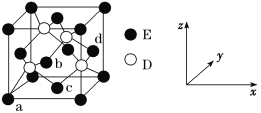
①在该晶胞中,E的配位数为________。
②原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为(1/2,0,1/2);c为(1/2,1/2,0)。则d的坐标参数为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com