
科目: 来源: 题型:
【题目】用下列实验装置和方法进行相应实验,能达到实验目的的是()
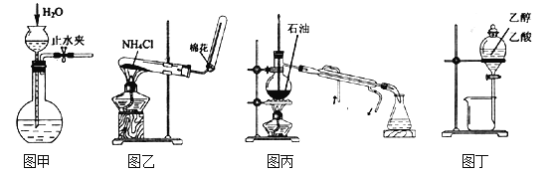
A. 用图甲所示方法检查装置的气密性
B. 用图乙所示装置制取氨气
C. 用图丙所示装置分馏石油获得汽油
D. 用图丁所示装置分离乙醇与乙酸
查看答案和解析>>
科目: 来源: 题型:
【题目】用于汽车刹车片的聚合物 Y 是一种聚酰胺纤维,合成路线如图:
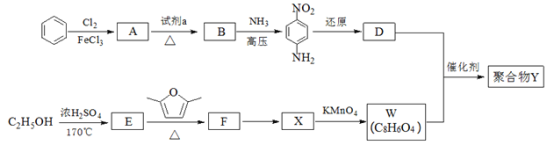
已知:![]()
(1)生成 A 的反应类型是_____。
(2)试剂 a 是_____。
(3)B 中所含的官能团的名称是_____。
(4)W、D 均为芳香化合物,分子中均只含两种不同化学环境的氢原子。
①F 的结构简式是_____。
②生成聚合物 Y 的化学方程式是_____。
(5)Q 是 W 的同系物且相对分子质量比 W 大 14,则 Q 有______种,其中核磁共振氢谱有4 组峰,且峰面积比为 1∶2∶2∶3 的为___________(写一种结构简式即可)。
(6)试写出由 1,3﹣丁二烯和乙炔为原料(无机试剂及催化剂任用)合成![]() 的合成路线__________________。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
的合成路线__________________。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2CO3是一种重要的化工原料,工业上生产Na2CO3的主要流程可表示如下:
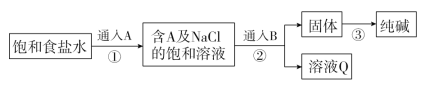
则下列说法中正确的是
A. A气体是CO2,B是NH3
B. ③中生成的CO2可循环使用,它可完全满足生产的需要
C. 通入B后的离子方程式为Na++NH3+CO2+H2O=NaHCO3↓+NH4+
D. 溶液Q的成分是NH4Cl,可通过降温结晶的方法使其析出
查看答案和解析>>
科目: 来源: 题型:
【题目】NaNO2是一种食品添加剂,过量摄入能致癌。酸性KMnO4 溶液与NaNO2反应的方程式是MnO4-+NO2-+![]() ―→Mn2++NO3-+H2O。下列叙述中正确的是
―→Mn2++NO3-+H2O。下列叙述中正确的是
A. 该反应中NO2-被还原
B. 反应过程中溶液的pH增大
C. 生成1 mol NaNO3需消耗0.2 mol KMnO4
D. ![]() 中的粒子是OH-
中的粒子是OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】下表列出了5种元素在周期表中的位置。
族 周期 | ⅠA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ |
(1)①的元素符号是_______,⑤的原子结构示意图是__________;
(2)以上元素中,非金属性最强的是___________(填元素符号);
(3)④元素的最高价氧化物对应的水化物呈______性(填“酸”或“碱”或“两”);
(4)③④⑤三种元素按原子半径由大到小的顺序是______(填元素符号);
(5)元素①与元素②的单质氧化性较强的是________(填化学式)。;
(6)元素④的最高价氧化物与元素③的最高价氧化物对应的水化物相互反应的化学方程式__。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是_________mol;
(2)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是____________,又变为棕黄色的原因是用离子方程式解释____________;
(3)在100mL FeBr2溶液中通入标况下2.24LCl2,溶液中有1/4的Br-被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】己知乙烯能发生以下转化:
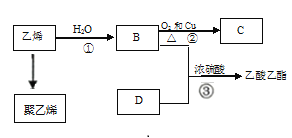
(1)写出化合物中的官能团的化学式或名称:B中所含官能团名称_;D中所含官能团化学式__;
(2)写出反应的化学方程式:
①_____________________, 反应类型:_____________;
②_____________________ , 反应类型:_____________;
③_____________________ , 反应类型:_____________;
查看答案和解析>>
科目: 来源: 题型:
【题目】铜及其合金是人类最早使用的金属材料。
(1)下图是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为___________。

(2)Cu2+能与NH3、H2O、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有_____________(填序号)。
A.配位键 B.金属键 C.极性共价键 D.非极性共价键 E.离子键
②[Cu(NH3)4]2+具有对称的空间构型,[Cu(NH3)4]2+中的两个NH3被两个Cl-取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___________。
(3)第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。
①H、C、N、O四种元素的电负性由小到大的顺序为_______________________。
②下列叙述不正确的是____________。(填字母)
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水
B.HCHO和CO2分子中的中心原子均采用sp2杂化
C.C6H6分子中含有6个![]() 键和1个大
键和1个大![]() 键,C2H2是非极性分子
键,C2H2是非极性分子
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式________________。
(4)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。与Fe原子或离子形成配合物的分子或离子应具备的结构特征是_________ 写出一种与 CN- 互为等电子体的单质分子式_______________________。
(5)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:
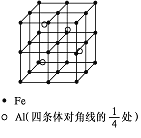
①确定该合金的化学式______________。
②若晶体的密度=ρ g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为__________cm。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组为了证明SO2和Cl2的漂白性,设计了如图所示的实验装置:
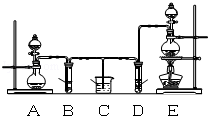
(1)他们制备Cl2依据的原理是:MnO2+4HCl(浓)△MnCl2+2H2O+Cl2↑,应选用图A、E装置中的 (填序号)制Cl2,反应中浓盐酸所表现出的性质是 、 .
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管中的液体加热,B试管中的现象是 .
(3)写出过量NaOH溶液与SO2气体反应的离子方程式是 .
(4)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色.查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】锌及锌的化合物应用广泛。例如,测定铜合金中的铅、锌时要利用锌配离子的下列反应:
[Zn(CN)4]2-+4HCHO+4H2O==Zn2++4HOCH2CN+4OH-,回答下列问题:
(1)基态Zn2+的电子排布式为_____________,基态 C原子核外电子占据_____个不同原子轨道。
(2)C、N、O三种元素的第一电离能由大到小的顺序为___________,HOCH2CN分子中含有的σ键与π键数目之比为_________。
(3)HCHO分子中碳原子轨道的杂化类型是________,福尔马林是HCHO的水溶液,HCHO极易与水互溶的主要原因是_________________________。
(4)[Zn(CN)4]2-中Zn2+与CN-之间的化学键称为_________,提供孤电子对的成键原子是________。
(5)Zn与S形成某种化合物的晶胞如图所示。
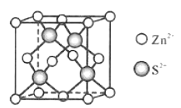
①Zn2+填入S2-组成的___________空隙中;
②已知晶体密度为d g/cm3,该晶胞的边长表达式为______pm(写计算表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com