
科目: 来源: 题型:
【题目】从海带中提取碘,可经过以下实验步骤完成。下列有关说法正确的是
![]()
A. 灼烧过程中使用的玻璃仪器有酒精灯、烧杯、玻璃棒
B. 氧化过程中发生反应的离子方程式为 2I-+H2O2 =I2+2OH-
C. 检验碘单质时,可选用淀粉碘化钾试纸,若试纸变蓝说明海带中含有碘单质
D. 分液时,先打开活塞放出下层液体,再关闭活塞从上口倒出上层液体
查看答案和解析>>
科目: 来源: 题型:
【题目】国际计量大会第26次会议修订了阿伏加德罗常数并于2019年5月20日正式生效(NA=6.02214076×1023mol-1),下列叙述正确的是 ( )
A.标准状况下,22.4LH2O含有的分子数为1 NA
B.常温常压下,16g O2含有的原子数为1 NA
C.通常状况下,1NA 个SO2分子占有的体积约为22.4L
D.物质的量浓度为0.5mol/L的K2SO4溶液中,含有SO42-个数为0.5 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. ![]() 分子中的所有原子有可能共平面
分子中的所有原子有可能共平面
B. ![]() 中有8个碳原子可能在同一条直线上
中有8个碳原子可能在同一条直线上
C. 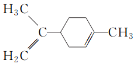 所有碳原子一定在同一平面上
所有碳原子一定在同一平面上
D. ![]() 至少有16个原子共平面
至少有16个原子共平面
查看答案和解析>>
科目: 来源: 题型:
【题目】甲溶液可能含有K+、Ca2+、NH4+、Cu2+、NO3-、Cl-、SO42-、CO32-八种离子中的若干种![]() 为确定甲溶液的组成,将其分成两等份,进行如下实验:
为确定甲溶液的组成,将其分成两等份,进行如下实验:
①向一份溶液中加入足量的NaOH浓溶液并加热,产生的气体在标准状况下体积为4.48L。
②向另一份溶液中加入0.6 mol/L的BaCl2溶液500mL,恰好可以与溶液中的离子完全反应,过滤得66.3g沉淀及滤液。
③向上述沉淀中加入过量的盐酸,产生的气体通入足量澄清的石灰水中,得到一定量的沉淀X。
④向上述滤液中加入1 mol/L AgNO3溶液650 mL,恰好可完全反应,据此,请回答下列问题![]() 用相应的离子符号表示
用相应的离子符号表示![]() :
:
⑴上述实验③中得到沉淀X的质量为______;生成沉淀X的离子方程式为______.
⑵甲溶液中一定不存在的离子是______;可能存在的离子是______.
⑶甲溶液一定存在的离子中,物质的量最大的离子是______;物质的量最小的离子是______,此物质的量最小的离子其物质的量为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】挥发性有机物(VOCs)对环境易造成污染,VOCs催化燃烧处理技术具有净化率高、燃烧温度低、无明火、不会有 NOz等二次污染物产生等优点。图甲是VOCs处理过程中固体催化剂的催化原理,图乙是反应过程中的能量变化图。下列叙述正确的是( )
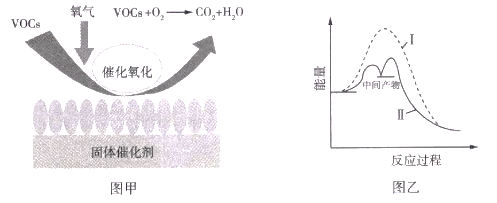
A.图甲中固体催化剂表面既有化学键断裂,也有化学键形成
B.图甲中固体催化剂可提高VOCs的平衡转化率
C.图乙中曲线II使用了固体催化剂,反应活化能降低
D.VOCs催化氧化过程中所有反应均为放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组利用硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)来制备FeCO3,其流程如图:
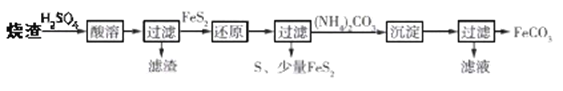
已知:①FeS2不溶于稀硫酸;②“还原”时,Fe3+通过两个反应被还原,其中一个反应为 FeS2+14Fe3++8H2O=15Fe2++2![]() +16H+ 。
+16H+ 。
下列说法不正确的是( )
A.“还原”时另一个反应的离子方程式为2Fe3++FeS2=2S+3Fe2+
B.“还原”后可以用KSCN检验Fe3+是否反应完全
C.流程中多次进行过滤,过滤所用的玻璃仪器为烧杯、漏斗、胶头滴管和玻璃棒
D.所得FeCO3需充分洗涤,可以用稀盐酸和BaCl2溶液检验FeCO3是否已洗涤干净
查看答案和解析>>
科目: 来源: 题型:
【题目】11.2L甲烷、乙烷、HCHO(g)组成的混合气体,完全燃烧后生成15.68LCO2(气体体积均在标准状况下测定),混合气体中甲烷的体积分数可能为
A. 40%B. 60%C. 70%D. 80%
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.按要求填空
(1)5.4gH2O物质的量为____________mol,约含有___________________个原子;
(2)已知1.204×1023个X气体的质量是6.4g。则X气体的摩尔质量是_________ g/mol;
(3)同温同压下,同体积的甲烷CH4和CO2质量之比为________,质子数之比_______;
(4)VLAl2(SO4)3溶液中含Al3+ag,该Al2(SO4)3溶液的物质的量浓度为_____mol/L,取出![]() L再加入水稀释到4VL。则稀释后溶液中SO42-的物质的量浓度是_____mol/L。
L再加入水稀释到4VL。则稀释后溶液中SO42-的物质的量浓度是_____mol/L。
Ⅱ.按要求书写下列反应的方程式
(1)亚硫酸氢钠电离方程式(NaHSO3)________________________________________________;
(2)醋酸溶液与NaHCO3溶液反应的离子方程式为________________________________;
(3)0.8molL﹣1NaHSO4与0.4molL﹣1Ba(OH)2溶液等体积混合,反应的离子方程式为___________;
(4)黑火药爆炸的化学方程式为________________________________。
Ⅲ.请配平以下化学方程式
(1)____FeSO4+____K2O2+____H2O =____ Fe(OH) 3+____ Fe2(SO4) 3+____KOH
(2)_____BiO3-+_____Mn2++____=_____Bi3++_____ MnO4- +____
查看答案和解析>>
科目: 来源: 题型:
【题目】氨气可有效消除NO2的污染,相关反应为8NH3+6NO27N2+12H2O,在1 L恒容密闭容器中,控制不同温度,分别加入0.50 mol NH3和1.2 mol NO2,测得n(NH3)随时间变化的有关实验数据如下表。
温度 n(NH3)/mol 时间/min | 0 | 10 | 20 | 40 | 50 |
T1 | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | 0.50 | 0.30 | 0.20 | … | 0.18 |
下列说法正确的是( )
A.T1温度下,0-20 min内,NO2的降解速率为0.0125 molL-1min-1
B.实验条件为T1<T2,且该反应为放热反应
C.40 min时,表格中T2对应的数据为0.20
D.0~10 min内,T1温度下NH3的降解速率大于T2温度下的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com