
科目: 来源: 题型:
【题目】人造空气(氧气与氦气的混合气)可用于减轻某些病痛或供深水潜水员使用。标准状况下,5.6 L“人造空气”的质量是2.4 g,其中氧气与氦气的质量比是( )
A. 1∶1 B. 2∶1 C. 1∶4 D. 2∶3
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 常温常压下,8g甲烷中含C-H键数目为0.4NA
B. 标准状况下,11.2LSO3中含分子数目为0.5NA
C. 1L0.1mol/LNH4NO3溶液中含氧原子数目为0.3NA
D. 7.8gNa2O2与足量CO2完全反应转移电子数目为0.1NA
查看答案和解析>>
科目: 来源: 题型:
【题目】用等体积的0.1mol/L的BaCl2 溶液,可使相同体积的Fe2 (SO4 )3 、Na2 SO4 、KAl(SO4)2 三种溶液中的SO42-完全沉淀,则三种硫酸盐的物质的量浓度之比为( )
A. 3:2:3 B. 3:1:2 C. 2:6:3 D. 1:1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,8 g O2含有4NA个电子
B.1 L 0.1 mol·L-1的氨水中有0.1NA个NH4+
C.标准状况下,22.4 L盐酸含有NA个HCl分子
D.1 mol Na被完全氧化生成Na2O2,失去2NA个电子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是()
A.将1 mol/L NaAlO2和1.5 mol/L的HCl等体积互相均匀混合:6AlO+9H++3H2O=5Al(OH)3↓+Al3+
B.NaHCO3溶液中加入过量的Ba(OH)2溶液:2![]() +Ba2++2OH-=BaCO3↓+2H2O
+Ba2++2OH-=BaCO3↓+2H2O
C.Fe(OH)3溶于HI溶液:Fe(OH)3+3H+=Fe3++3H2O
D.在过氧化氢里加入酸性的高锰酸钾:2![]() +3H2O2 + 6H+ =2Mn2+ + 4O2↑+ 6H2O
+3H2O2 + 6H+ =2Mn2+ + 4O2↑+ 6H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物c的制备原理如下:
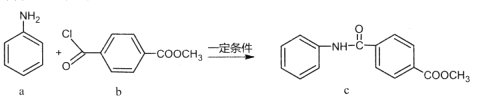
下列说法正确的是
A.该反应为加成反应B.化合物a中所有原子一定共平面
C.化合物C的一氯代物种类为5种D.化合物b、c均能与NaOH溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下.某同学进行CO2与Na2O2反应的探究实验(本实验所涉及气体休积均在相同状况下测定)。请回答下列问题:
(1)用下图装置制备纯净的CO2.
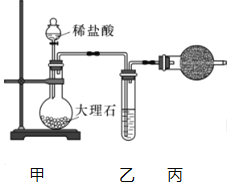
①丙装置的名称是_______,乙装置中盛装的试剂是_______.
②若CO2中混有HCl,则HCl与Na2O2发生反应的化学方程式为_________。
(2)按下图所示装置进行实验(夹持装置略)。
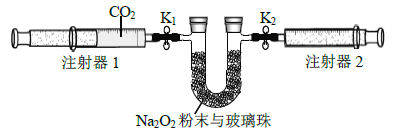
①先组装仪器.然后________.再用注射器1抽取100 mL纯净的CO2,将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。
②打开止水夹K1、K2,向右推动注射器1的活塞。可观察到的现象是________。
③实验过程中.需缓慢推入CO2,其目的是__________.为达到相同目的,还可进行的操作是__________________________。
(3)实验结束后,当注射器1的活塞推到底时,测得注射器2中气体的体积为65 mL。则CO2的转化率是_______________.
查看答案和解析>>
科目: 来源: 题型:
【题目】有八种短周期主族元素x、y、z、d、e、f、g、h,其中x、y、d、f随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。z、e、g、h的最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH与原子序数的关系如图2所示。
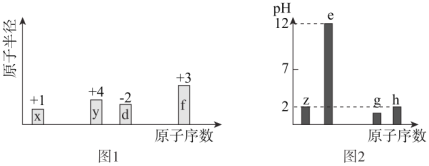
根据上述信息进行判断,并回答下列问题:
(1)g在元素周期表中的位置是______;
(2)比较d、e、f的简单离子半径大小为 < < (用离子符号表示)______;y、h的最高价氧化物对应水化物酸性较强的是______ (用化学式表示);
(3)下列可作为比较c和f金属性强弱的依据是______;
①测同温同压同浓度相应氯化物水溶液的pH
②测两种元素单质的硬度和熔、沸点
③比较单质作还原剂时失去的电子数目的多少
④比较两种元素在化合物中化合价的高低
⑤比较单质与同浓度盐酸反应的难易程度
(4)由上述元素中的y、z、e组成的某剧毒化合物eyz不慎泄露时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为______。已知eyz含有Z2分子中类似的化学键,写出化合物eyz的电子式___。
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是以植物细胞中半纤维素木聚糖为原料合成镇痛药品莫沙朵林(G)的路线:
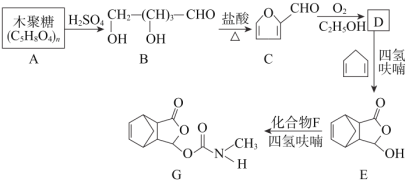
已知:①四氢呋喃(![]() )在流程中作反应的催化剂;
)在流程中作反应的催化剂;
②
③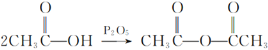
回答下列问题:
(1)B中官能团的名称为______;
(2)E→G的反应类型:______;
(3)D和F的结构简式分别是______、______;
(4)C与新制氢氧化铜反应的化学方程式为:______;
(5)写出同时满足下列条件的E的一种同分异构体的结构简式:______。
①分子中含有苯环②能发生银镜反应③能与FeCl3溶液发生显色反应
(6)有机物H(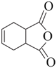 )是合成抗病毒药物阿昔洛韦的中间体。按上述合成路线,写出以1,3-丁二烯为原料制备
)是合成抗病毒药物阿昔洛韦的中间体。按上述合成路线,写出以1,3-丁二烯为原料制备![]() 的合成路线流程图______(无机试剂任选);
的合成路线流程图______(无机试剂任选);
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:用NH3催化还原NOx时包含以下反应.
反应①:4NH3 (g)+6NO(g) ![]() 5N2(g)+6H2O(l) H1=-1 807. 0 kJ·mol—1,
5N2(g)+6H2O(l) H1=-1 807. 0 kJ·mol—1,
反应②:4NH3(g)+6NO2(g) ![]() 5N2(g)+3O2(g)+6H2O(l) H2=?
5N2(g)+3O2(g)+6H2O(l) H2=?
反应③:2NO(g)+O2(g) ![]() 2NO2(g) H3=-113.0kJ·mol一1
2NO2(g) H3=-113.0kJ·mol一1
(1)反应②的H2==_____________。
(2)为探究温度及不同催化剂对反应①的影响.分别在不同温度、不同催化剂下.保持其他初始条件不变重复实验.在相同时间内测得N2浓度的变化情况如下图所示。
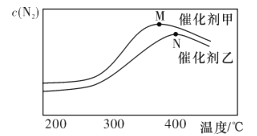
①反应①的平衡常数的表达式K=________。相同温度下.在催化剂甲的作用下反应的平衡常数______(填“大于”“小于”或“等于”)在催化剂乙的作用下反应的平衡常数。
②N点后N2浓度减小的原因可能是_____________________。
(3)某温度下,在1 L恒容密闭容器中初始投入4 mol NH3和6 mol NO发生反应①.当气体总物质的量为7.5mol时反应达到平衡.则NH3的转化率为____,达平衡所用时间为5 min.则用NO表示此反应0~5 min内的平均反应速率为______.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com