
科目: 来源: 题型:
【题目】用无机矿物资源生产部分材料,其产品流程示意图如下,下列说法正确的是( )

A. 制取粗硅时生成的气体产物为CO2
B. 生产铝、铜、高纯硅及玻璃的过程中都涉及氧化还原反应
C. 电解精炼铜时,当电路中转移0.2mol电子时阳极质量减轻6.4g
D. 粗硅制高纯硅时,提纯四氯化硅可用多次分馏的方法
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如下图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是
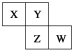
A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性Z比W强
C. Y的气态氢化物的稳定性较Z的弱
D. 四种元素的单质中,Z的熔、沸点最高
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸铵是一种常见的化肥,某工厂用石膏、NH3、H2O、CO2制备硫酸铵的工艺流程如下:
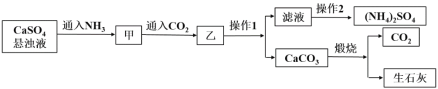
下列说法不正确的是
A. 操作1为过滤,操作2为蒸馏
B. 滤液中的主要阳离子可通过向少量滤液中加NaOH溶液,加热,并用湿润的红色石蕊试纸来检验
C. 甲到乙反应的离子方程式为CaSO4+2NH3+CO2+H2O==CaCO3↓+2NH4++ SO42-
D. 工艺流程中产生的CO2可循环利用
查看答案和解析>>
科目: 来源: 题型:
【题目】下图中a、b、c表示相应仪器中加入的试剂,可用如图装置制取、净化、收集的气体是( )
编号 | 气体 | a | b | c |
|
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
C | NO | 稀硝酸 | 铜屑 | H2O | |
D | NO2 | 浓硝酸 | 铜屑 | NaOH溶液 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】在一密闭容器中加入A和B,随着反应的进行,各物质的物质的量浓度变化如图所示。下列说法不正确的是
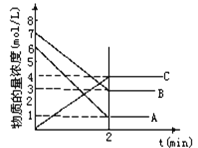
A.该反应的化学方程式为:5A+4B![]() 4C
4C
B.该反应达到平衡时,A、B、C的浓度比为5∶4∶4
C.用B的浓度变化表示2min内的速率为2 mol·L-1·min-1
D.2 min前,正反应速率逐渐减小,逆反应速率逐渐增大
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积。该小组设计的简易实验装置如图所示:
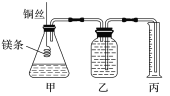
该实验的主要操作步骤如下:
①用已知浓度的浓盐酸配制100 mL 1.0 mol·L-1的盐酸(需要用到的仪器有:量筒、玻璃棒、烧杯、____________;
②用10 mL的量筒量取8.0 mL 1.0 mol·L-1的盐酸加入锥形瓶中;
③准确称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为___________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请回答下列问题:
(1)步骤①中,配制100 mL 1.0 mol·L-1的盐酸时,下列会使所配制溶液的浓度偏小的操作有_________(填字母)。
A.用量筒量取浓盐酸时,俯视量筒的刻度线
B.容量瓶未干燥即用来配制溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线未做处理
E.在容量瓶中定容时俯视容量瓶刻度线
F.烧杯中有少量水
G.未冷却至室温即定容
(2)请填写操作步骤中的空格:
步骤①:_________________________;
步骤③:________________________。
(3)实验步骤⑤中应选用的量筒规格是_______。
(4)读数时除需要恢复至室温外,还需要注意(回答一点即可):___________________________。
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=________L·mol-1。
查看答案和解析>>
科目: 来源: 题型:
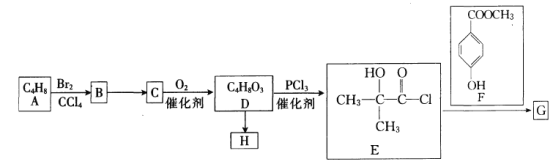
【题目】化合物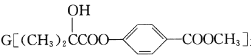 是一种医药中间体,它的一种合成路线如下:
是一种医药中间体,它的一种合成路线如下:
已知:![]() 。请回答下列问题:
。请回答下列问题:
(1)A的化学名称是______________,G的分子式为____________________。
(2)由B生成C的反应条件为____________,由E和F生成G的反应类型是___________。
(3)D在浓硫酸/加热条件下会反应生成一种含六元环的化合物,该化合物的结构简式为______________。
(4)H是一种高聚酯。D生成H的化学方程式为__________________________________。
(5)符合下列要求的F的同分异构体共有___________种。
①苯环上有三个取代基;②能发生银镜反应;③1mol该物质能与2molNa2CO3反应。
请写出其中能与足量浓溴水反应,所得产物的苯环上不存在氢原子的F的同分异构体结构简式:_______________________(任写一种)。
(6)已知酚羟基不易与羧酸发生酯化反应,写出以苯酚、甲苯为原料制备苯甲酸苯酯![]() 的合成路线(其他无机试剂任选):____________。
的合成路线(其他无机试剂任选):____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以MnO2、KClO3、CaCO3及盐酸等为原料制取KMnO4的步骤如下:
Ⅰ.MnO2的氧化![]()
Ⅱ.CO2的制取![]()
Ⅲ.K2MnO4的歧化及过滤和结晶等
回答下列问题:
(1)实验前称取2.5g KClO3、5.2g KOH、3.0g MnO2并充分混合。氯酸钾需过量,其原因是____________________________;熔融时除了需要酒精灯、三脚架、坩埚钳、细铁棒及铁坩埚外,还需要的硅酸盐质仪器有___________________
(2)为了体现“绿色化学”理念,某同学设计了如图所示的“K2MnO4歧化”实验装置。在大试管中装入块状CaCO3,并关闭K2,向长颈漏斗中加入一定量6mol·L-1的盐酸;向三口烧瓶中加入K2MnO4溶液。
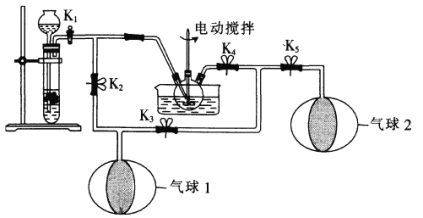
①实验时,不用装置(a)(启普发生器)制取CO2而用装置(b)制取,这是因为______。
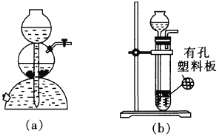
②为了充分利用CO2,实验开始时需关闭____________(填“K1”“K2”“K3”“K4”或“K5”,下同),其余均打开;待“气球1”中收集到足够多的CO2时,关闭______,其余均打开。
③三口烧瓶中物质发生反应生成KMnO4的同时还会生成MnO2和K2CO3,该反应的离子方程式为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I.下图是抚州市某儿童微量元素体检报告单的部分数据:
抚州市某医疗机构临床检验结果报告单 | ||||
分析项目 | 检测结果 | 单位 | 正常值参考范围 | |
1 | 锌(Zn) | 109.62 | μmol/L | 66-120 |
2 | 铁(Fe) | 5.92↓ | mmol/L | 7.52-11.82 |
3 | 钙(Ca) | 1.68 | mmol/L | 1.55-2.10 |
…… | ||||
根据上表的数据,回答下列问题:
(1)该儿童_____元素含量偏低。
(2)报告单中“μmol/L”是__________(填“质量”、“体积”或“浓度”)的单位。
(3)服用维生素C可使食物中的Fe3+转化为Fe2+。在这个过程中体现维生素C的________(填“氧化性”或“还原性”)。
II. 高铁酸钾(K2FeO4,铁元素为+6价)是一种新型、高效、多功能绿色水处理剂,无二次污染。制备高铁酸钾的离子反应方程式为:___Fe(OH)3+__ClO-+___OH- = ___FeO42-+___Cl-+ __H2O
回答下列问题:
(4)配平该离子方程式。
(5)每生成1molFeO42-转移的电子数为___________,若反应过程中转移了0.3mo1电子,则还原产物的物质的量为________mo1。
查看答案和解析>>
科目: 来源: 题型:
【题目】明矾[KA1(SO4)2·12H2O]是一种复盐,在造纸等方面应用广泛。采用废易拉罐制备明矾的过程如下图所示。
下列叙述错误的是
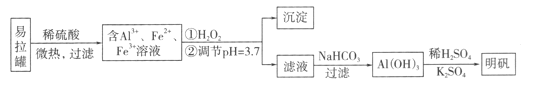
A. 合理处理易拉罐有利于环境保护和资源再利用
B. 从易拉罐中可回收的金属元素有Al、Fe
C. “沉淀”反应的金属离子为Fe3+
D. 上述流程中可用NaHSO4代替NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com