
科目: 来源: 题型:
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气![]() 进行此实验,所用仪器如图:
进行此实验,所用仪器如图:
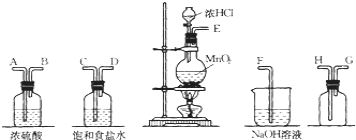
![]() 连接上述仪器的正确顺序是:____________。
连接上述仪器的正确顺序是:____________。
![]() 气体发生装置中进行的反应化学方程式是 ______ ;当
气体发生装置中进行的反应化学方程式是 ______ ;当![]() 参与反应时,被氧化的HCl的质量为 ______ 。
参与反应时,被氧化的HCl的质量为 ______ 。
![]() 在装置中:
在装置中:![]() 饱和食盐水的作用是 ______。
饱和食盐水的作用是 ______。
![]() 化学实验中检验是否有
化学实验中检验是否有![]() 产生常用湿润的淀粉
产生常用湿润的淀粉![]() 试纸
试纸![]() 如果有
如果有![]() 产生,可观察到的现象是 ______ ,写出反应方程式 ______ 。
产生,可观察到的现象是 ______ ,写出反应方程式 ______ 。
![]() 写出尾气吸收装置中进行的反应的化学方程式 ______ 。
写出尾气吸收装置中进行的反应的化学方程式 ______ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据如图所示实验装置,回答下列问题:
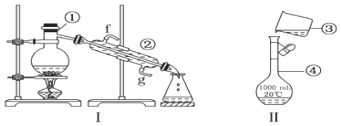
![]() 写出下列仪器的名称:
写出下列仪器的名称:![]() ______;
______;
![]() 若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器有______,将仪器补充完整后进行的实验操作的名称为______;
若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器有______,将仪器补充完整后进行的实验操作的名称为______;![]() 的进水口是______
的进水口是______![]() 填f或
填f或![]()
![]() 某同学用装置Ⅱ配制
某同学用装置Ⅱ配制![]() NaCl溶液,指出图中的错误操作______.
NaCl溶液,指出图中的错误操作______.
查看答案和解析>>
科目: 来源: 题型:
【题目】控制、治理氮氧化物对大气的污染是改善大气质量的重要方法。回答下列与雾霾治理有关的问题:
Ⅰ.(1)在催化剂作用下,甲烷可还原氮氧化物,从而达到治理氮氧化物污染的目的。已知:①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1;②4NO2(g)+2N2(g)= 8NO(g) ΔH=+586 kJ·mol-1。则CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) ΔH=________ kJ·mol-1。
(2)工业烟气中的氮氧化物可用NH3催化还原,反应原理如图所示。

其中X为一种无毒的气体,则NH3催化还原氮氧化物的化学方程式为______。
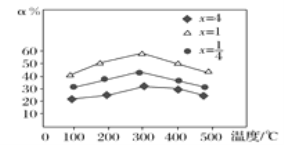
(3)用NH3催化还原烟气中的氮氧化物时,当![]() =x,用Fe作催化剂时,在NH3充足的条件下,不同x值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图所示,当x=_____时,脱氮效果最佳,最佳的脱氮温度是____ ℃。
=x,用Fe作催化剂时,在NH3充足的条件下,不同x值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图所示,当x=_____时,脱氮效果最佳,最佳的脱氮温度是____ ℃。
Ⅱ.(4)甲醇是一种绿色燃料,甲醇的工业合成方法较多,如CO(g)+2H2(g)![]() CH3OH(g)。在2 L恒容密闭容器中充入1 mol CO和2 mol H2混合原料气,充分反应达到平衡,测得平衡时混合物中CH3OH的体积分数与压强、温度的关系如图所示。
CH3OH(g)。在2 L恒容密闭容器中充入1 mol CO和2 mol H2混合原料气,充分反应达到平衡,测得平衡时混合物中CH3OH的体积分数与压强、温度的关系如图所示。
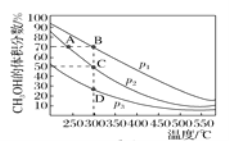
①图中压强p1、p2、p3的大小关系是_______。
②C点平衡常数K=___,A、B、D三点的平衡常数K(分别用KA、KB、KD表示)的大小关系是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】元素周期表中钌(Ru)与铁相邻位于铁的下一周期,某钌光敏太阳能电池的工作原理如下图所示,图中RuII*表示激发态。下列说法正确的是

A. 电池工作时,直接将太阳能转化为电能
B. 理论上,n(被还原的I3-):n(被氧化的Ru II*)=1:2
C. 在周期表中,钌位于第五周期第ⅧB族
D. 电池工作时,正极的电极反应式为Ru3++e-=Ru2+
查看答案和解析>>
科目: 来源: 题型:
【题目】某科研人员提出HCHO(甲醛)与O2在羟基磷灰石(HAP)表面催化生成H2O的历程,该历程示意图如下(图中只画出了 HAP的部分结构):

下列说法不正确的是
A. HAP能提高HCHO与O2的反应速率
B. HCHO在反应过程中,有C-H键发生断裂
C. 根据图示信息,CO2分子中的氧原子全部来自O2
D. 该反应可表示为:HCHO+O2![]() CO2+H2O
CO2+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】制备金属钾的反应:Na+KCl ![]() K+NaCl,有关沸点的数据如下:
K+NaCl,有关沸点的数据如下:
物质 | K | Na | KCl | NaCl |
沸点(°C) | 759 | 883 | 1420 | 1465 |
下列说法不正确的是
A.该反应说明,Na的金属性强于K
B.850°C时,钾蒸气逸出,平衡正向移动,KCl转化率增大
C.升温至900°C,收集金属钾,钾的纯度会降低
D.金属钾中含有杂质钠,可通过真空蒸馏的方法分离提纯
查看答案和解析>>
科目: 来源: 题型:
【题目】如图装置甲是某可充电电池的示意图,该电池放电的化学方程式为2K2S2+KI3=K2S4+3KI,图中的离子交换膜只允许K+通过,C、D、F均为石墨电极,E为铜电极。工作一段时间后,断开K,此时C、D两电极产生的气体体积相同,E电极质量减少 1.28 g。

(1)装置甲的A电极为电池的__极,电解质的K+向__(填“左侧”或“右侧”)迁移;B电极的电极反应式为____。
(2)装置乙中D电极析出的气体是___,体积为____mL(标准状况)。
(3)若将装置丙中的NaCl溶液改换成FeCl2和FeCl3的混合溶液。从反应初始至反应结束,丙装置溶液中金属阳离子物质的量浓度与转移电子的物质的量的变化关系如图所示。
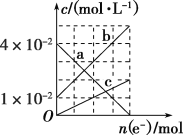
①图中b表示的是_____(填金属离子符号)的变化曲线。
②反应结束后,若用0.5 mol·L-1NaOH溶液沉淀丙装置溶液中的金属阳离子(设溶液体积为100 mL),则至少需要0.5 mol·L-1NaOH溶液______mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】将1 mol N2和 3 mol H2充入体积可变的恒温密闭容器中,在380 ℃下发生反应:N2(g)+3H2(g)![]() 2NH3(g),平衡时,体系中氨的体积分数
2NH3(g),平衡时,体系中氨的体积分数![]() (NH3)随压强变化的情况如下表:
(NH3)随压强变化的情况如下表:
压强/MPa | 10 | 20 | 30 | 40 |
| 0.30 | 0.45 | 0.54 | 0.60 |
下列说法正确的是( )
A.10 MPa时,H2的转化率为75%
B.20 MPa时,NH3的物质的量浓度是10 MPa时的1.5倍
C.40 MPa时,若容器的体积为V L,则平衡常数K=![]()
D.30 MPa时,若向容器中充入惰性气体,则平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4molA和 2molB进行如下反应:3A(g)+2B(g)![]() 4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6molC,则下列说法正确的是( )
4C(s)+2D(g)。反应一段时间后达到平衡,测得生成1.6molC,则下列说法正确的是( )
A.该反应的化学平衡常数表达式是 K=![]()
B.此时,B的平衡转化率是40%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.增加 B,平衡向右移动,B的平衡转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com