
科目: 来源: 题型:
【题目】已知白磷和P4O6的分子结构如图所示,又知化学键的键能是形成(或断开)1 mol化学键时释放(或吸收)的能量,现查知P—P键能为198 kJ·mol-1、P—O键能为360 kJ·mol-1、O===O键能为498 kJ·mol-1。若生成1 mol P4O6,则反应P4(白磷)+3O2=P4O6中的能量变化为( )
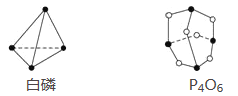
A. 吸收1 638 kJ能量 B. 放出1 638 kJ能量
C. 吸收126 kJ能量 D. 放出126 kJ能量
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据物质的量的相关公式,完成下列问题。(注意书写单位)
(1)3.01×1023个NH3分子的物质的量__。
(2)0.5molH2SO4含有的氧原子的物质的量__。
(3)2.3gNO2的物质的量__。
(4)标况下,33.6LN2的物质的量___。
(5)0.5mol /LK2SO4溶液中,c(K+)=__。
查看答案和解析>>
科目: 来源: 题型:
【题目】G是合成某新型药物的中间体,下图是合成 G的部分流程:
已知:

乙酸酐的结构简式为![]()
请回答下列问题:
(1)G 中含氧官能团的名称是_______、________。
(2)反应 A→B 的化学方程式为________________。
(3)有机物 F的结构简式为_________________。
(4)反应 ④、⑤的反应类型分别是_________、___________。
(5)写出满足下列条件的 C 的同分异构体的结构简式______________________。
Ⅰ.苯环上只有两种取代基
Ⅱ.分子中只有 4 种不同化学环境的氢原子
Ⅲ.能与NaHCO3溶液反应生成 CO2
(6)以乙酸酐和![]() 为原料,制备
为原料,制备![]() 的部分流程图如下。请结合相关信息和已学知识,将合成路线补充完整(无机试剂任选)。
的部分流程图如下。请结合相关信息和已学知识,将合成路线补充完整(无机试剂任选)。
![]() ______________
______________
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单的二苯乙炔类化合物是![]() 。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:

回答下列问题:
(1)A的分子式为________;
(2)D中含有的官能团是________,分子中最多有________个碳原子共平面;
(3)①的反应类型是________,③的反应类型是________;
(4)⑤的化学方程式为________;
(5)B的同分异构体中能同时满足如下条件:a.苯环上有两个取代基,b.能发生银镜反应,共有______种(不考虑立体异构),其中核磁共振氢谱为5组峰,且峰面积比为6∶2∶2∶1∶1的是________(写结构简式);
(6)参照上述合成路线,设计一条由苯乙烯和甲苯为起始原料制备![]() 的合成路线:___。(其他试剂任用)(合成路线常用的表示方法:起始原料A
的合成路线:___。(其他试剂任用)(合成路线常用的表示方法:起始原料A![]() B……
B……![]() 目标产物)。
目标产物)。
查看答案和解析>>
科目: 来源: 题型:
【题目】钠、铝、铁是三种重要的金属。请回答:
(1)三种金属与同浓度盐酸反应,反应最慢的是___(填选项)。
a.钠 b.铝 c.铁
(2)金属钠与水发生反应的离子方程式为___;(填选项)
a.2Na +2H2O=2NaOH+H2↑
b.2Na+2H2O=2Na++2OH-+H2↑
c.2Na +2H2O=2Na++2OH-+O2↑
(3)可观察到的实验现象正确的是__(填选项)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(4)填写a、b、c化学式并书写①的化学方程式(a、b、c均为含Al化合物);
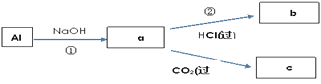
a:___,b:___,c:___;
①____________;
(5)Fe跟Cl2在一定条件下反应,所得产物为___。
(6)将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成__色。
b.向另一支试管中滴加NaOH溶液,产生__色沉淀。
查看答案和解析>>
科目: 来源: 题型:
【题目】铁被称为“第一金属”,铁及其化合物在生产、生活中有广泛用途。
(1)铁原子外围电子轨道表示式为____________________,铁原子核外电子发生跃迁时会吸收或释放不同的光,可以用_________摄取铁元素的原子光谱。
(2)FeCoOx是一种新型光电催化剂。第四电离能大小关系是I4(Co)____I4(Fe)(填“>”或“<” ) ,原因是_____________。
(3)二茂铁[(C5H5)2Fe]可用作火箭燃料添加剂、汽油抗爆剂。二茂铁熔点172℃,沸点249 ℃,易升华,难溶于水,易溶于有机溶剂,它属于_____________晶体。
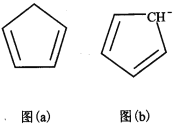
(4)环戊二烯(C5H6)结构如图(a),可用于制二茂铁。环戊二烯中碳原子的杂化方式为________。分子中的大π键可用符号![]() 表示,其m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,环戊二烯负离子(C5H5―)结构如图(b),其中的大π键可以表示为_________________。
表示,其m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,环戊二烯负离子(C5H5―)结构如图(b),其中的大π键可以表示为_________________。
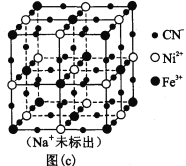
(5)某普鲁士蓝类配合物可作为新型钠离子电池电极材料。它由Na+、Ni2+、Fe3+和CN―构成,其晶胞结构如图(c)。该物质中,不存在________(填标号)。A.离子键 B. σ键 C. π键 D. 氢键 E. 金属键
(6)该晶胞中Fe3+采用的堆积方式与_______(选填Po、Na、Mg、Cu)相同,单个晶胞的配位空隙中共容纳_____个 Na+。
查看答案和解析>>
科目: 来源: 题型:
【题目】现用Na2SO4固体来配制480mL0.2mol·L-1的Na2SO4溶液。可供选择的仪器如图:
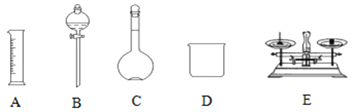
(1)如图所示的仪器中配制溶液不需要的是__ (填选项),配制上述溶液还需用到的玻璃仪器是___、__ (填仪器名称)。
(2)使用容量瓶之前必须进行的操作是___。(填选项)
A.检查气密性 B.检查是否漏水 C.烘干
(3)经计算,需Na2SO4的质量为___g。
(4)你选用的容量瓶规格为___mL。
(5)配制溶液时,一般可分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其操作顺序:②→__→__→__→__→__→__(填序号)。___
(6)在配制过程中,其他操作都准确,定容时俯视刻度线会使所配溶液浓度__(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】请回答下列问题
Ⅰ.离子反应及离子方程式的书写在高中化学学习中占有重要的地位。电解质在水溶液中发生的反应一般是离子反应。
(1)现有下列几种物质:①盐酸 ②石墨 ③四氯化碳 ④SO2 ⑤熔融KHSO4 ⑥氨水 ⑦金属铜 ⑧NaHCO3晶体 ⑨氧化钙。这些物质中能导电的有_______;属于电解质的有_______________;属于非电解质的是_________(以上均填序号)。
(2)写出下列反应的离子方程式
①碳酸镁与稀硫酸反应_________________________________________________
②硫酸氢钠与氢氧化钠溶液反应_________________________________________
③向烧碱溶液中通入少量CO2气体:______________________________________
④向澄清石灰水中滴加足量的碳酸氢钠溶液:________________________________
⑤铝与氢氧化钠溶液反应:________________________________
⑥硫酸铝溶液与足量氨水反应:________________________________
Ⅱ.某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中,肯定存在的离子是_______,有关离子方程式为_________
(3)取(2)中的滤液,加入过量的NaOH,出现白色沉淀,说明原溶液中肯定有______________,有关的离子方程式为________________________________
(4)原溶液可能大量存在的阴离子是下列的__________
A.Cl- B.NO3- C.CO32- D.OH-
Ⅲ.实验室中,制取Fe(OH)3胶体的离子方程式是______________________________,
证明胶体已经制成的方法是_______________________________________________。
Ⅳ.检测人的血液中葡萄糖(简称血糖,分子式为C6H12O6,相对分子质量为180)含量,参考指标常以两种计量单位表示,即“mmol/L”和“mg/dL”(1 L=l0dL)。以“mmol/L”表示时,人的血糖正常值在3.6~6.0 mmol/L之间。如果以“mg/dL”表示,血糖正常值范围是__________________
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲酸是一种重要的化工产品,某学习小组设计方案制备苯甲酸。反应原理如下:C6H5-CH3+2KMnO4![]() C6H5-COOK+KOH+2MnO2↓+H2O,C6H5-COOK+HCl→C6H5-COOH+KCl,已知甲苯的熔点为-95℃,沸点为110.6℃,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4℃,在25℃和95℃下溶解度分别为0.3g和6.9g。
C6H5-COOK+KOH+2MnO2↓+H2O,C6H5-COOK+HCl→C6H5-COOH+KCl,已知甲苯的熔点为-95℃,沸点为110.6℃,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4℃,在25℃和95℃下溶解度分别为0.3g和6.9g。
(制备产品)30.0mL甲苯和25.0mL1mol/L高锰酸钾溶液在80℃下反应30min,装置如图所示:
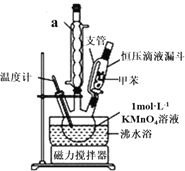
(1)仪器a的名称是___,图中支管的作用是______;
(2)相对于用酒精灯直接加热,用沸水浴加热的优点是_____,在本实验中,三颈烧瓶最合适的容积是___(填字母);
A.50mL B.100mL C.200mL D.250mL
(分离产品)他们设计如下流程分离粗产品苯甲酸和回收甲苯:

(3)操作Ⅰ的名称是____;含杂质的产物经操作Ⅱ进一步提纯得无色液体A,则操作Ⅱ的名称是_____;
(4)操作Ⅲ的名称是_____,固体B中可能会有________杂质离子,检验该离子的方法是_________;提纯B所用的方法是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以石油化工产品为原料合成聚酯类功能高分子材料R及某药物合成原料E的一种合成路线如下(部分反应条件和产物略去):
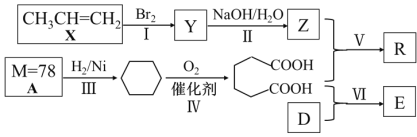
已知D与乙醇属于同系物,E在核磁共振氢谱上有3组峰且峰面积比为2∶2∶3。请回答下列问题:
(1)Y的名称是____;Z的官能团名称是____;A的分子式是__________ ;
(2)反应Ⅳ的反应类型是_____;
(3)写出X发生加聚反应的化学方程式________;
(4)写出II反应的化学方程式_____________;
(5)写出Ⅵ反应的化学方程式___________;
(6)写出由Z和乙二酸在浓硫酸的作用下反应生成的一种六元环状化合物的键线式____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com