
科目: 来源: 题型:
【题目】影响化学反应速率的因素很多,某化学小组用实验的方法进行探究。
I.探究活动一:
备选药品:铁片、锌片、0.5mol/LH2SO4、1.5mol/LH2SO4、18.4mol/LH2SO4
甲同学研究的实验报告
实验步骤 | 现象 | 结论 |
①分别取等体积的1.5mol/L的硫酸于两支试管中; ②_____________________。 | 反应速率: 锌>铁 | 金属的性质越活泼,反应速率越快 |
(1)甲同学实验报告中的实验步骤②为__________________________________。
(2)甲同学的实验目的是_______________________________;要得出正确的实验结论,还需控制的实验条件是__________________。
乙同学为了定量研究浓度对化学反应速率的影响,利用如图所示装置进行实验:

(3)乙同学在实验中需要测定的数据是_________________________。
(4)乙同学不会选用___________mol/L硫酸完成该实验,理由是_________________。
II.探究活动二:
备选药品:0.1mol/LNa2S2O3溶液、0.2mol/LNa2S2O3溶液、0.1mol/LH2SO4溶液、0.2mol/LH2SO4溶液。
已知:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O
实验 编号 | Na2S2O3用量 | H2SO4用量 | 温度(℃) |
① | 0.1mol/L5mL | 0.1mol/L5mL | 10 |
② | 0.2mol/L5mL | 0.2mol/L5mL | 25 |
③ | 0.1mol/L5mL | 0.1mol/L5mL | 25 |
④ | 0.1mol/L5mL | 0.1mol/L5mL | 40 |
(1)若想探究温度对化学反应速率的影响,可选的实验编号有___________。
(2)若想探究浓度对化学反应速率的影响,可选的实验编号有___________。
(3)在该实验过程中,需要观察和记录________________,来比较化学反应速率的快慢。
(4)Na2S2O3在碱性溶液中可被I2氧化为Na2SO4,写出该反应的离子方程式___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知用甲醇制乙烯、丙烯等烯烃时,在温度为400 ℃时,发生的主反应为2CH3OH![]() C2H4+2H2O、3CH3OH
C2H4+2H2O、3CH3OH![]() C3H6+3H2O,副反应为2CH3OH
C3H6+3H2O,副反应为2CH3OH![]() CH3OCH3+H2O。乙烯和丙烯的选择性(转化的甲醇中生成乙烯和丙烯的百分比)及丙烯对乙烯的比值(Cat.1和Cat.2代表两种等量的催化剂)如图所示,下列说法不正确的是
CH3OCH3+H2O。乙烯和丙烯的选择性(转化的甲醇中生成乙烯和丙烯的百分比)及丙烯对乙烯的比值(Cat.1和Cat.2代表两种等量的催化剂)如图所示,下列说法不正确的是
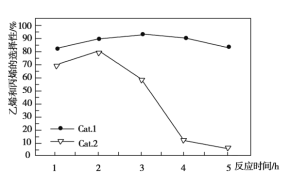
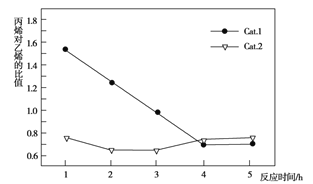
A. 使用Cat.2反应2小时后乙烯和丙烯的选择性下降
B. 使用Cat.1反应3小时后产生的烯烃主要是乙烯
C. 使用Cat.2反应3小时内产生的烯烃主要是丙烯
D. 使用Cat.1时乙烯和丙烯的选择性一直高于使用Cat.2时
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,向A和B中都充人2molX和2molY,起始VA=0.8a L,VB=a L保持温度不变,在有催化剂的条件下,两容器中各自发生下列反应:X(g)+Y(g)![]() 2Z(g)+W(g)达到平衡时,VA=0.9a L,则下列说法错误的是 ( )
2Z(g)+W(g)达到平衡时,VA=0.9a L,则下列说法错误的是 ( )
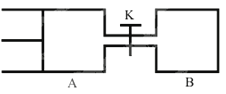
A. 两容器中达到平衡的时间A<B
B. 打开K达到新平衡后,升高B容器温度,A容器体积相比原平衡状态时一定增大
C. A容器中X的转化率为25%,且比B容器中的X的转化率小
D. 打开K一段时间达平衡时,A的体积为0.8a L(连通管中的气体体积不计)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对古文献记载内容理解错误的是
A. 《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无沙黏土而为之”。“瓦”,传统无机非金属材料,主要成分为硅酸盐。
B. 《本草纲目》“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也”。这里所用的“法”是指蒸馏。
C. 《抱朴子·金丹篇》中记载:“丹砂烧之成水银,积变又还成丹砂”。该过程未发生氧化还原反应。
D. 《本草经集注》中关于鉴别硝石(KNO3)和朴硝(Na2SO4)的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了焰色反应。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家研制了一种新型的高比能量锌-碘溴液流电池,其工作原理示意图如下。图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是

A. 放电时,a电极反应为
B. 放电时,溶液中离子的数目增大
C. 充电时,b电极每增重![]() ,溶液中有
,溶液中有![]() 被氧化
被氧化
D. 充电时,a电极接外电源负极
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(气)+3B(气)![]() 2C(气)+2D(固)达到平衡的标志的是( )
2C(气)+2D(固)达到平衡的标志的是( )
①C的生成速率与C的分解速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④A、B、C的分压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦A、B、C、D的分子数之比为1:3:2:2
A.②⑦B.②⑤⑦C.①③④D.②⑤⑥⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用。为探究氯气的性质,某同学设计了如图1所示的实验装置。
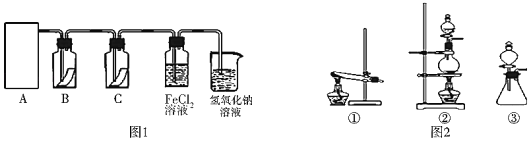
(1)实验中制取氯气的反应原理为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,该反应中还原剂是_____,还原产物是_____
MnCl2+Cl2↑+2H2O,该反应中还原剂是_____,还原产物是_____
(2)利用(1)中制气原理,从图2中选择合适的制气装置(A处):_____(填写序号)。
(3)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,理论上装置_____中的红色布条退色,但实验过程中该同学发现装置B、C中的布条均退色,其原因可能是_____,说明该装置存在明显的缺陷,请提出合理的改进方法_____
(4)为了验证氯气的氧化性,将氯气通入FeCl2溶液中,写出氯气与FeCl2溶液反应的离子方程式_____
(5)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是_____(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属及其化合物在人类生产、生活中发挥着重要的作用
(1)钠、铝、铁三种金属元素所形成的各种氧化物中具有强氧化性的是_____(填化学式,下同),适宜做耐火材料的是_____
(2)若Na2CO3粉末中混有少量 NaHCO3杂质,最适宜的除杂方法是_____,反应的化学方程式_____
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入铁粉,其原因是_____(用离子方程式表示)
(4)Na2O2可用作呼吸面具中的供氧剂写出有关反应的化学方程式_____
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用勒夏特列原理(平衡移动原理)解释的是
①铁在潮湿的空气中容易生锈
②二氧化氮与四氧化氮的平衡体系,加压缩小体积后颜色加深
③实验室可用排饱和食盐水的方法收集氯气
④钠与氯化钾共融制备钾 Na(l)+KCl(l)![]() K(g)+NaCl(l)
K(g)+NaCl(l)
⑤开启啤酒瓶后,瓶中马上泛起大量泡沫
A. ③④ B. ①② C. ①⑤ D. ①②⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】某反应进行过程中,各物质物质的量的变化情况如图所示。下列说法正确的是
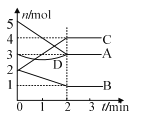
A. C、D是生成物
B. 反应的方程式为2A + B![]() 2C
2C
C. 2 min后各物质的量不再变化
D. 该反应不是可逆反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com