
科目: 来源: 题型:
【题目】铁是人体不可缺少的微量元素,硫酸亚铁晶体(FeSO4·7H2O)在医疗上常用作补血剂。某课外活动小组为测定该补血剂中铁元素的含量,设计如下实验。
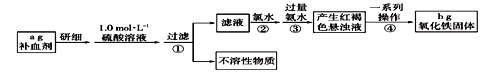
(1)实验时用18.4 mol·L-1的浓硫酸配制100mL1.0 mol·L-1的硫酸溶液,所需浓硫酸的体积为______mL(保留一位小数)。
(2)步骤①过滤后的滤液中加入氯水后发生反应的离子方程式为__________________________。
(3)向滤液中直接加入过量氨水时,生成的白色沉淀迅速变为灰绿色,最后变为红褐色,沉淀颜色变化的原因用化学方程式表示为_______________________。
(4)该补血剂中铁元素的质量分数为____________,若步骤③加入氨水的量不足,则实验结果_____(填“偏大”、“偏小”、“无影响”)
(5)科学研究表明服用含硫酸亚铁的补血剂时,同时服用维生素C有利于铁元素的吸收。则维生素C在其过程中的作用是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上可用铁盐溶液溶解黄铁矿(主要成分为FeS2),发生如下过程。下列说法错误的是
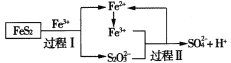
A.过程I每溶解120 g FeS2,理论上消耗6 mol Fe3+
B.过程Ⅱ每生成1 mol SO42-转移8 mol e-
C.总反应为FeS2+14Fe3++8H2O=2SO42-+15Fe2++16H+
D.反应过程中鼓入大量的空气有利于反应的进行
查看答案和解析>>
科目: 来源: 题型:
【题目】十九大报告中提出“打赢蓝天保卫战”,对污染防治要求更高。某种利用垃圾渗透液实现发电、环保二位一体结合的装置示意图如下。当该装置工作时,下列说法正确的是
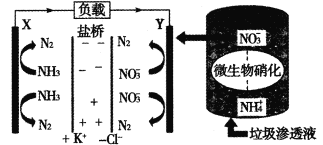
A.盐桥中Cl-向Y极移动
B.电路中流过7.5 mol电子时,共产生N2的体积为44.8 L(标况)
C.电流由X极沿导线流向Y极
D.Y极发生的反应为2NO3-+10e-+6H2O=N2↑+12OH-,周围pH增大
查看答案和解析>>
科目: 来源: 题型:
【题目】N2(g)与H2(g)在一定条件下反应生成NH3(g),过程如下图,下列说法正确的是
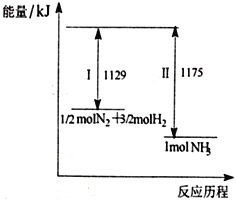
A. I为放热过程、Ⅱ为吸热过程
B. 1/2 molN2和3/2molH2的键能之和大于1 mol NH3的键能
C. 1/2molN2和3/2molH2所具有的能量之和低于1 mol NH3所具有的能量
D. 该过程的热化学反应方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92 kJ/mol
2NH3(g) ΔH=-92 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应中绚丽的颜色变化往往展现了化学的神奇,体现了化学之美。下列变化中的a、b、c、d可以是混合物,关于物质类别或者反应类型的叙述一定正确的是
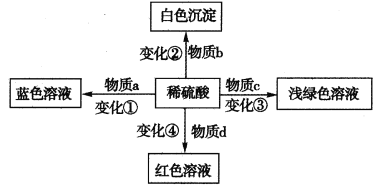
A.变化①一定不属于氧化还原反应
B.变化②得到的白色沉淀一定是硫酸盐
C.物质c中一定不能含有铁红或磁性氧化铁
D.物质d可能是某有机物的水溶液
查看答案和解析>>
科目: 来源: 题型:
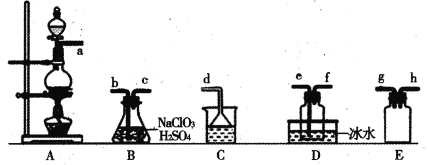
【题目】二氧化氯(C1O2)是易溶于水且不与水反应的黄绿色气体,沸点为11℃。某小组在实验室中制备C1O2的装置如下:[已知:SO2+2NaC1O3+H2SO4=2C1O2+2NaHSO4]
下列说法正确的是
A.连接装置时,导管口a应接h或g,导管口c应接e
B.装置C中装的是饱和食盐水,导管口a通过的气体为SO2
C.装置D放冰水的目的是液化SO2,防止污染环境
D.可选用装置A,用1 mol·L-1盐酸与MnO2反应制取Cl2
查看答案和解析>>
科目: 来源: 题型:
【题目】今有如下3个热化学方程式:H2(g)+![]() O2(g)= H2O(g) △H=a kJ/mol,H2(g)+
O2(g)= H2O(g) △H=a kJ/mol,H2(g)+ ![]() O2(g)= H2O(l) △H=b kJ/mol,2H2(g) +
O2(g)= H2O(l) △H=b kJ/mol,2H2(g) + ![]() O2(g)= 2H2O(l) △H=c kJ/mol,关于它们的下列表述正确的是:
O2(g)= 2H2O(l) △H=c kJ/mol,关于它们的下列表述正确的是:
A.它们都是吸热反应B.a、b、c均为正值C.a=bD.c=2b
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组的同学在学习了二氧化碳与过氧化钠的反应后,对过氧化钠与二氧化硫的反应进行实验探究。
(1)提出假设:
假设1. 固体产物是Na2SO3
假设2. _________________________
假设3. 固体产物是Na2SO3和Na2SO4的混合物。
(2)实验验证:用如图所示装置对上述假设进行实验。
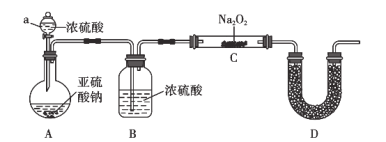
(1)仪器a的名称为__________,装置A中发生反应的化学方程式为:________________________。
(2)装置B的作用为________________________,装置D中试剂的名称为________。
(3)装置C中固体完全反应后,得到白色固体,进行如下实验。
实验操作 | 预期现象与结论 |
步骤1.取少量白色固体于试管中,加入足量的稀盐酸,将生成的气体通入品红溶液。 | 若_____________,说明白色固体中含有Na2SO3。 |
步骤2.在步骤1反应后的溶液中加入________ | 若_____________,说明白色固体中含有Na2SO4。 |
通过实验探究发现上述两个实验现象均有,则说明假设3正确。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了研究物质的性质和用途,需要对物质进行分离与提纯。根据下列信息回答问题。
(1)要从氯化钠和纯碱的混合物中分离出纯碱晶体可采取的方法是_______(填代号)
a.溶解,过滤 b. 溶解,蒸发结晶,过滤 c. 溶解,蒸发浓缩,降温结晶

(2)某同学设计的分离CO2和CO混合气体的实验。装置如图所示:

关闭b,打开a,混合气体通过该装置时,先得到的气体是_________,然后进行的操作是________________________,得到的气体是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知磷酸分子(![]() )中的三个氢原子都可与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。则下列说法正确的是
)中的三个氢原子都可与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能与D2O发生氢交换。则下列说法正确的是
A.H3PO2在水溶液中发生电离:H3PO2![]() H++H2PO2-、H2PO2-
H++H2PO2-、H2PO2-![]() H++HPO22-
H++HPO22-
B.H3PO4属于三元酸、H3PO2属于二元酸
C.NaH2PO2属于酸式盐,其水溶液呈酸性
D.H3PO2具有较强的还原性,其结构式为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com