
科目: 来源: 题型:
【题目】1L稀硝酸和稀硫酸的混合液,其物质的量浓度分别为0.1mol/L和0.4mol/L。若向该混合溶液中加入足量的铜粉,从离子反应的角度分析,则最多能溶解铜粉的质量为( )
A. 9.6gB. 6.4 gC. 3.2 gD. 2.4 g
查看答案和解析>>
科目: 来源: 题型:
【题目】黄铁矿(主要成分FeS2)、黄铜矿(主要成分CuFeS2)均是自然界中的常见矿物资源。
(1)Stumm和Morgan提出黄铁矿在空气中氧化的四步反应如题20图-1所示:
① a反应中每生成1molFeSO4转移电子的物质的量为___mol。
② d反应的离子方程式为_______________。
(2)用细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高浸取速率,其原理如题20图-2
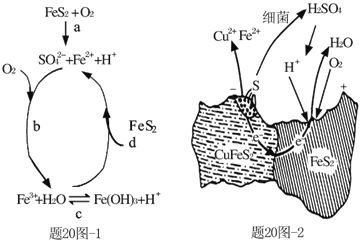
①冶炼过程中,正极周围溶液的pH___(选填:“增大”、“减小”或“不变”)
②负极产生单质硫的电极反应式为___。
这里,否则就错了!!阅后删除! |
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见下表),其相关反应的平衡常数的对数值与温度的关系如题20图-3。
相关反应 | 反应热 | 平衡常数K |
FeS2(s) + H2(g) | ΔH1 | K1 |
1/2 FeS2(s) + H2(g) | ΔH2 | K2 |
FeS(s) + H2(g) | ΔH3 | K3 |
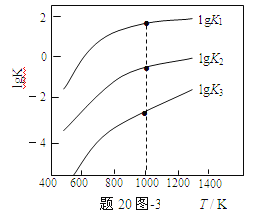
①上述反应中,ΔH1___0(选填:“>”或“<”)。
②提高硫的脱除率可采取的措施有___(举1例)。
③1000K时,平衡常数的对数lgK1、lgK2和lgK3之间的关系为___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法正确的是
A.马口铁(镀锡铁皮)镀层破损后铁仍不易腐蚀
B.CH3Cl(g)+Cl2(g)![]() CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0
CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0
C.MnS悬浊液中滴加少量CuSO4溶液可生成CuS沉淀,则Ksp(CuS)< Ksp(MnS)
D.合成氨生产中将NH3液化分离,一定能加快正反应速率,提高H2的转化率
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①过量Na2O2投入到CuCl2溶液中
②过量Ba(OH)2溶液和硫酸铝溶液混合
③少量Ca(OH)2投入过量NaHCO3中
④澄清石灰水中通入少量CO2
⑤CaCl2与NaOH的混合溶液中通入过量CO2
A.全部B.①⑤C.②③④D.②③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)25 ℃时,将体积Va、pH=a的某一元强碱与体积为Vb、pH=b的某二元强酸混合。
①若所得溶液的pH=11,且a=13,b=2,则Va∶Vb=____________。
②为了更好的表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG的定义为AG=lg![]() 。25 ℃时,若溶液呈中性,则AG=___,溶液的pH与AG的换算公式为AG=_____。
。25 ℃时,若溶液呈中性,则AG=___,溶液的pH与AG的换算公式为AG=_____。
(2)常温下,浓度均为0.1molL-1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①上述盐溶液中的阴离子,结合H+能力最强的是____。
②根据表中数据,浓度均为0.01 molL-1的下列四种酸的溶液分别稀释100倍,pH变化最大的是__(填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(3)已知常温下,Ksp[Fe(OH)3]=4.0×10-38,在FeCl3溶液中加入NaHCO3溶液产生沉淀和气体,反应的离子方程式为:_______;若将所得悬浊液的pH调整为4,则溶液中Fe3+浓度为__mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法.保持污水的pH在5.0- 6.0 之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体有吸附性,可吸附污物而沉积下来,具有净水作用.模拟处理装置如图所示,下列说法正确的是
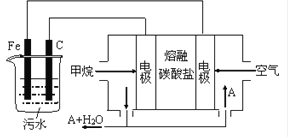
A.该燃料电池负极的电极反应式为CH4-8e-+10OH-=CO32-+7H2O
B.工作时熔融盐中的CO32-移向正极
C.该电解池中Fe极的电极反应式为: 2H++2e-=H2↑
D.为使电池长时间稳定工作必须有部分A物质参与循环,则A为CO2
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A. 常温常压下,2.24 L H2O中含有极性共价键的数目为0.2NA
B. 0.1 mol·L-1NH4Cl溶液中含有NH![]() 的数目小于0.1NA
的数目小于0.1NA
C. 100 mL 12 mol·L-1的浓HNO3与过量Cu反应转移电子的数目为0.6NA
D. 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】对Al、Fe二种金属元素,下列说法正确的是
A. 铝能够稳定存在于空气中,而铁很容易生锈,说明铁比铝活泼
B. 等物质的量的Al、Fe分别与足量盐酸反应放出等质量的H2
C. 二者的氢氧化物都不可以通过氧化物化合反应直接制备
D. 二者的单质都能与强碱溶液反应生成H2
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中:按CO2与H2的物质的量之比为1:3进行投料,发生反应2CO2(g)+6H2(g)![]() CH3CH2OH(g)+3H2O(g) △H<0,在5MPa 下测得不同温度下平衡体系中各种物质的体积分数 ( V% ) 如图所示,下列说法中正确的是
CH3CH2OH(g)+3H2O(g) △H<0,在5MPa 下测得不同温度下平衡体系中各种物质的体积分数 ( V% ) 如图所示,下列说法中正确的是
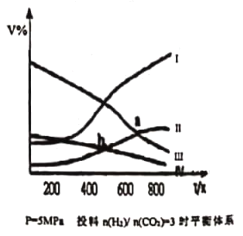
A.表示CH3CH2OH组分的曲线是IV
B.图中曲线交点a、b 对应的上述反应平衡常数Ka > Kb
C.图中曲线交点a 对应的 CO2 转化率为 40%
D.若甲、乙两个密闭容器起始时的容积、温度及投料方式均相同,甲:恒温恒压,乙;恒温恒容,反应达平衡时CH3CH2OH产率:甲<乙
查看答案和解析>>
科目: 来源: 题型:
【题目】下列变化不可能通过一步反应直接完成的是
A. Al(OH)3 → Al2O3 B. Al2O3 → Al(OH)3
C. Al → AlO2- D. Al3+ → Al(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com