
科目: 来源: 题型:
【题目】2019年诺贝尔化学奖已授予约翰·班宁斯特·古迪纳夫、斯坦利·惠廷汉姆和吉野彰,三位科学家的获奖理由是为锂电池的发展做出了卓越贡献。下图是我国一项电解制备金属锂的新方法发明专利装置图。下列说法不正确的是
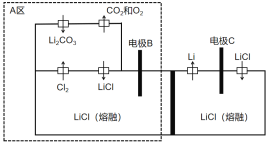
A.电极B的电势比电极C高
B.理论上该装置不需要补充电解质LiCl
C.电极B中氯离子和碳酸根离子放电
D.A区避免熔融碳酸锂对设备的腐蚀且减少了环境污染
查看答案和解析>>
科目: 来源: 题型:
【题目】外循环三相反应器连续制备高锰酸钾新技术是目前高锰酸钾工业发展的主要方向。该法以软锰矿(主要成分为MnO2)为原料生产高锰酸钾。该工艺路线制备高锰酸钾如下:

![]()
已知:一些化合物溶解度(单位:g)随温度的变化如表
温度℃ | KMnO4 | KCl | K2CO3 |
20 | 6.4 | 34.0 | 52.5 |
90 | 45.2 | 56.7 | 60.9 |
回答下列问题:
(1)原料软锰矿与氢氧化钾按一定的比例在“进料”时加热熔融后再和氧气进行“反应”,“进料”前应将软锰矿粉碎,其作用是____。
(2)“反应”中发生反应的化学方程式为____。
(3)将K2MnO4转化为KMnO4的生产有两种工艺。
①“CO2歧化法”是传统工艺,即向溶液中通入CO2气体,使体系呈中性或弱碱性。
K2MnO4发生歧化反应时,能否用盐酸代替CO2____(请填写“能”或“不能”)。待锰酸钾全部歧化后,静置一段时间后过滤。从滤液中得到高锰酸钾晶体的操作是:____。
②“电解法”为现代工艺,即电解K2MnO4水溶液,电解槽中阳极发生的电极反应为____,电解产物____可以循环利用。
③“CO2歧化法”和“电解法”相比较,K2MnO4的理论利用率之比为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】为了避免NO、NO2、N2O4对大气的污染,常采用NaOH溶液进行吸收处理(反应方程式:2NO2+2NaOH===NaNO3+NaNO2+H2O;NO2+NO+2NaOH===2NaNO2+H2O)。现有由a mol NO、b mol NO2、c mol N2O4组成的混合气体恰好被V L NaOH溶液吸收(无气体剩余),则此NaOH溶液的物质的量浓度为( )
A. ![]() mol·L-1 B.
mol·L-1 B. ![]() mol·L-1
mol·L-1
C. ![]() mol·L-1 D.
mol·L-1 D. ![]() mol·L-1
mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】药物阿比朵尔具有很好的抗病毒活性,其合成路线如下:
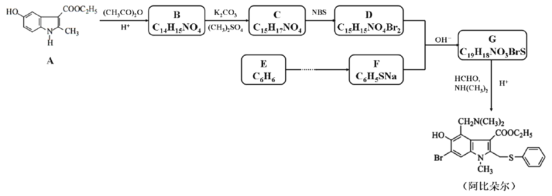
已知:①![]() +HCHO+
+HCHO+
![]()

②RX![]() RLiX
RLiX![]() RSH
RSH
请回答:
(1)下列说法正确的是___________。
A.化合物A能发生加成、取代和氧化反应,不发生还原反应
B.化合物B具有弱碱性
C.化合物D与FeCl3溶液发生显色反应
D.阿比朵尔的分子式是C22H25N2O3BrS
(2)写出化合物D的结构简式___________。
(3)写出G→阿比朵尔的化学方程式___________。
(4)设计从E→F的合成路线(用流程图表示,无机试剂任选)___________。
(5)写出化合物A同时符合下列条件的同分异构体的结构简式___________。
①1H-NMR谱和IR谱检测表明:分子中共有4种氢原子,含氮氧单键和碳氧双键;
②含有苯环和含氮五元杂环,且两环共棱连接。
查看答案和解析>>
科目: 来源: 题型:
【题目】将3. 84 g铜粉与一定质量浓硝酸反应,当铜完全作用时,溶液中的NO3-减少0.1mol,则所消耗硝酸的物质的量是
A.0.1 molB.0.11 molC.0.16 molD.0.22 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】乙酰基二茂铁常用作火箭燃料添加剂、汽油抗爆剂等。某兴趣小组制备乙酰基二茂铁,流程如下:

已知:
a.反应原理:![]() +(CH3CO)2O
+(CH3CO)2O![]() CH3COOH+
CH3COOH+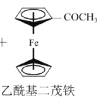
b.二茂铁熔点173℃,沸点249℃,100℃易升华。
c.乙酰基二茂铁熔点81℃,沸点163℃。不溶于水,易溶于有机溶剂。
请回答:
(1)步骤I,在50 mL圆底烧瓶中,加入新制的、经提纯后0.5 g二茂铁,5 mL乙酸酐,在振摇下滴入1 mL 85%磷酸,提纯二茂铁的方法为_______________。
(2)步骤II,加料毕,用装填有CaCl2的干燥管塞住圆底烧瓶瓶口。如图所示,其目的是__________。

(3)步骤IV,反应完毕后,将紫色混合物倾入含40 g碎冰烧杯中,并用10 mL冷水洗涤烧瓶,将洗涤液并入烧杯,在搅拌下加入NaHCO3(s),判断溶液呈中性的实验方法为__________。
(4)步骤V,包括结晶、吸滤、洗涤、干燥等多步操作。下列说法正确的是__________。
A.为较快地析出晶体,可以用玻璃棒摩擦烧杯内壁
B.吸滤装置由吸滤瓶、布氏漏斗、抽气泵组成
C.宜用乙醇洗涤,洗涤后乙醇易挥发
D.可在100℃红外灯下干燥
(5)①粗产品中含有杂质为___________,可以用来鉴别的仪器是___________。
②分离提纯粗产品后,用薄层层析来测定Rf值。选出其正确操作并按序列出字母:a→c→_______→_______→________→_________→g。
a.制备薄层色谱板
b.用少量纯二茂铁和提纯后的产品分别溶于2 mL甲苯中,配成浓溶液
c.用细玻璃管拉制两根微量滴管(尖端处约0.7mm)
d.将色谱板插入盛有乙醚的槽内,盖上盖子
e.待溶剂上升到色谱板3/4高度时,取出色谱板,并标记溶剂所到高度
f.分别用微量滴管浸入两浓溶液,在色谱板两原点处点样,待干燥后,再重复点样
g.计算Rf值
查看答案和解析>>
科目: 来源: 题型:
【题目】碳在冶金工业上具有重要用途。已知氧与碳的反应主要有:
Ⅰ.C(s)+O2(g)CO2(g) △H1=-394kJ·mol-1
Ⅱ.2C(s)+O2(g)2CO(g) △H2=-221kJ·mol-1
Ⅲ.2CO(g)+O2(g)2CO2(g) △H3
上述反应的△G~T如图所示,且满足△G=△H-T△S。
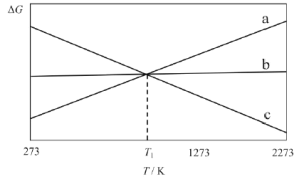
请回答:
(1)曲线a代表反应_________(填“I”、“II”或“III”),理由是__________。
(2)研究发现,以CO2替代高温水蒸气作为煤气化反应(H2O与C反应)的气化剂,实现了CO2零排放的新工艺。写出反应IV的热化学方程式___________(碳的计量数为1)。在1273K时,测得碳转化率[α(C)]与时间t变化如图所示。保持其它条件不变,请画出1773K时α(C)~t关系图______。
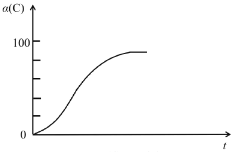
(3)当T=T1时,反应IV处于平衡状态,下列关于反应IV的说法正确的是_________。
A.因平衡时△G=0,若△H变化173.3kJ·mol-1,△S变化173.3J·K-1·mol-1,计算得T1=1000K
B.T<T1时,反应向逆反应方向移动
C.当碳的浓度不再变化时,一定处于平衡状态
D.因平衡常数K的值不再变化,反应达到了平衡
(4)当T=1273K时,仅存在CO、CO2两种气体,且维持总压为1 atm,此时反应IV的Kp=112,则CO气体所占的分压p(CO)为___________atm。(列式即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】乙二酸,又称草酸,通常在空气中易被氧化而变质。其两分子结晶水(H2C2O4·2H2O)却能在空气中稳定存在。在分析化学中常用H2C2O4·2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是
A.草酸是二元弱酸,其电离方程式为H2C2O4![]() 2H++C2O
2H++C2O![]()
B.草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂
C.乙二酸可通过乙烯经过加成、水解、氧化再氧化制得
D.将浓H2SO4滴加到乙二酸上使之脱水分解,分解产物是CO2和H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.2-丁烯不存在顺反异构体
B.已知丙烷的二氯代物有四种异构体,则其六氯代物的异构体数目为六种
C.菲的结构简式为 ,它与硝酸反应,可生成4种一硝基取代物
,它与硝酸反应,可生成4种一硝基取代物
D.乙醛的核磁共振氢谱中有二个峰,峰面积之比是1:3
查看答案和解析>>
科目: 来源: 题型:
【题目】A,B,C,D,E均为有机化合物,A是分子式为C5H10O的直链化合物,B与NaHCO3溶液完全反应,其物质的量之比为1:2,它们之间的关系如图所示(提示:RCH=CHR′在酸性高锰酸钾溶液中反应生成RCOOH和R′COOH,其中R和R′为烷基).下列叙述错误的是( )
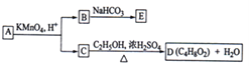
A.B的结构简式为HOOCCH2COOHB.C与乙醇发生了酯化反应
C.A可以与氢氧化钠溶液发生中和反应D.E的分子式为C3H2O4Na2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com