
科目: 来源: 题型:
【题目】室温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=2的溶液:Na+、Fe2+、I-、NO3-
B.c(AlO2-)=0.1 mol·L-1的溶液:K+、Na+、OH-、SO42-
C.![]() =0.1 mol·L-1的溶液:Na+、NH4+、SiO32-、ClO-
=0.1 mol·L-1的溶液:Na+、NH4+、SiO32-、ClO-
D.c(Fe3+)=0.1 mol·L-1的溶液:Mg2+、NH4+、Cl-、SCN-
查看答案和解析>>
科目: 来源: 题型:
【题目】MgCl2·6H2O可用于医药、农业等领域。一种用镁渣[含有MgCO3、Mg(OH)2、CaCO3、Fe2O3和SiO2]制备MgCl2·6H2O的实验流程如下:

(1)“煅烧”只有MgCO3、Mg(OH)2发生分解。“煅烧”须用到下列仪器中的________(填字母)。
A. 蒸发皿 B. 坩埚 C. 泥三角
(2) “蒸氨”在如图所示装置中进行(NH4Cl溶液仅与体系中的MgO反应)。

①三颈烧瓶中发生主要反应的离子方程式为______________。
②倒扣漏斗的作用是________________。
③烧杯中溶液红色深浅不再变化可判断“蒸氨”已完成,其原因是________________。
(3) “过滤”所得滤液经盐酸酸化、蒸发、结晶、过滤、洗涤和低温干燥得到产品。向所得产品中加入蒸馏水,测得溶液呈碱性,其可能原因是_________________。
(4) 请补充完整以“滤渣”为原料,制取FeSO4溶液的实验方案:边搅拌边向滤渣中加入1.0 mol·L-1盐酸,_________,得FeSO4溶液(实验中必须用的试剂:1.0 mol·L-1 NaOH溶液、1.0 mol·L-1 H2SO4溶液、铁粉、蒸馏水)。
已知部分金属离子形成氢氧化物沉淀的pH范围如下表:
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Ca2+ | 11.3 | — |
Mg2+ | 8.4 | 10.9 |
查看答案和解析>>
科目: 来源: 题型:
【题目】钛酸钡(BaTiO3)是电子陶瓷器件的重要基础原料。工业上以钛精矿(主要成分为TiO2)和BaCl2为主要原料制备钛酸钡粉体的工艺流程如下:

已知:①TiCl4水解生成H2TiO3沉淀;
②水溶液中含碳微粒随pH的分布如图所示。

(1) “氯化”在800 ℃时进行,其反应的化学方程式为________。
(2) “共沉淀”时,需控制溶液pH为10~11,其原因是:①___________;② ________。
(3) “滤液”中溶质的主要成分为________(填化学式)。过滤得到的固体通常用一定浓度的NH4HCO3溶液进行洗涤,其主要原因是___________。
(4) “煅烧”得到的钛酸钡粉体中钡钛质量比![]() ,钛酸钡粉体中可能含有的杂质为____________(填化学式)。
,钛酸钡粉体中可能含有的杂质为____________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物A是一种重要的化工原料,以A为主要起始原料,通过下列途径可以合成高分子材料PA及PC。

试回答下列问题
(1)B的化学名称为_____________,B到C的反应条件是_____________;
(2)E到F的反应类型为_____________,高分子材料PA的结构简式为_____________;
(3)由A生成H的化学方程式为_______________________________________;
(4)实验室检验有机物A,可选择试剂_____________或_____________;
(5)E的同分异构中,既能与碳酸氢钠溶液反应又能发生银镜反应的有机物共有_____________种。其中核磁共振氢谱图有5组峰,且峰面积之比为6:1:1:1:1的物质的结构简式为_____________;
(6)由B通过三步反应制备1,3-环己二烯的合成路线为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeCl3溶液在工业上用于蚀刻铜箔制造电路板。从蚀刻后的废液中可以回收铜并使蚀刻液再生。流程如下(部分物质有省略):

回答下列问题:
(1)氯化铁溶液蚀刻铜箔反应的离子方程式为_______________________________________。
(2)从固体中分离出铜,加入的试剂X可以是________________。
(3)使滤液再生为蚀刻液可采用的方法是___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】![]() 用于石油工业脱硫与脱色,是一种不溶于水和乙醇的白色粉末,在潮湿空气中可被迅速氧化。实验室用
用于石油工业脱硫与脱色,是一种不溶于水和乙醇的白色粉末,在潮湿空气中可被迅速氧化。实验室用![]() 混合溶液与
混合溶液与![]() 溶液反应制取
溶液反应制取![]() ,相关装置如图。回答以下问题:
,相关装置如图。回答以下问题:
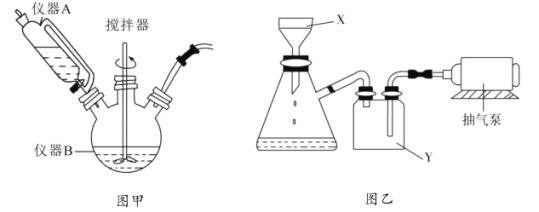
(1)图甲中仪器B的名称是__________,制备过程中![]() 过量会发生副反应生成
过量会发生副反应生成![]() ,为提高产率,仪器A中所加试剂应为__________________;
,为提高产率,仪器A中所加试剂应为__________________;
(2)丙图是体系pH随时间变化关系图,制取![]() 反应的离子方程式为____________,丁图是产率随pH变化关系图,实验过程中往往用
反应的离子方程式为____________,丁图是产率随pH变化关系图,实验过程中往往用![]() 混合溶液代替单一
混合溶液代替单一![]() 溶液,其中
溶液,其中![]() 的作用是____________;
的作用是____________;
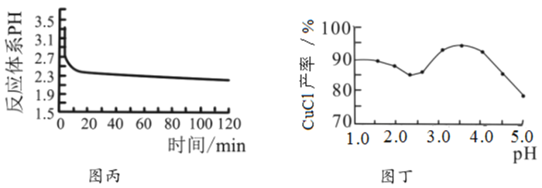
(3)反应完成后经抽滤、洗涤、干燥获得产品。抽滤装置如图乙所示,抽滤所用的仪器包括布氏漏斗、吸滤瓶、安全瓶和抽气泵。其中抽气泵的作用是使吸滤瓶与安全瓶中的____________________,跟常规过滤相比,采用抽滤的优点是____________(写一条);洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是__________________。
(4)![]() 不稳定易分解为
不稳定易分解为![]() ,
,![]() 时
时![]() 的
的![]() ,
,![]() 的
的![]() ,把
,把![]() 固体和
固体和![]() 溶液混合,加热,得到红色沉淀,该沉淀的化学式为___________。
溶液混合,加热,得到红色沉淀,该沉淀的化学式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验题。实验室有化学纯的浓硫酸,其试剂瓶标签上的部分内容如下图:
硫酸 化学纯(CP)
(500 mL)
品名:硫酸
化学式:H2SO4
相对分子质量:98
密度:1.84 g·cm-3
质量分数:98%
请回答下列问题:
(1)配制溶液时,一般可以分为以下几个主要步骤:
①量取 ②计算 ③溶解 ④定容 ⑤转移 ⑥洗涤 ⑦装瓶,其正确的操作顺序为________(填序号)。
(2)实验室只有100 mL、250 mL、500 mL三种规格的容量瓶,但要配制240 mL 0.1 mol·L-1的稀硫酸,需取该浓硫酸________ mL,计算所需浓硫酸的体积用到的公式___________。
(3)接下来完成此实验将用到的仪器有10 mL量筒、烧杯、玻璃棒、___________。
(4)要从所配溶液中取出50 mL盛装于试剂瓶中,给它贴上标签,则标签的内容是_________;若再从中取出10 mL溶液稀释至20 mL,则稀释后溶液的物质的量浓度为________。
(5)下列操作会使所配溶液浓度偏高的是____(填字母)。
A 转移溶液时未洗涤烧杯
B 定容时俯视容量瓶的刻度线
C 容量瓶用蒸馏水洗净后仍残留有蒸馏水
D 用量筒量取浓硫酸,读数时仰视刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】I。草酸(H2C2O4)与高锰酸钾在酸性条件下能够发生反应:
(实验1)甲同学用8.00 mL 0.001 mol/L KMnO4溶液与5.00 mL 0.01 mol/L H2C2O4溶液反应,研究不同条件对化学反应速率的影响。改变的条件如下:
组别 | KMnO4溶液 /mL | H2C2O4溶液 /mL | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 8.00 | 5.00 | 3.00 | 20 | |
Ⅱ | 8.00 | 5.00 | 3.00 | 30 | |
Ⅲ | 8.00 | 5.00 | 1.00 | 20 | 2.00 mL蒸馏水 |
(1)写出草酸(H2C2O4)与高锰酸钾溶液在酸性条件下反应的离子方程式________。
(2)上述进行实验Ⅰ、Ⅲ的目的是探究__________对化学反应速率的影响。
(实验2)乙同学在研究草酸与高锰酸钾在酸性条件下反应的影响因素时发现,草酸与酸性高锰酸钾溶液开始一段时间反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
(3)针对上述现象,乙同学认为草酸与高锰酸钾反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是_______的影响。
(4)若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是____(填字母)。
a.硫酸钾 b.水 c.二氧化锰 d.硫酸锰
Ⅱ.用如图所示的装置进行中和热的测定实验,分别取![]() 的
的![]() 溶液、
溶液、![]() 的硫酸进行实验,回答下列问题:
的硫酸进行实验,回答下列问题:
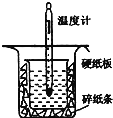
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是__________,除此之外,装置中的一个明显错误是__________。
(2)近似认为![]() 的NaOH溶液和
的NaOH溶液和![]() 的硫酸溶液的密度都是
的硫酸溶液的密度都是![]() ,中和后生成溶液的比热容
,中和后生成溶液的比热容![]() ,通过以下数据计算中和热△H=__________(结果保留小数点后一位)。
,通过以下数据计算中和热△H=__________(结果保留小数点后一位)。
温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | ||
H2SO4 | NaOH | 平均值 | ||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
2 | 27.0 | 27.4 | 27.2 | 32.3 |
3 | 25.9 | 25.9 | 25.9 | 29.2 |
4 | 26.4 | 26.2 | 26.3 | 29.8 |
(3)上述实验数值结果与![]() 有偏差,产生偏差的原因可能是(填字母)_____。
有偏差,产生偏差的原因可能是(填字母)_____。
a.实验装置保温、隔热效果差
b.用温度计测定![]() 溶液起始温度后直接测定H2SO4溶液的温度
溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把![]() 溶液倒入盛有硫酸的小烧杯中
溶液倒入盛有硫酸的小烧杯中
d.将以上四实验测量温度均纳入计算平均值
查看答案和解析>>
科目: 来源: 题型:
【题目】AA705合金(含![]() 和
和![]() )几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
)几乎与钢一样坚固,但重量仅为钢的三分之一,已被用于飞机机身和机翼、智能手机外壳上等。回答下列问题:
(1)![]() 和
和![]() 中阳离子基态核外电子排布式为_____________________,
中阳离子基态核外电子排布式为_____________________,![]() 三种元素的第一电离能由大到小为_____________________;
三种元素的第一电离能由大到小为_____________________;
(2)以![]() 和抗坏血酸为原料,可制备
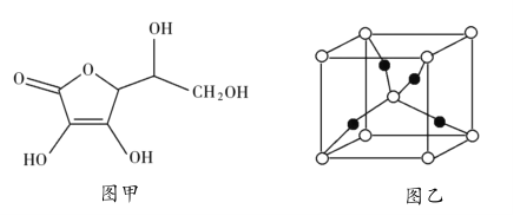
和抗坏血酸为原料,可制备![]() 。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为_______________,推测抗坏血酸在水中的溶解性:_______________(填“难溶于水”或“易溶于水”),一个
。抗坏血酸的分子结构如图1所示,分子中碳原子的轨道杂化类型为_______________,推测抗坏血酸在水中的溶解性:_______________(填“难溶于水”或“易溶于水”),一个![]() 晶胞(见图2)中,
晶胞(见图2)中,![]() 原子的数目为_______________;
原子的数目为_______________;
(3)![]() 和
和![]() 等配体都能与
等配体都能与![]() 形成配离子。
形成配离子。![]() 含______
含______![]() 键,中心离子的配位数为______________;
键,中心离子的配位数为______________;
(4)![]() 因杀虫效率高、廉价易得而被广泛应用。已知
因杀虫效率高、廉价易得而被广泛应用。已知![]() 的熔点为2000℃,其晶胞结构如图所示。
的熔点为2000℃,其晶胞结构如图所示。
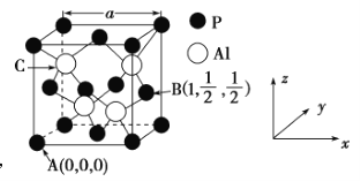
①磷化铝的晶体类型为______________,
②A、B点的原子坐标如图所示,则C点的原子坐标为___________,
③磷化铝的晶胞参数![]() ,其密度为____________
,其密度为____________![]() (列出计算式即可,用
(列出计算式即可,用![]() 表示阿伏加德罗常数的值);
表示阿伏加德罗常数的值);
(5)![]() 具有对称的立体构型,
具有对称的立体构型,![]() 中的两个
中的两个![]() 被两个
被两个![]() 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则![]() 的空间构型为________________。
的空间构型为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】烟气的脱硝(除![]() )技术和脱硫(除
)技术和脱硫(除![]() )技术都是目前环境科学研究的热点。
)技术都是目前环境科学研究的热点。
(1)工业上可以采用“质子膜电解槽”对烟气进行脱硫脱硝,其工艺如图甲所示:
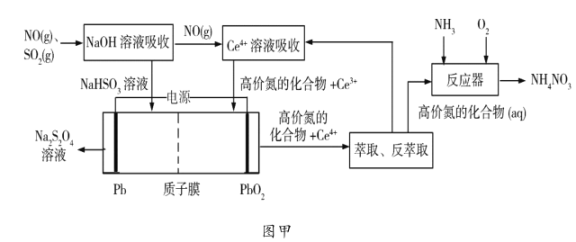
①![]() 溶液吸收
溶液吸收![]() 主要反应的化学方程式为___________;
主要反应的化学方程式为___________;
②电解的主要目的是______________,阴极的电极反应式为______________;
③“高价氮的化合物”中NO2在反应器中发生化合反应的化学方程式为______;
(2)利用活性焦炭的吸附作用,可以对烟气进行脱硫和脱硝。被吸附的![]() 与活性焦炭反应生成
与活性焦炭反应生成![]() 和
和![]() ,当生成
,当生成![]() 时,转移电子的物质的量为__________
时,转移电子的物质的量为__________![]() ;
;
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入![]() 的
的![]() 乳浊液中,发生的反应如下:
乳浊液中,发生的反应如下:![]() ,
,![]() ,改变
,改变![]() ,
,![]() 的去除率变化情况如图乙所示。
的去除率变化情况如图乙所示。
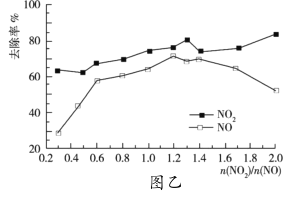
①当![]() 大于1.4时,
大于1.4时,![]() 去除率升高,但
去除率升高,但![]() 的去除率却降低。其可能的原因是__;
的去除率却降低。其可能的原因是__;
②![]() 和
和![]() 发生的主要反应为
发生的主要反应为![]() 。保持
。保持![]() 的初始浓度不变,改变
的初始浓度不变,改变![]() ,将反应后的混合气体通入
,将反应后的混合气体通入![]() 乳浊液中吸收。为节省
乳浊液中吸收。为节省![]() 的用量,又能保持
的用量,又能保持![]() 去除效果,则
去除效果,则![]() 合适的值约为___________;
合适的值约为___________;
(4)已知:![]() ,
,![]() ,则
,则![]() ______________________。
______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com