
科目: 来源: 题型:
【题目】乳酸亚铁晶体{[CH3CH(OH)COO]2Fe3H2O}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3 反应制得:2CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe3H2O+CO2↑。
Ⅰ.制备FeCO3:装置如图所示。
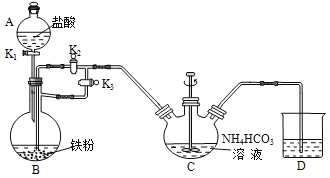
(1)B的名称是____。
(2)①清洗仪器,检查装置气密性的方法是:在D处导管末端套上夹止水夹的橡胶管,在A中加入水,分别打开活塞K1和K3。关闭活塞K2,若观察到___,则气密性良好。
②倒掉A中的水,加入盐酸,在B中加入铁粉、C中加入NH4HCO3溶液。关闭活塞K2,打开活塞K1和K3;滴入足量盐酸后,关闭活塞K1,开动搅拌器,反应一段时间后关闭活塞K3,打开活塞K2,C中发生的反应的离子方程式为____。
Ⅱ.制备乳酸亚铁晶体:将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应。然后再加入适量乳酸。
(3)加入少量铁粉的作用是___。从所得溶液中获得乳酸亚铁晶体所需的实验操作是:隔绝空气低温蒸发,冷却结晶,____、洗涤、干燥。
查看答案和解析>>
科目: 来源: 题型:
【题目】近年科学家提出“绿色自由”构想。把空气中的CO2进行转化,并使之与H2反应生成可再生能源甲醇。
(1)工业生产中可利用H2还原CO2制备清洁能源甲醇。
①下列关于氢能的说法正确的是____。
A.氢能是清洁能源 B.氢能是二次能源
C.氢能是不可再生能源 D.气态氢能源更容易保存和运输
②已知CO(g)和H2(g)的燃烧热(△H)分别为-283.0kJmol-1、-285.8kJmol-1。CO与H2合成甲醇的能量变化如图甲所示:
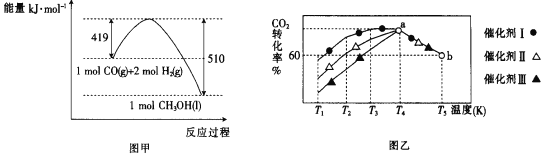
则用CO2(g)和H2(g)制备液态甲醇的热化学方程式为____。
③将一定量的CO2和H2充入到某恒容密闭容器中,测得在不同催化剂作用下,相同时间内CO2的转化率与温度的变化如图乙所示:催化效果最好的是催化剂____(选填“Ⅰ”“Ⅱ”或“Ⅲ”)。
(2)利用CO和水蒸气可生产H2,反应的化学方程式:CO(g)+H2O(g)CO2(g)+H2(g)。将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行如下反应,得到三组数据如表所示:
温度/℃ | 起始量 | 达到平衡 | |||
CO/mol | H2O/mol | H2/mol | CO转化率 | 时间/min | |
650 | 4 | 2 | 1.6 | 10 | |
900 | 3 | 2 |
| 5 | |
900℃时,达到平衡时的反应速率v(H2O)=____。(保留2位小数)。
(3)科学家还研究了其他转化温室气体的方法,利用如图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为____。
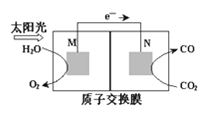
查看答案和解析>>
科目: 来源: 题型:
【题目】冠病毒(如图)由蛋白质和核酸组成,核酸由核苷酸组成.核苷酸的单体由五碳糖 、磷酸基和含氮碱基构成.下列说法错误的是
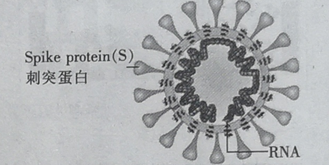
A.蛋白质和核酸均是高分子化合物
B.蛋白质中含C、H、O、N 等元素
C.五碳糖( C5H10O5)与葡萄糖互为同系物
D.NaClO溶液用作消毒剂,是因为NaClO 能使病毒蛋白变性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式中的∣△H∣能表示可燃物的燃烧热的是( )
A.H2(g)+![]() O2(g)=H2O(1)△H=-285.8kJ/mol-1
O2(g)=H2O(1)△H=-285.8kJ/mol-1
B.H2(g)+C12(g)=2HCl(g)△H=-184.6kJ/mol-1
C.2CO(g)+O2(g)=2CO2(g)△H= 一566kJ/mol-1
D.CH4(g)+2O2(g)=2H2O(g)+CO2(g)△H= 一802.3kJ/mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是
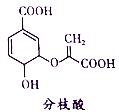
A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目: 来源: 题型:
【题目】Zn3(PO4)2·2H2O(溶于酸,难溶于水)是一种无毒害作用的防锈颜料,利用锌浮渣(主要含Zn、ZnO、ZnCl2,还含少量的铁、锰、铜、铅及砷的化合物等)制取Zn3(PO4)2·2H2O的工艺流程如图:
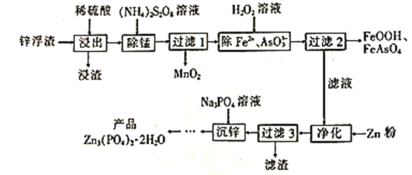
回答下列问题:
(1)“浸出”时,下列措施能提高锌的浸取率的是__(填字母)。
A.用浓硫酸代替稀硫酸 B.适当升高浸取液的温度
C.将“浸渣”再次浸取 D.缩短“浸出”时间
(2)“除锰”时,Mn2+发生反应的离子方程式为__(S2O![]() 被还原为SO
被还原为SO![]() )。
)。
(3)流程中除铁、砷时,当生成8.9gFeOOH和7.8gFeAsO4时,消耗H2O2__mol。
(4)“净化”时加锌粉的目的是__。
(5)“沉锌”时发生反应的化学方程式为__。
(6)“沉锌”至得到“产品”还需要经过的操作是__、洗涤、__。证明产品已洗涤干净的实验方法是__。
(7)Meyer等认为磷酸锌防腐机理是在钢铁表面形成组成近似为Zn2Fe(PO4)2·4H2O的覆盖膜,则在形成该覆盖膜的过程中,负极的电极反应式为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。M、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01 mol·L-1 r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )
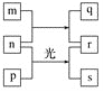
A.W、X组成的化合物只含有极性共价键
B.Y的氢化物常温常压下为液态
C.元素的非金属性Z>X>Y
D.X的最高价氧化物的水化物为强酸
查看答案和解析>>
科目: 来源: 题型:
【题目】1,3—环己二酮(![]() )常用作医药中间体,用于有机合成。1,3—环己二酮的一种合成路线如图所示。
)常用作医药中间体,用于有机合成。1,3—环己二酮的一种合成路线如图所示。
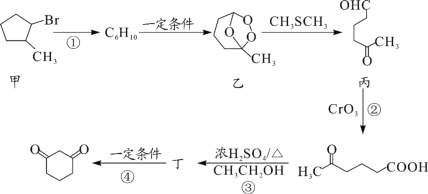
回答下列问题:
(1)甲的分子式为___。
(2)丙中含有官能团的名称是___。
(3)反应①所需的试剂和条件是___;②的反应类型是___。
(4)丁的结构简式为___。
(5)写出丙与新制氢氧化铜悬浊液反应的化学方程式___。
(6)符合下列条件的乙的同分异构体共有___种。
①能发生银镜反应
②能与NaHCO3溶液反应
其中核磁共振氢谱峰面积之比为1∶1∶2∶6的一种同分异构体的结构简式为___(任写一种)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:
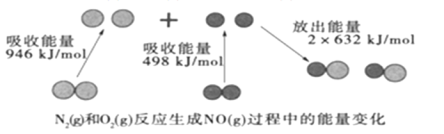
下列说法中正确的是( )
A.1molN2(g)和1molO2(g)完全反应放出的能量为180kJ
B.通常情况下,N2(g)和O2(g)混合能直接生成NO
C.1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目: 来源: 题型:
【题目】苯甲酸乙酯(C9H10O2)稍有水果气味,用于配制香水香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为
![]() +C2H5OH
+C2H5OH![]()
 +H2O
+H2O
已知:
物质 | 颜色、状态 | 沸点(℃) | 密度(g·cm-3) | 相对分子质量 |
苯甲酸 | 无色、片状晶体; 100℃会迅速升华 | 249 | 1.2659 | 122 |
苯甲酸乙酯 | 无色澄清液体 | 212.6 | 1.05 | 150 |
乙醇 | 无色澄清液体 | 78.3 | 0.7893 | 46 |
环己烷 | 无色澄清液体 | 80.8 | 0.7318 | 84 |
实验步骤如下:
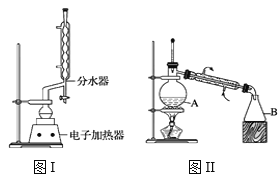
①在100mL圆底烧瓶中加入12.20g苯甲酸、25mL乙醇(过量)、20mL环己烷,以及4mL浓硫酸,混合均匀并加入沸石,按图I所示装好仪器,控制温度在65~70℃加热回流2h。反应时环己烷—乙醇—水会形成“共沸物”(沸点62.6℃)蒸馏出来。再利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中液体后,关闭旋塞。继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入Na2CO3至溶液呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并有机层。加入氯化钙,对粗产品进行蒸馏(装置如图II所示)。低温蒸出乙醚后继续升温,接收span>210~213℃的馏分。
⑤检验合格,测得产品体积为12.86mL。
(1)步骤①中加入沸石的目的是______;使用分水器不断分离除去水的目的是___。
(2)步骤②中继续加热的温度应控制在____(填标号)。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(3)步骤③中若Na2CO3加入不足,在步骤④蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是____。
(4)步骤④中分液操作叙述正确的是___(填标号)。
A.向盛有水层的分液漏斗中加入乙醚,盖好玻璃塞,将分液漏斗倒转,用力振荡
B.振荡几次后需打开分液漏斗的下口活塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.液体分层后,将分液漏斗上的玻璃塞打开,或使塞上的凹槽对准漏斗上的小孔
E.分液操作时,分液漏斗中的下层液体由下口放出,然后再将上层液体由下口放出
(5)图II中仪器A的名称是___,步骤④中氯化钙的作用是___。
(6)该实验产品的产率为___(结果保留三位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com