
科目: 来源: 题型:
【题目】已知反应①2BrO3-+Cl2=Br2+2ClO3-;②5Cl2+I2+6H2O=2HIO3+10HCl;③ClO3-+5Cl-+6H+=3Cl2+3H2O。下列物质氧化能力强弱顺序正确的是
A.![]() B.
B.![]()
C.![]() D.
D.![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年5月23日,《南阳日报》发消息称,“水氢发动机”在当地下线,文中称,“车载水可以实时制取氢气,车辆只需加水即可行驶。”文章发布后引发广泛质疑。据报道,该发动机的核心原理是用铝粉与水进行反应得到氢气,作为发动机的燃料。美军曾经报道过“尿氢能”技术,与“水氢汽车”的原理如出一辙,纳米铝粉加尿可得大量氢气,且用尿液与铝粉反应的产氢速率比正常的水高出一倍。下列说法不正确的是( )
A.常温下铝和水的反应不能自发反应,将铝加工为精细铝粉,增大了反应接触面积,使该反应变为自发反应
B.推测尿液与铝粉反应比水快的可能原因是因为尿液呈弱酸性,金属与酸反应速率加快
C.水作为铝的氧化剂的缺点是反应生成的氢氧化铝或氧化铝会吸附在铝表面,阻碍反应进行
D.若需得到标况下体积为10L的氢气,加入的铝粉至少为8.0g
查看答案和解析>>
科目: 来源: 题型:
【题目】在下列反应中,单质只作氧化剂的是
A.2F2+2H2O═4HF+O2↑
B.Cl2+2NaOH═NaCl+NaClO+H2O
C.2Na+2H2O═2NaOH+H2↑
D.H2+CuO![]() H2O+Cu
H2O+Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】下表中各组物质不能实现如图所示转化的是
![]()
选项 | 甲 | 乙 | 丙 |
A | CO2 | NaHCO3 | Na2CO3 |
B | AlCl3 | Al2O3 | NaAlO2 |
C | AlCl3 | Al | Al(OH)3 |
D | AlCl3 | Al(OH)3 | NaAlO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与足量很稀的硝酸充分反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列说法不正确的是( )
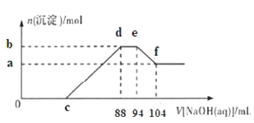
A.硝酸的还原产物全部是![]() B.b点与a点的差值为0.05mol
B.b点与a点的差值为0.05mol
C.原硝酸溶液中硝酸的物质的量为0.47molD.样品中铝粉和铁粉的物质的之比为5:3
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
A. 用CCl4提取溴水中的Br2
用CCl4提取溴水中的Br2
B. 除去乙醇中的四氯化碳
除去乙醇中的四氯化碳
C. 从KI和I2的固体混合物中回收I2
从KI和I2的固体混合物中回收I2
D. 配制100mL 0.1000molL-1的NaCl溶液
配制100mL 0.1000molL-1的NaCl溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.常温常压下,14 g N2含有分子数为NA
B.过氧化钠与水反应,生成0.1 mol氧气时,转移的电子数为0.2NA
C.物质的量浓度为0.5 mol/L的MgCl2溶液,含有Cl-数目为1NA
D.一定条件下,0.01 mol FeCl3与水完全反应制成胶体,其含有的Fe(OH)3胶粒数为0.01 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】四种短周期元素W、X、Y、Z,原子序数依次增大,请结合表中信息回答下列问题。
W | X | Y | Z | |
结构 | 最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物 | 焰色反应呈黄色 | 在同周期主族元 | 最高正价与最 |
(1)Z在元素周期表中位于 族。
(2)上述元素的最高价氧化物对应的四种水化物中,有一种物质在一定条件下均能与其它三种物质发生化学反应,该元素是 (填元素符号)。
(3)①下列可作为比较X和Y金属性强弱的依据是 (填序号)。
A.自然界中的含量 B.相应氯化物水溶液的pH
C.单质与水反应的难易程度 D.单质与酸反应时失去的电子数
②W、X、Y的离子半径由大到小的顺序为 。(填对应的离子符号)
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸相似。体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是 ,混合后溶液中离子浓度由大到小的顺序是 。
(5)Y单质和Mg组成的混合物是一种焰火原料,某兴趣小组设计如下所示的实验方案,测定混合物中Y的质量分数。

能确定混合物中Y的质量分数的数据有 (填序号)。
A.m、n B.m、y C.n、y
查看答案和解析>>
科目: 来源: 题型:
【题目】以硫铁矿(主要成分为FeS2)为原料制备硫酸亚铁晶体(FeSO4xH2O)的工艺流程如下:
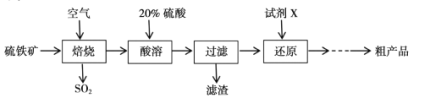
(1)已知焙烧后得到的固体主要成分为Fe2O3。写出焙烧过程主要反应的化学方程式____。
(2)写出酸溶过程主要反应的离子方程式____。
(3)试剂X是(写化学式)____。
(4)从还原得到的溶液中获得硫酸亚铁晶体(FeSO4xH2O)的操作是____
(5)利用如图装置测定FeSO4xH2O中结晶水含量:
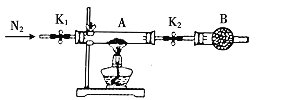
实验前通入N2,的主要目的是____,装置B中盛放的试剂是____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com